Clear Sky Science · ja
Th17細胞はマウスモデルにおける酸化的DNA損傷を制御するためにDNA修復センサーXPCを必要とする
免疫防御者の守り手
ヘルパーT細胞の一種であるTh17細胞は、腸や皮膚などのバリアを巡回して細菌や真菌を排除する特殊な白血球です。しかし、その応答が暴走すると自己免疫疾患にも関与します。本研究は一見単純な問いを投げかけます:感染と戦う過程で自ら生み出す化学的ストレスから、こうした高活性の細胞はどのように自分たちのDNAを守っているのか?答えは、主に皮膚細胞の紫外線ダメージ保護で知られるDNA損傷センサーXPCにあります。ここで示されたのは、XPCがTh17細胞の健康、エネルギー、機能維持に不可欠であるということです。
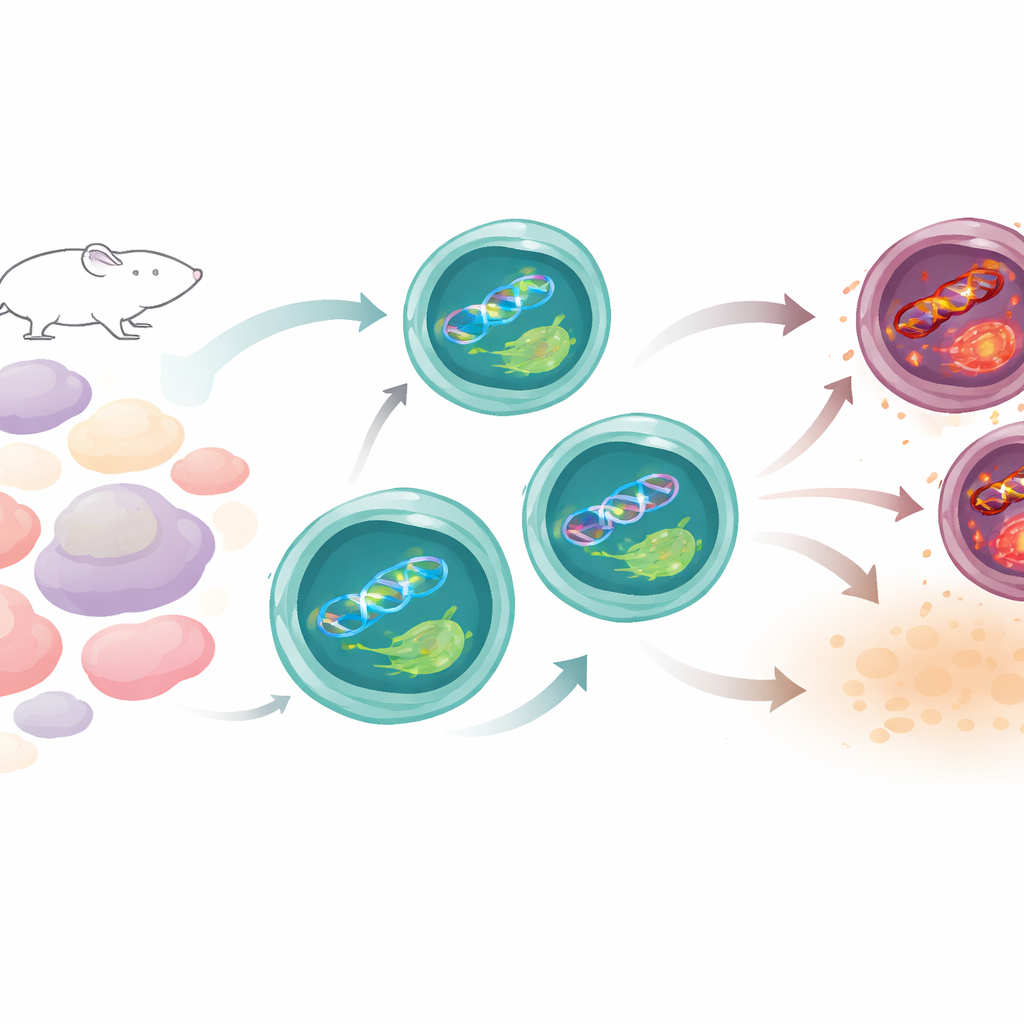
Th17細胞が通常どのように均衡を保つか
Th17細胞は危険な生活を送っています。機能するために代謝を高め、DNAを傷つけうる活性酸素種を産生します。研究チームはマウスのTh17細胞と他のT細胞型を比較し、強い活動性にもかかわらずTh17細胞は多くの同胞よりもDNA損傷をあまり蓄積しないことを見出しました。重要な手がかりは、特に日焼けで生じる損傷を修復する経路に属する遺伝子群がTh17でより強く発現していた点です。その中にはDNAの構造的損傷をスキャンするタンパク質XPCも含まれていました。Th17細胞が成熟するにつれてXPCの量が増え、核内の損傷部位に局在することから、遺伝的完全性を維持するために常時見回りしていることが示唆されます。
DNAセンサーが欠けると何が起きるか
XPCの重要性を確かめるために、研究者たちはこのタンパク質を欠くように設計したマウスを用いました。一見すると免疫系はほぼ正常に見え、全体的なT細胞数や多くのT細胞サブタイプに変化はありませんでした。しかしTh17細胞に注目すると著しい欠陥が明らかになりました。XPCがないと、はるかに少ない細胞しかTh17の代表的分子であるIL-17を産生せず、Th17プログラムを駆動する主要な同一性マーカーやシグナルスイッチが抑えられていました。培養皿内では、これらのマウス由来のナイーブT細胞は完全なTh17へと分化するのに苦労しました。移入したT細胞が腸炎を誘導する標準モデルでは、XPC欠損のT細胞は大腸炎を引き起こせず、炎症誘導能が低下していることが反映されました。同時に、免疫応答を抑える制御性T細胞が増加しており、攻撃と抑制のバランスが変化していることを示唆しています。
DNA損傷、エネルギー産生装置、化学的ストレス
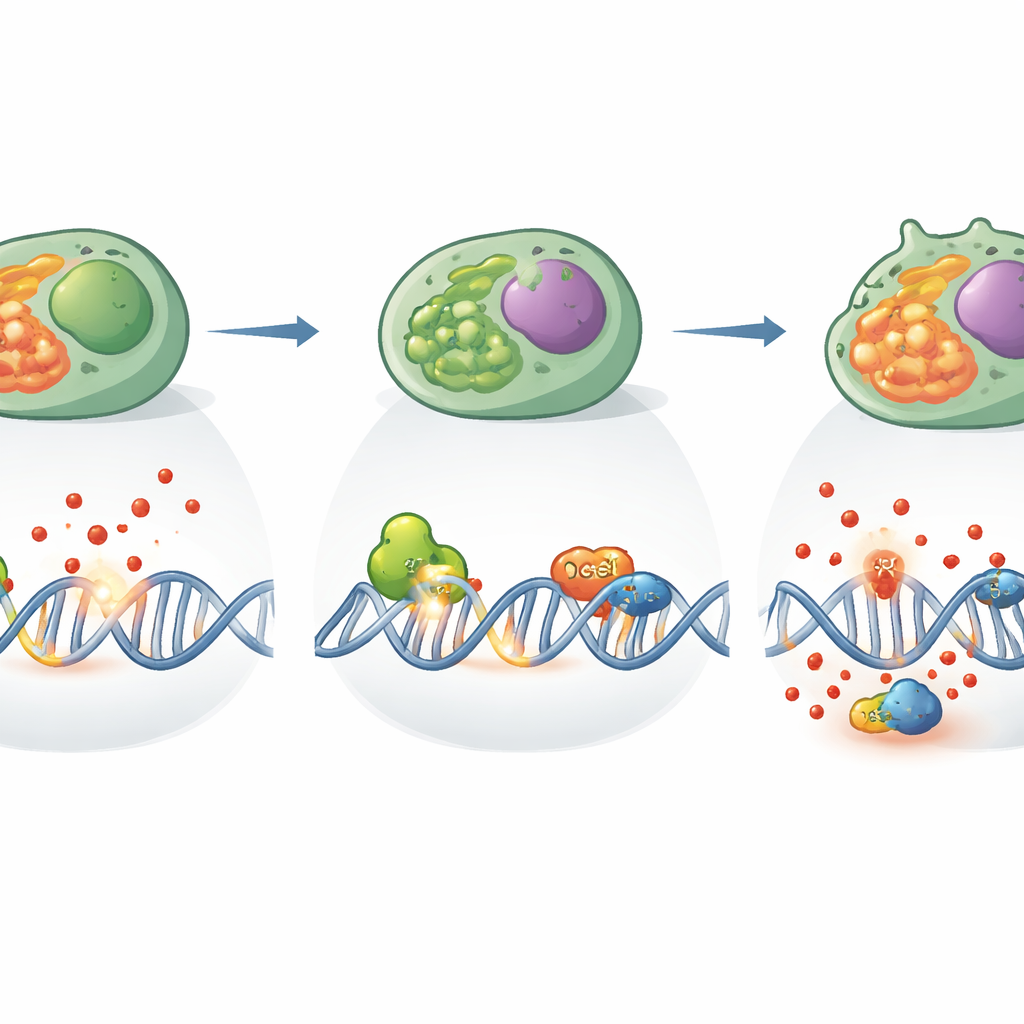
さらに掘り下げると、XPCを欠くTh17細胞は切断されたDNA鎖や酸化されたDNA塩基をより多く抱えており、これは活性酸素種による攻撃の特徴です。通常DNA損傷を感知して細胞周期を停止させる遺伝子群の発現も低下しており、警報システムが弱まっていることが示されました。細胞のエネルギー代謝は再構成され、速く燃える糖代謝経路の一部を失い、細胞内の小さな発電所であるミトコンドリアにより依存するようになりました。しかしミトコンドリアはより多くの活性酸素種を漏出し、疲弊の兆候を示しており、化学的ストレスの増加とDNA損傷の悪循環を生み出していました。注目すべきことに、抗酸化剤で処理するとIL-17産生が回復しDNA損傷が減少し、酸化ストレスが観察された機能不全に直接関与していることが示されました。
損傷DNA修復におけるチームワーク
古典的役割を越えて、XPCは一般的な酸化塩基を認識する修復タンパク質OGG1とも連携して働きました。研究者たちはこれら二つのタンパク質がTh17細胞内で物理的に結合し、損傷した塩基の除去を協調していることを示しました。XPCが欠けるとOGG1の切断活性は実際に増加し、過剰な損傷に対して代償しようとしているかのようでした。しかしこの過剰活性は高い酸化ストレスと崩れた修復ネットワークのもとで起こっており、正常なTh17機能を回復するには不十分でした。遺伝学的および構造的解析は、XPCが異なる修復経路とレドックス制御をつなぐハブとして機能し、損傷を検出するだけでなく、細胞が分裂を続け保護分子を産生できるように処理されることを保証していることを示唆しました。
疾病と治療にとっての意義
一般読者に向けた主なメッセージは、免疫細胞が私たちを守る間に健全さを保つために内部のボディガードを必要とする、ということです。本研究は、かつて皮膚細胞を紫外線から守ることで有名だったXPCが、Th17細胞の重要な守護者でもあり、酸化ストレス下でDNAを保ちエネルギー系を均衡させていることを明らかにしました。XPCが欠けるとTh17細胞は遺伝的・代謝的に脆弱になり、炎症性産出が減少し、攻撃よりも制御に免疫バランスが傾く可能性があります。Th17細胞は炎症性腸疾患、乾癬、多発性硬化症などの病態で中心的役割を担うため、XPCが制御する経路は、これらの細胞がDNAを修復し酸化ストレスに対処する仕組みを調節することで、有害な炎症を鎮める、あるいは防御を強化する新たな免疫調節の標的になり得ます。
引用: Leite, J.A., Bos, N.N., Menezes-Silva, L. et al. Th17 cells require the DNA repair sensor xeroderma pigmentosum complementation Group C to control oxidative DNA damage in a murine model. Nat Commun 17, 3157 (2026). https://doi.org/10.1038/s41467-026-69914-y
キーワード: Th17細胞, DNA修復, 酸化ストレス, XPCタンパク質, 自己免疫疾患