Clear Sky Science · ja
がん治療法としての文脈依存的翻訳阻害
タンパク質工場をがんに向ける
がん細胞は、増殖と分裂を維持する短命の“ドライバー”タンパク質を大量に継続的に合成することで生き延びています。本研究は、リボソームという細胞のタンパク質合成機構を微妙に“詰まらせる”ことでがんと戦う新たな手法を探ります。しかも特定の配列を合成しようとする場合に限って作用し、特にMYCのような薬剤化が難しいオンコジーンに見られる配列に対して選択的に干渉します。その選択的阻害により、腫瘍細胞を死滅させつつ正常なタンパク質合成の多くを温存できる可能性があります。
細胞がタンパク質を作る仕組み—そしてどこが問題になりうるか
すべての細胞は、遺伝情報(mRNA)を読み取りアミノ酸をつなげてタンパク質を合成する小さな分子工場、リボソームに依存しています。抗生物質や従来のがん薬のようにリボソームを標的にする既存薬の多くは、鈍い道具のように作用し、タンパク質合成を広範に停止させてしまうため、健康な細胞にも損傷を与え深刻な副作用を生じることがあります。著者らは、新生ポリペプチド鎖それぞれが固有の配列と化学的性質を持つことを利用し、特定の配列がリボソーム内にある場合にのみリボソームを遮断する小分子を設計できる可能性があると考えました。これにより細胞全体のタンパク質生産を大きく損なうことなく選択的に作用させられるかもしれません。
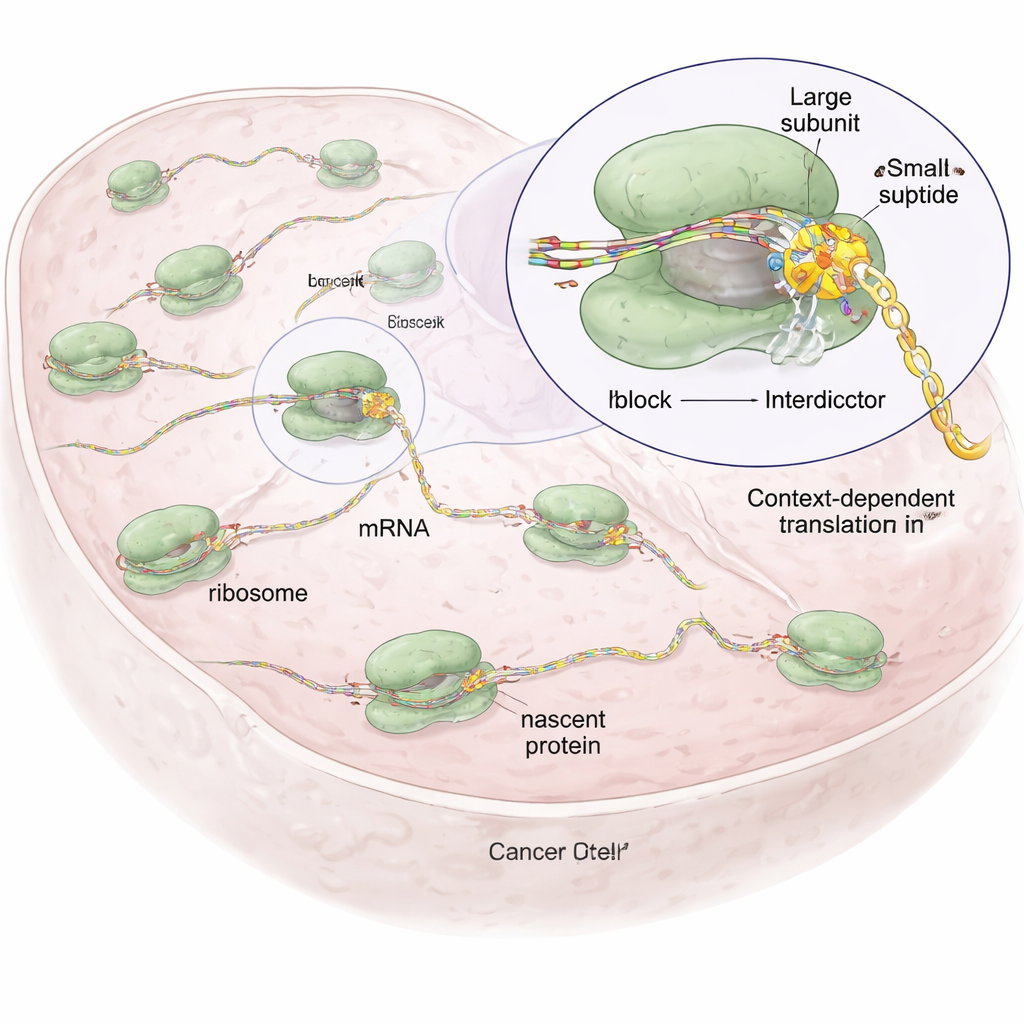
特定のタンパク質配列だけを止めるデザイナ―分子
ペプチド結合が形成されるリボソームの触媒部位に結合する天然化合物アニソマイシンを出発点として、研究者たちは「インターディクター(阻害子)」と呼ぶ一群の合成分子を作り出しました。これらは共通のコア骨格でリボソーム内に固定されますが、成長中のポリペプチド鎖に向かって伸びる側鎖が異なります。側鎖は特定の種類のアミノ酸を好むように調整されており、たとえば一つのインターディクター(IDB‑001)は負に帯電した残基に引き寄せられ、別の(IDB‑002)は小さく疎水的な残基を好みます。リボソームプロファイリングと呼ばれる手法で、細胞内のmRNA上でリボソームがどこで一時停止するかを全体的にマップしたところ、各化合物が新生鎖の短い特定モチーフで停止を引き起こし、しばしば末端から一つ前(−1)のアミノ酸で止めることが示されました。これは無差別な停止ではなく配列依存的な作用を示しています。
薬とリボソームの出会いを原子単位で観る
この選択性が物理的にどのように働くかを解明するために、著者らは設計したペプチド配列を翻訳中のヒトリボソームを凍結し、クライオ電子顕微鏡で準原子分解能の像を得ました。インターディクターがリボソームの活性部位に収まり、新生鎖の最後の数個のアミノ酸と精密に接触している様子が観察されました。ある構造では、IDB‑002の疎水性側鎖がペプチド中の小さくかさばらない残基に抱かれており、そこで大きな側鎖が不利になる理由を説明します。別の構造では、MYC由来の酸性側鎖がIDB‑001の正に帯電した基と塩橋を形成するために向きを変えます。薬の存在は近傍のリボソームrRNA塩基を新しい位置に押しやり、活性部位を狭め次のtRNAの挿入を部分的に妨げることで、こうした好まれた配列での伸長停止を助けていることも分かりました。
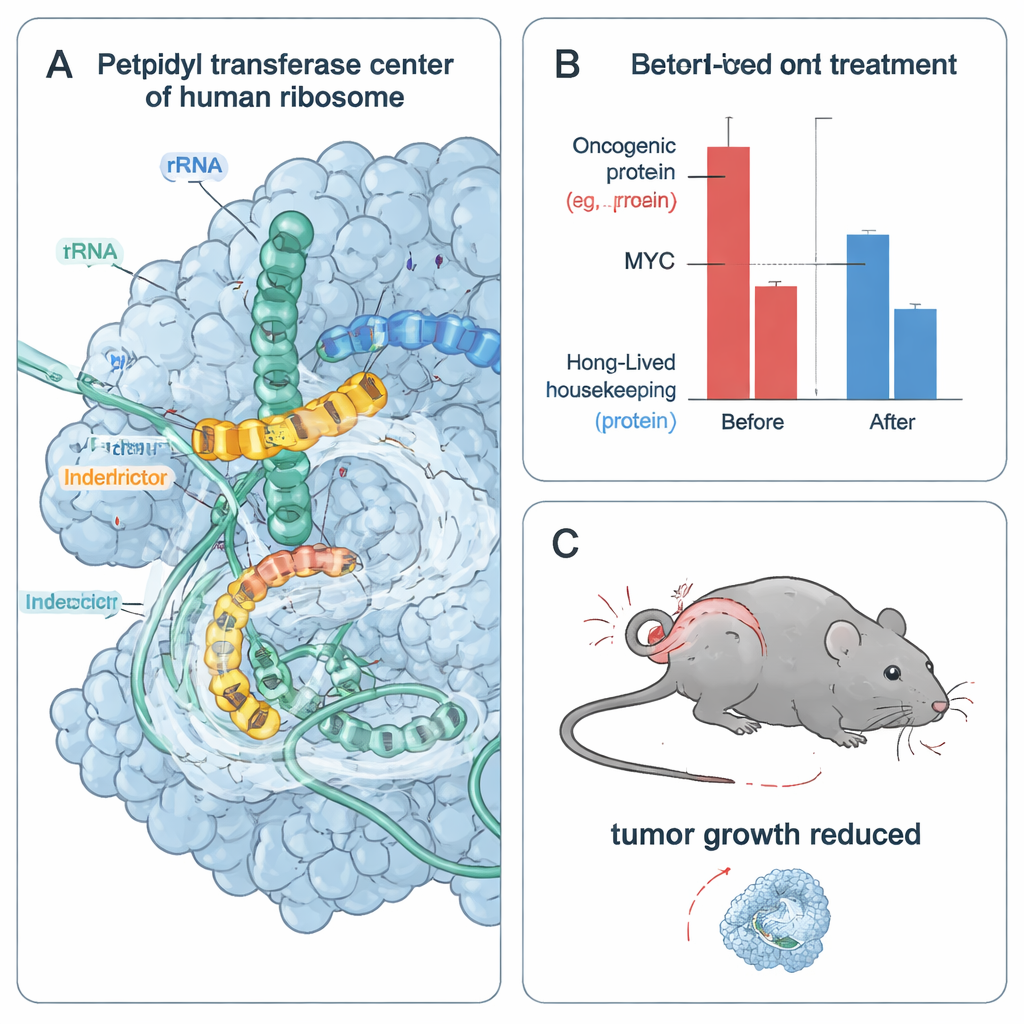
停止したリボソームからストレスを受け死滅する腫瘍細胞へ
急速に分裂するがん細胞はMYCやCCND1のような短命の腫瘍促進タンパク質に強く依存しているため、研究チームはインターディクターが腫瘍細胞の生存に与える影響を検証しました。複数のMYC依存性がん細胞株で、IDB‑001とIDB‑002はナノモーラーから低マイクロモーラーの濃度で細胞生存率を低下させました。さらに最適化したアナログIDB‑003はより強力で経口投与に適していました。細胞内ではこれらの化合物がMYCやほかのターンオーバーの速いオンコタンパク質を迅速に枯渇させる一方で、同じ時間枠では寿命の長いハウスキーピングタンパク質は比較的安定に保たれました。薬はまた衝突したリボソームに関連する細胞ストレス応答を誘導しましたが、これらのストレスシグナル経路を遮断しても生存率低下は解消されず、重要な腫瘍性タンパク質の直接的な枯渇が腫瘍細胞死の主要因であることを示唆しています。
困難な乳がんモデルでの概念実証
このアプローチが動物で機能するかを試すため、著者らはヒト由来トリプルネガティブ乳がん腫瘍を有するマウスに経口投与でIDB‑003を投与しました。28日間で投与群の腫瘍は対照群より著しく増殖が遅く、高用量では最大80%の腫瘍増殖抑制が観察され、本研究では深刻な毒性は報告されませんでした。腫瘍の遺伝子発現解析ではMYC標的遺伝子プログラムの強い下方制御が示され、in vivoでのMYC活性低下と一致しました。これらの結果は、特定のタンパク質配列でリボソームを選択的に止めることで、不安定な腫瘍ドライバーに依存する腫瘍を弱体化させ、古典的な翻訳阻害薬の広範な毒性を回避できる可能性を示しています。
将来のがん治療にとっての意義
本研究は従来と異なる種類の小分子薬を提示します。完成したタンパク質に結合するのではなく、タンパク質が作られている過程でそれを傍受し、短い“住所タグ”配列が存在する場合にだけ作用する薬です。多くのがん促進タンパク質は柔軟で短命であったり、従来の薬が狙える明確なポケットを欠いているため、それらの合成をリボソームで直接標的にすることは、MYCのような現在“非ドラッガブル”とされる遺伝子によって駆動される腫瘍の治療への道を開く可能性があります。また、インターディクターの化学を調整することで、将来の医薬品は異なる配列モチーフや疾患ターゲットに焦点を当てるよう設計でき、この戦略をがん以外の、特定のタンパク質の抑制が健康回復につながる状況へ拡張することが示唆されます。
引用: Diamond, P.D., Sauer, P.V., Holm, M. et al. Context-dependent translation inhibition as a cancer therapeutic modality. Nat Commun 17, 1963 (2026). https://doi.org/10.1038/s41467-026-69891-2
キーワード: リボソーム標的のがん治療, 翻訳阻害, MYC駆動腫瘍, 文脈依存性小分子, トリプルネガティブ乳がん