Clear Sky Science · ja
水性バッファー中での選択的水素同位体交換によるオリゴペプチドの放射標識(重水素および三重水素)
原子レベルで薬を追跡する
現代の医薬品には、ペプチドや小さなタンパク質のような複雑な生体分子が増えています。これらの薬が体内でどこへ行き、どれくらいの期間残るかを明らかにするために、研究者は通常の原子を追跡可能な希少あるいは放射性の原子に置き換えます。本論文は、これまでの多くの方法よりも生体に近い水性溶液中で、ペプチド薬にそのような追跡可能な原子を直接「タグ付け」する手法を示しています。
なぜ小さな原子置換が重要なのか
通常の水素を重い同位体である重水素や三重水素に置き換えると、日常的な分子が強力な科学的トレーサーになります。標識された分子は元の薬とほぼ同じ挙動を示しつつ、質量や放射線を検出する高感度の装置で追跡できます。低分子薬物では、こうした標識化のための手法が豊富に揃っていますが、ペプチドやタンパク質のような大きく壊れやすい生物製剤を標識する方法は限られ、複雑で、水性環境(血液や細胞液に近い条件)に適していないことが多いのが現状です。著者らはこのギャップを埋めるため、水性バッファー中で直接、選択的に重水素や三重水素を挿入する簡便な方法を開発しました。
水中でのワンポット標識戦略
研究チームは水素同位体交換という反応に着目しました。これは分子上の水素原子が、重水素(D2)や三重水素(T2)といったガス由来の重い同位体に入れ替わる反応です。彼らはイリジウム金属を基盤とし、特定のホスフィン助触媒を組み合わせたインサイチュ触媒を構築しました。やや塩基性のバッファー中で加熱すると、この系はアミノ酸や短いペプチドの特定の炭素–水素結合を活性化し、ガスから重水素または三重水素を置換します。重要なのは、この過程が単一の工程で、水を多く含む媒体中、かつ極めて少量の金属で行える点で、壊れやすいペプチド薬や実験室での実用性に優しい条件になっていることです。 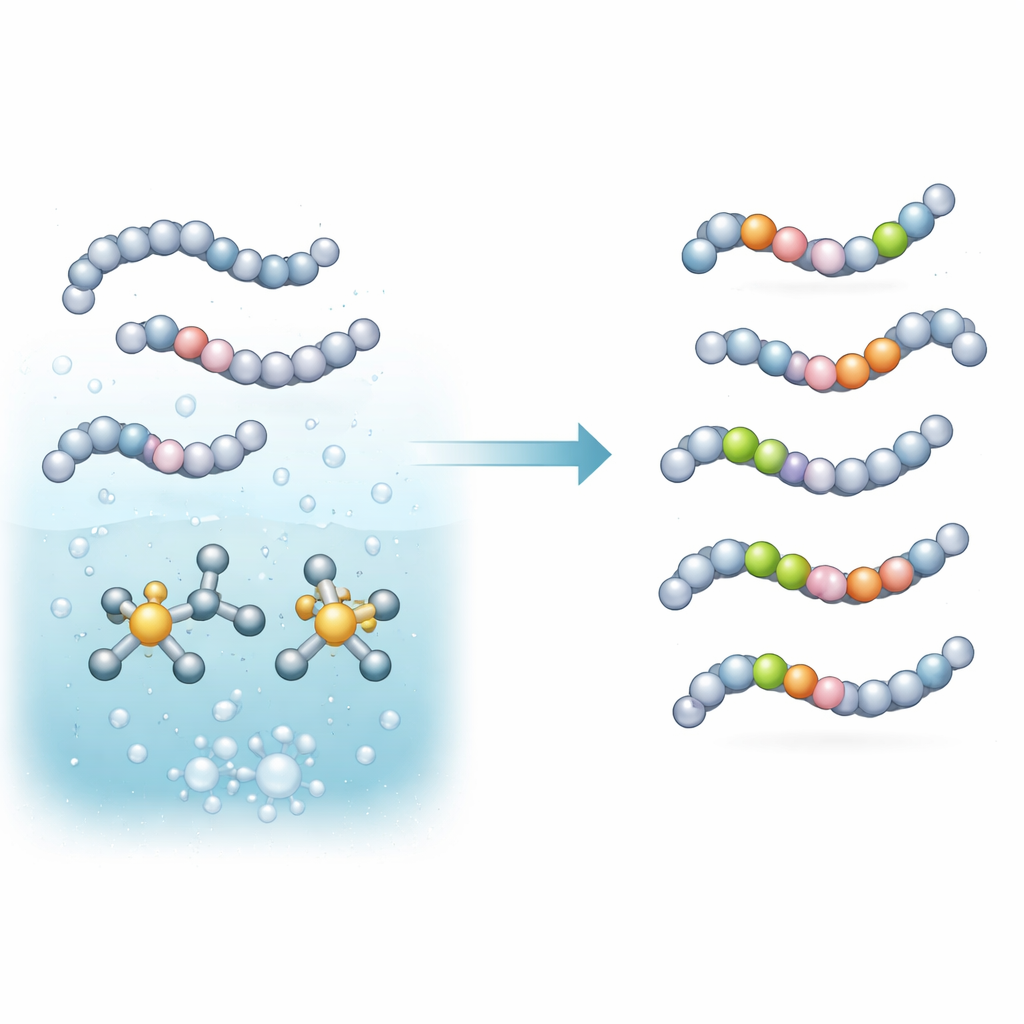
ペプチドの狙うべき部位を選ぶ
ペプチド中のすべての水素原子がラベルに適しているわけではありません。代謝過程で容易に失われる水素は放射タグが消えてしまうため不適です。著者らは触媒がどこに作用することを好むかを注意深く調べました。その結果、保護されていないリシンやアルギニンのようなアミノ酸が特に適していることが分かりました。リシンでは側鎖の炭素(いわゆるγ位)が選択的に標識され、これは「非活性化」部位と見なされ体内でより安定に残る可能性が高い場所です。アルギニンでも側鎖の近傍の位置で類似の挙動が見られました。一連の関連分子(2つのアミノ基を持つ短鎖など)を試すことで、2つの窒素部位が適切に配置されていると金属触媒が分子にクランプのように結合して標的の炭素–水素結合に到達しやすくなることがわかりました。
触媒の内部を覗く
なぜこの選択性が生じるのかを理解するため、研究者たちは実験と密度汎関数理論を用いた詳細な計算機シミュレーションを組み合わせました。これらの計算は、二量体前駆体からイリジウム錯体が形成され、水と結合し、次にアミノ酸に結合し、最終的に特定の炭素–水素結合に挿入されるまでのエネルギー地形を描き出します。モデルは、ある種の前駆体では水中でイリジウム二量体を切断することがエネルギー的に可能である一方、密接に関連する別の前駆体では不可能であり、そのため一部の開始錯体だけが有効であることを説明します。さらに、基質自身が作用中心の金属を安定化し、不活性な粒子に凝集するのを防ぐ助けとなることも示されました。最も有利な経路では、アミノ酸が二つの窒素を介して結合し、単一の炭素–水素結合を重水素や三重水素と交換するように配列する「ピンチャー状」の把持が形成されます。
単純な構成要素から現実的なペプチド医薬へ
機構を把握したうえで、研究チームは単一アミノ酸から7残基までの短いペプチド、さらに最大13残基のより複雑で治療を想定した配列へと手法を拡張しました。いずれの場合も、標識はペプチド末端のリシンまたはアルギニンの側鎖で起こり、反応条件下でもペプチドは大部分が無事であることが示されました。三重水素化では、低圧のガス条件で反応を最適化して高い比活性(分子の大部分が少なくとも1個の三重水素を持つこと)を安全に達成しました。これらの三重水素標識ペプチドはワンポットで作製され、in vitroや場合によってはin vivoのトレーサーとしてすぐに利用可能です。 
将来の医薬品にとっての意義
本研究は、現実的なペプチド薬に対して、代謝的に堅牢な位置を標的にしつつ、簡便な水性ワンステップで重水素または三重水素を選択的に導入できることを示しました。医薬品開発者にとって、これは吸収・分布・代謝の測定に不可欠な正確に標識されたペプチド製品へのアクセスを容易にすることを意味します。トレーサー製造にとどまらず、イリジウム触媒がアミノ酸とどのように相互作用するかについての機構的洞察は、複雑な生体分子の修飾位置や方法をより精密に調整する新たな手段を生む可能性があり、将来の生物由来医薬の化学的制御の扉を開くでしょう。
引用: Martinelli, E., Weck, R., Güssregen, S. et al. Radiolabeling of oligopeptides by selective hydrogen isotope exchange with deuterium and tritium in aqueous buffers. Nat Commun 17, 2317 (2026). https://doi.org/10.1038/s41467-026-69850-x
キーワード: 放射標識ペプチド, 水素同位体交換, 重水素および三重水素標識, ペプチド治療薬, イリジウム触媒