Clear Sky Science · ja
ベータ細胞由来のコレシストキニンが肥満関連の膵臓腺癌発生を促進する
余分な体重が膵臓に語りかけるとき
肥満は最も致死率の高いがんの一つである膵臓がんのリスクを高めることが知られているが、余分な体脂肪と腫瘍を結びつける生物学的な「対話」は不明瞭だった。本研究は、予想外のメッセンジャーを明らかにする:膵臓のインスリン産生細胞の内部で産生される消化ホルモン、コレシストキニン(CCK)である。代謝ストレス下でこれらの細胞がどのように変化するかをたどることで、体が対処するために用いるはずのホルモンがいかにしてがんを助長しうるかを示し、病気が定着する前に阻止する新しい方法を示唆している。
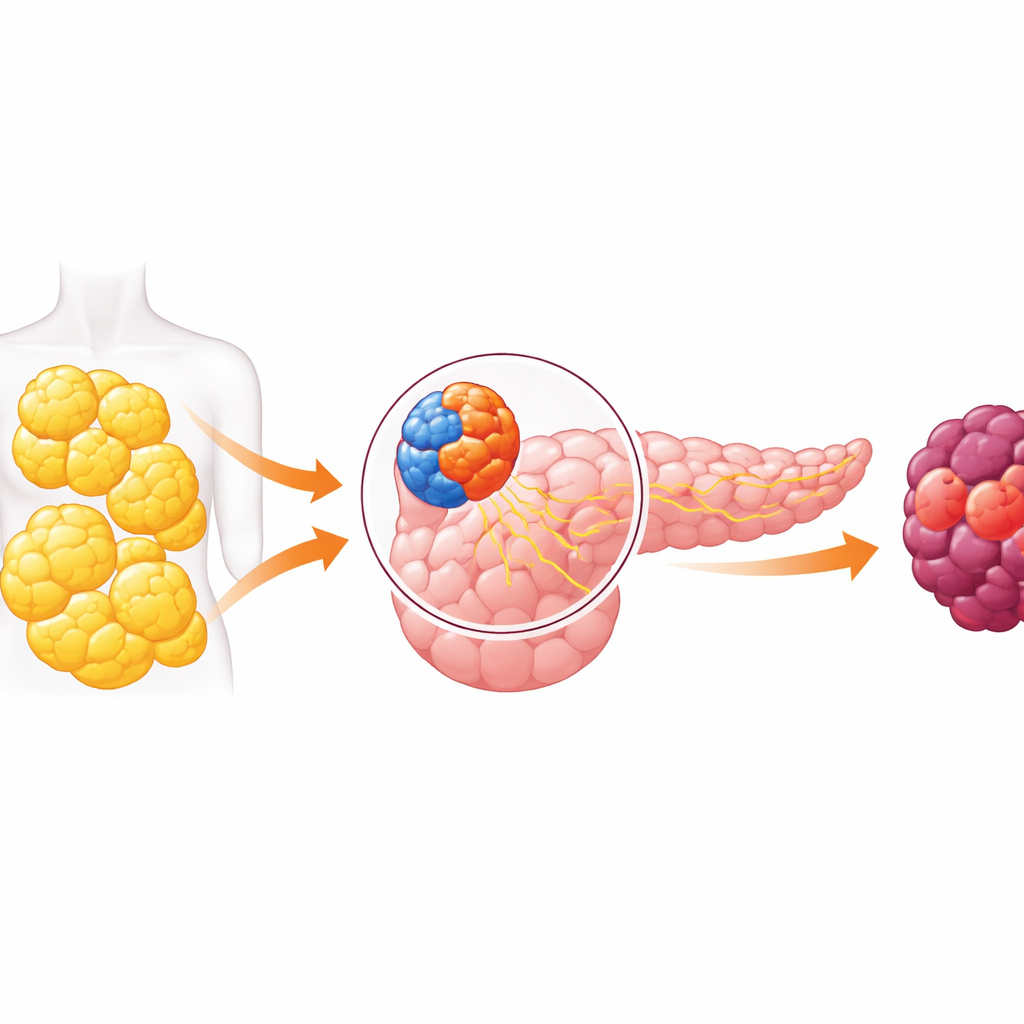
二面性を持つ器官と危険な対話
膵臓には主に二つの役割がある。一方は内分泌部で、インスリンのようなホルモンを放出して血糖を制御する小さな島状の細胞群を含む。もう一方は外分泌部で、消化液を作り、膵臓がんを最もよく生み出す細胞を含む。長年、研究者はこれらの区画がほとんど孤立して働くと考えていた。近年の研究はこの考えを覆し、ホルモン産生細胞からのシグナルが近傍の消化細胞に影響を与えうることを示した。本論文はそのクロストークを深堀りし、肥満では消化側ががんへと傾く方向に押し進められることを発見した。
ホルモン細胞のストレスが新たなシグナルを点火する
肥満下では、インスリンを産生するベータ細胞は増大するインスリン需要に応えるために常時負荷を受けている。研究者たちは単一細胞RNAシーケンシングと高度な計算手法を用いて、マウスが痩せから過体重、重度の肥満へ移行する際の個々のベータ細胞を追跡した。未熟なベータ細胞のサブセットが拡大し、徐々に専門化したインスリン産生の同一性を失っていくことが分かった。これらの細胞がストレスを受けるにつれて、タンパク質折りたたみの負荷や細胞損傷のマーカーが上昇し、インスリン産生は低下した。同時に、これらの細胞は通常は腸に関連するホルモンであるCCKを高レベルで産生し始め、CCKは消化細胞の増殖や変化を刺激しうる。
助けとなるはずのホルモンががんの燃料に
新たに産生されたCCKが単なるストレスの副産物なのか、病気の能動的な駆動因子なのかを検証するため、研究チームは肥満でなくてもベータ細胞が余剰のCCKを産生するよう遺伝子改変したマウスを作成した。これらの動物は、体重や血糖値が正常であるにもかかわらず、肥満マウスと同様の程度に膵臓の前がん病変や浸潤性腫瘍を発症した。対照的に、肥満マウスの膵臓から特異的にCCKを除去すると、動物は依然として肥満で高インスリン状態であったにもかかわらず、腫瘍負荷は著しく低下した。複数のマウスモデルにおいて、膵臓内のCCKレベルは腫瘍量と密接に一致する一方で、インスリンレベルは逆の動きを示す傾向があった。これらは、これらの系ではインスリンではなくCCKが肥満と膵臓がんを結ぶ主要ホルモンであることを示唆している。
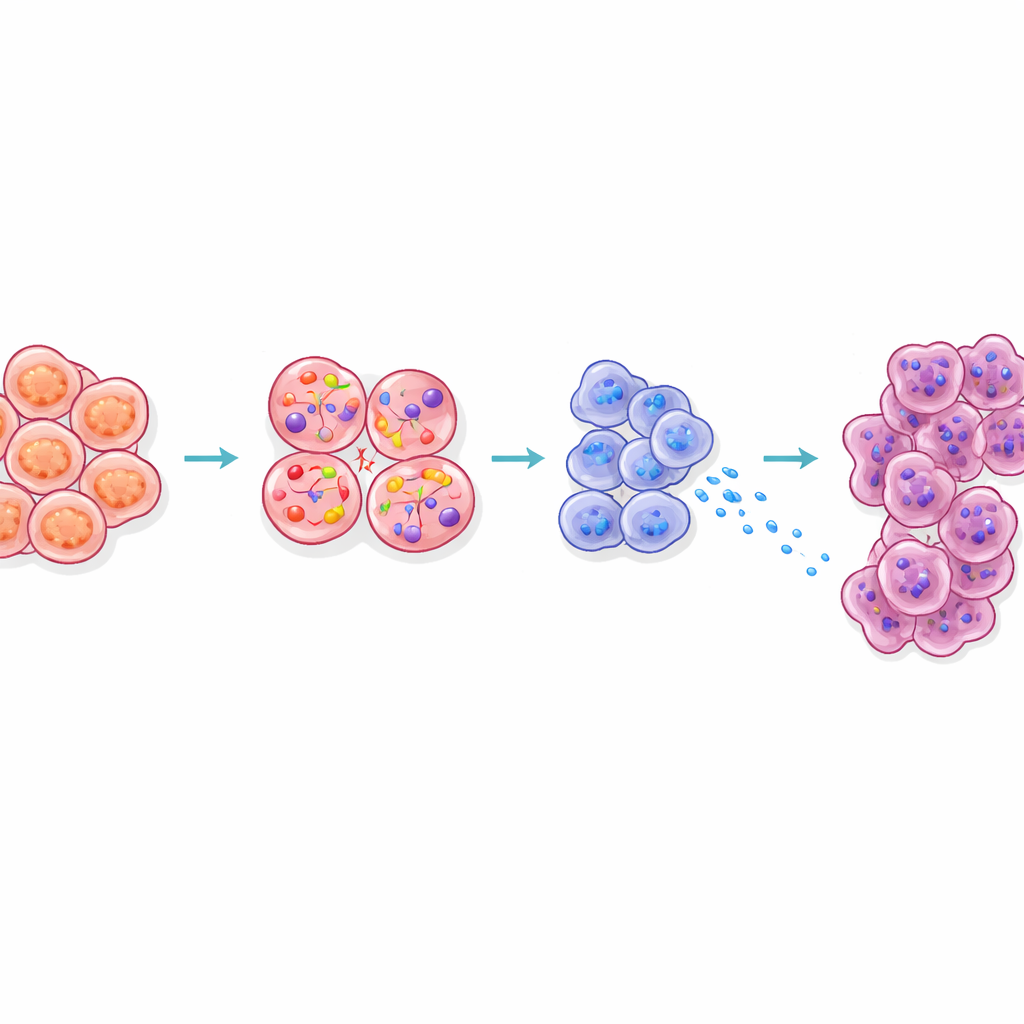
シグナルが近隣細胞に届き、準備させる仕組み
本研究はまた、ベータ細胞由来のCCKが周囲の組織をどのように再構築するかを調べた。通常消化酵素を分泌するアシナ―細胞は膵島のすぐ隣に位置する。肥満マウスでは、膵島に近いアシナ―細胞がストレスの署名を示し、消化酵素やRegと呼ばれるタンパク質を多く産生し、がんへと転換されやすい状態へと移行していた。肥満マウスでCCKシグナルを遮断するとこれらのRegシグナルは減少した。三次元イメージングはさらに、早期の前がん病変が肥満動物では膵島に異常に近い場所に発生する傾向があることを明らかにした。これらの結果は総じて、ストレスを受けたベータ細胞から拡散するCCKが膵島の周囲に“ホットゾーン”を作り、消化細胞が腫瘍化する準備をさせていることを示唆している。
ヒトの糖尿病との共通パターンと重要なスイッチ
マウスデータを2型糖尿病の有無を問わずヒトの膵組織と比較したところ、驚くべき類似点が見いだされた:糖尿病ドナー由来のベータ細胞は、肥満マウスで見られたストレスのかかった未熟な状態に対応していた。研究者らは次に、ベータ細胞で何がCCKをオンにするのかを調べるために制御解析を行い、ストレス応答性経路であるcJunを中心とした経路を同定した。肥満マウスや培養のベータ様細胞で上流のJNK–cJun経路を阻害するとCCKレベルは低下し、cJunがCCK遺伝子の調節領域近傍に結合していることが観察された。これは慢性的なストレスがJNK–cJunを活性化し、それがベータ細胞をCCK産生モードに切り替えることを示唆している。
リスクのある人々にとっての意味
一般読者にとっての核心メッセージは、肥満や糖尿病の負荷の下で膵臓のインスリン細胞は単に機能不全に陥るだけでなく、近隣の細胞ががん化するのを意図せず促すような適応を起こす、という点である。それらはCCKをスイッチオンし、このホルモンが近隣の消化細胞に対する成長およびストレスのシグナルとして働き、腫瘍形成にとって肥沃な土壌を作る手助けをする。膵臓由来のCCKは血糖制御を維持するために不可欠ではないため、この特定のホルモン源やそのストレス活性化スイッチを標的にすることで、全体のホルモンバランスを損なうことなく肥満や2型糖尿病のある人における膵臓がんリスクを理論的には低減できる可能性がある。本研究は膵臓が両側の誤ったコミュニケーションによる病気であると再定義し、早期予防の新たな道筋を浮かび上がらせている。
引用: Garcia, C.C., Venkat, A., McQuaid, D.C. et al. Beta cell-derived cholecystokinin drives obesity-associated pancreatic adenocarcinoma development. Nat Commun 17, 3292 (2026). https://doi.org/10.1038/s41467-026-69821-2
キーワード: 膵臓がん, 肥満, ベータ細胞, コレシストキニン, 2型糖尿病