Clear Sky Science · ja
心筋細胞でのIRF3活性化はPGC-1α抑制を介してミトコンドリアの酸化機能を損ない心不全を引き起こす
なぜストレスを受けた心臓と疲れた細胞が重要なのか
心不全はしばしば心臓が「摩耗する」と表現されますが、その内部では慢性的な炎症と心筋細胞内のエネルギー工場の枯渇という物語でもあります。本研究は、一見単純に見えるが含意の大きい問いを投げかけます:心筋細胞内に有害な炎症と失われたエネルギー産生を結びつける単一の分子スイッチが存在するのか、もしあるならそのスイッチを切り替えることで心不全の経過を変えられるか?その糸をたどることで著者らは重要な因子を明らかにし、心臓自身のエネルギープログラムを穏やかに高めることでマウスの心不全を部分的に救えることを示します。
病んだ人の心臓に見られる分子スイッチ
研究者たちはIRF3と呼ばれるタンパク質に着目しました。これはウイルス感染に応答することで知られる因子です。心筋梗塞後の血流低下によって生じる一般的な心不全の形態である虚血性心筋症の患者組織を調べると、これらの障害を受けた心臓ではIRF3が単に存在するだけでなく特定部位で化学的に活性化されており、遺伝子プログラムを駆動していることが示唆されました。同時に、ミトコンドリアが酸化的リン酸化によって燃料をエネルギーに変える仕組みは明らかに弱まっていました。同様のパターンは心筋梗塞モデルのマウスでも観察されます:冠動脈を結紮すると心筋細胞内のIRF3が強く活性化され、IRF3に制御された遺伝子群が発現しました。損傷したミトコンドリアから放出されるミトコンドリアDNAの断片――内部の“危険”シグナル――だけでも孤立した心細胞でIRF3をオンにするのに十分でした。
IRF3を切ると心臓は守られる
IRF3が実際に心筋細胞内で病態を悪化させるかを検証するため、研究チームはIRF3を心筋細胞に限って除去できるように遺伝子改変したマウスを作成し、免疫細胞や支持細胞はそのままにしました。心筋梗塞を誘発した後、これらのマウスは正常マウスと同じ初期損傷にもかかわらず、収縮能が良好で瘢痕化が少ないという改善を示しました。培養された心細胞では、IRF3をサイレンシングすると炎症遺伝子の発現が抑えられ、関連する他のタンパク質は妨げられませんでした。これらの結果は、心細胞内のIRF3が単なる傍観者ではなく、虚血後の炎症と構造的損傷を増幅し、心不全への移行を促進することを示しています。
IRF3が「オン」に固定されると燃料システムは崩壊する
著者らは実験を逆に行いました:心筋細胞内のIRF3を遺伝学的な“リン酸模倣”トリックで恒常的に活性化できるマウスを作成したのです。外的な誘因がなくとも、これらのマウスは急速に重度の心機能障害、血中の炎症性メッセンジャーの増加、細胞障害の兆候を示しました。心組織の詳細解析から、IRF3が慢性的に活性化している場合、PGC-1αと呼ばれる主要なエネルギー調整因子が抑制されることが分かりました。通常PGC-1αは健康なミトコンドリア、脂肪の効率的な燃焼、細胞エネルギーの均衡を促進します。PGC-1αが低下すると、複数のミトコンドリアタンパク質が減少し、電子伝達鎖が機能不全に陥り、心臓の燃料選択が変化します:カルニチンや脂質燃焼に関連する化合物が減少し、ケトン利用が損なわれ、グルコース処理も乱れます。NAD⁺/NADH比といった細胞の酸化還元バランスの指標も望ましくない方向に傾きました。
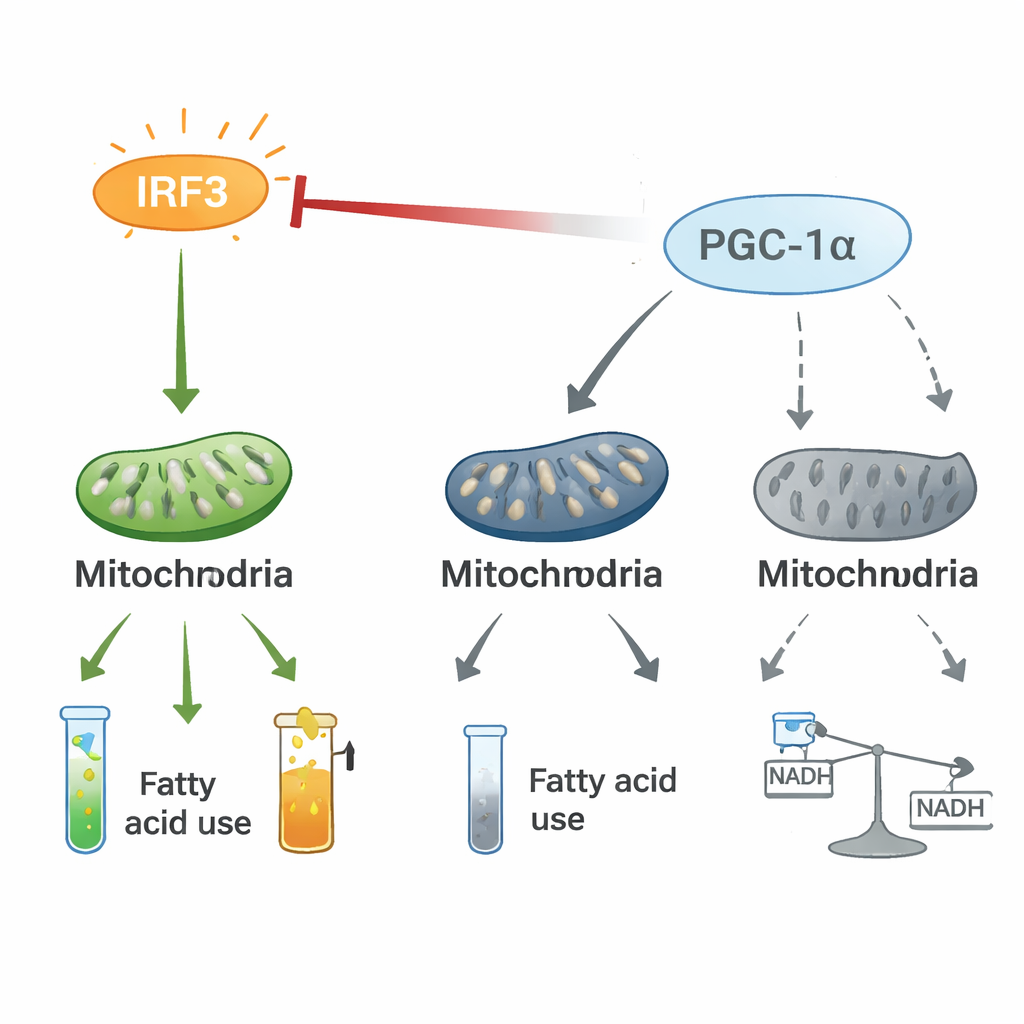
炎症とエネルギー制御の綱引き
機序を探る実験により、IRF3とPGC-1αが双方向の調節軸を形成していることが明らかになりました。心細胞では活性化されたIRF3が物理的にPGC-1αと結合し、脂肪燃焼遺伝子をオンにするPGC-1αの能力を鈍らせます。IRF3をノックダウンするとPGC-1αの量と活性が上がり、PGC-1αを増やすとIRF3駆動の炎症遺伝子が抑えられ、低酸素や細菌毒素のようなストレス下でもミトコンドリアマーカーが回復します。安定同位体トレーシングにより、IRF3活性化は通常のエネルギー産生であるクエン酸回路から炭素をひきはがしてペントースリン酸経路などの代替経路に回し、代謝物の流れを乱すことが示されました。この炎症促進スイッチ(IRF3)とエネルギーの副操縦士(PGC-1α)との綱引きは、心臓の代謝を炎症とエネルギー損失を助長する方向に再形成するようです。
心臓のバッテリーを穏やかに再充電する
最後に、PGC-1αを回復させることでIRF3の損傷に対抗できるかを検討しました。研究者らは心臓標的の遺伝子治療ベクターを用いて、IRF3が過活性な同じマウスでPGC-1αを過剰にならない程度に中程度に上げました。この穏やかな増強により、収縮能が改善し、ミトコンドリアタンパク質が増加し、脂肪燃焼やNAD代謝の遺伝子が活性化され、炎症性および線維化関連の遺伝子活性が減少しました。細胞実験では、活性化IRF3と共発現させたPGC-1αがNAD⁺/NADHバランスをより健全な状態に戻し、燃料利用を脂肪側へ戻しました。一般的に言えば、心臓の“バッテリーマネジメントシステム”を慎重に再充電することで、恒常的に“オン”になった炎症性スイッチの有害な影響を部分的に相殺できることを意味します。
将来の心不全治療への含意
本研究はIRF3を心筋細胞内での炎症とエネルギー不全をつなぐ中心的な連結点として位置づけます。心不全における炎症と代謝を別個の問題として扱うのではなく、IRF3–PGC-1α軸を介して絡み合っていることを示唆しています。これらの知見はマウスと細胞での結果に基づきますが、将来的にはIRF3活性を抑えるかPGC-1αとミトコンドリア機能を強化することで、心筋梗塞後の心不全を遅らせたり予防したりできる可能性を示しています。簡潔に言えば、過剰に働く細胞内の警報システムを鎮め、心臓のエネルギー工場を支えることが、弱った心臓をより長く力強く鼓動させるための有望な複合戦略となり得ます。
引用: Kumari, M., Evangelakos, I., Deshpande, A. et al. Activation of IRF3 in cardiomyocytes impairs mitochondrial oxidative function through PGC-1α inhibition and drives heart failure. Nat Commun 17, 2051 (2026). https://doi.org/10.1038/s41467-026-69792-4
キーワード: 心不全, 炎症, ミトコンドリア, 心筋細胞, PGC-1α