Clear Sky Science · ja
移植されたヒト神経前駆細胞における動的なトランスクリプトーム再編成がラット網膜色素変性モデルでの視力保護の機序を解明する
視力が失われるのを守ることが重要な理由
網膜色素変性は遺伝性の病気群であり、しばしば初期には夜盲から始まり、徐々に視力を奪っていきます。何百もの異なる遺伝子変異がこの病態を引き起こし得るため、それぞれに対して個別に遺伝子治療を行うのは難しいです。本研究はより普遍的なアプローチを検討します。すなわち、培養で得られた未熟な神経細胞であるヒト神経前駆細胞を眼内に移植して、残存する光受容細胞を保護するというものです。移植された細胞が実際にどのように振る舞い、どのように視力を保存するのかを解明することは、網膜色素変性だけでなく他の失明性疾患に対する将来の治療法にも影響を与える可能性があります。
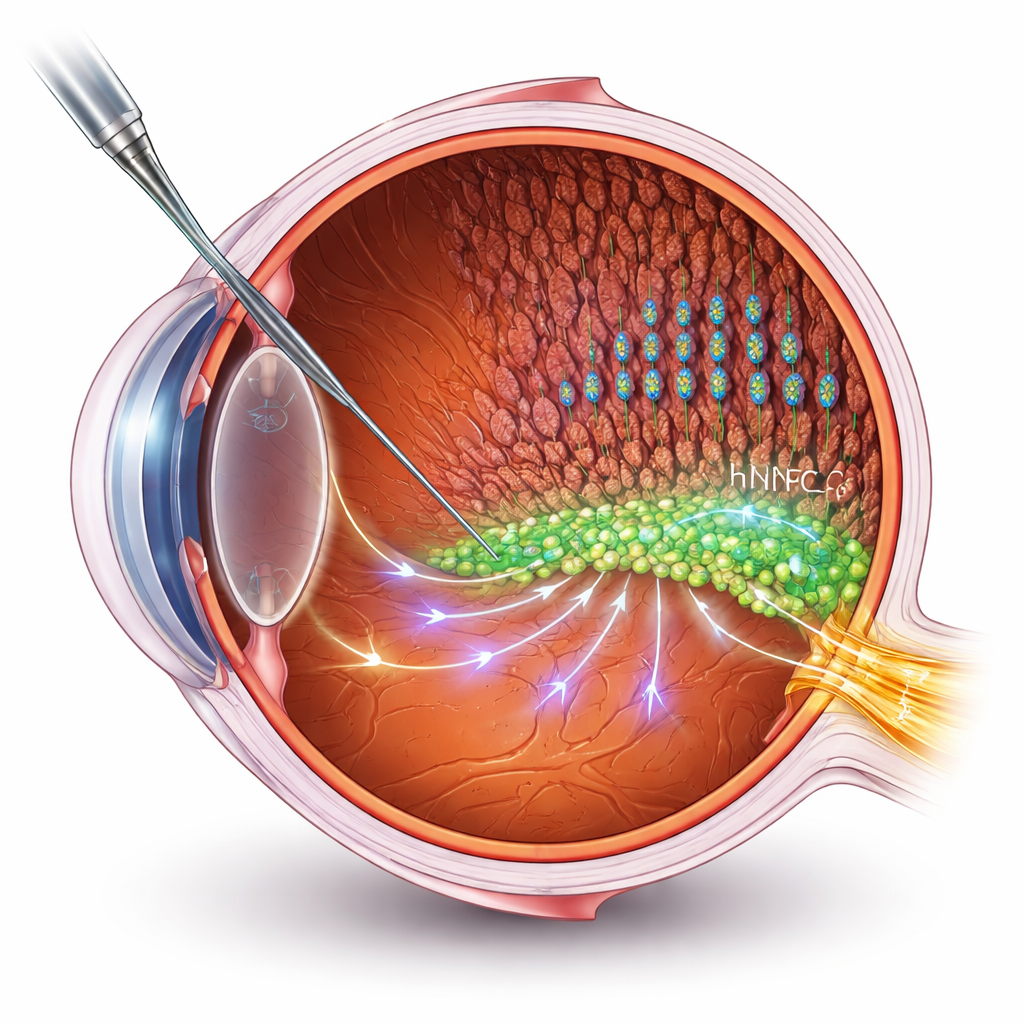
置き換えるのではなく、細胞を助ける
多くの幹細胞療法は死んだり損傷した細胞を置換することを目的とします。しかし進行した網膜疾患では脳との新しい結合を作ることが大きな技術的障壁です。本研究では別の道を取ります:ヒト神経前駆細胞(hNPC)を患者自身の網膜細胞を支える“ヘルパー”として用いるのです。研究者たちはhNPCを網膜下腔に移植し、電気生理記録や行動試験で視機能を評価しました。治療を受けたラットは未治療群に比べて視機能の維持と光受容細胞―光を捉えるロッドとコーンの層構造のより良い保持が見られましたが、変性は依然としてゆっくり進行しました。
疾患眼内で移植細胞がどのように変化するか
分子レベルでの変化を調べるため、研究チームは単一細胞RNAシーケンシングを用い、何千もの個々の細胞でどの遺伝子が発現しているかを解析しました。移植後の早期と後期に相当する2つの時点で移植されたhNPCを追跡しました。多くの移植細胞は新しい光受容細胞に分化するのではなく、むしろアストロサイト様の支持細胞へと成熟し、一部はオリゴデンドロサイトや未熟なニューロンのマーカーを示しました。時間とともにこれらの細胞は安定化し、変性が進むストレスの強い環境で生存し、隣接する網膜細胞と密接に相互作用するような性質を獲得していきました。
保護シグナル、代謝、クリアランス
hNPCはトロフィックファクターとして知られる多様な保護性タンパク質を産生しました。その中にはMANFやMYDGFが含まれ、これらは細胞生存の促進、酸化ストレスの低減、炎症の抑制と関連します。さらにミッドカインやプレオトロフィンのような神経細胞の成長や移動を支える因子も検出されました。これらの分子は移植片自身と周囲の網膜の両方に作用しているように見えました。治療群のロッドとコーンは、視覚信号伝達と細胞維持をよりよく支える遺伝子発現パターンを示し、移植細胞は細胞残骸の除去や代謝調整に関与する経路も上昇させ、光受容細胞が疾患で蓄積するエネルギー需要や毒性副産物に対処するのを助けていることを示唆しました。
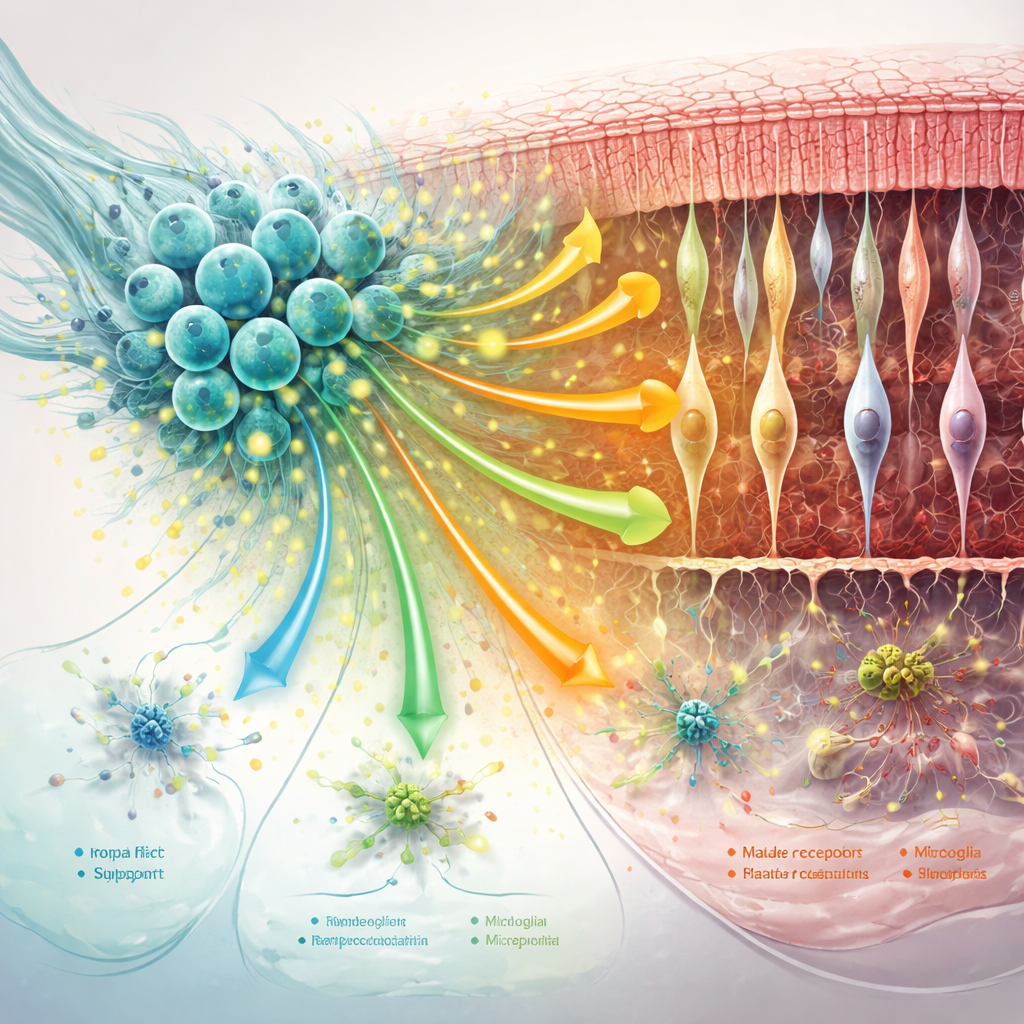
支持細胞の落ち着きと網膜の局所環境の再形成
網膜の支持ネットワーク―ミュラーグリア、ミクログリア、周囲のタンパク質マトリックス―は変性を悪化させるか遅らせるかで大きな役割を果たします。研究は、hNPC治療がミュラーグリアにおける有害な“反応性”変化の主要マーカーを抑え、特に早期の時点でミクログリアを過度に炎症性な状態からシフトさせたことを明らかにしました。同時にシナプスの安定化、細胞の接着、光受容細胞周囲の足場維持を助けるコミュニケーションシグナルが強化されました。病気が進行するにつれて、これらの利点の一部は薄れました:細胞間コミュニケーションは全体として弱まり、MANF関連シグナリングを含む特定の保護経路は低下し、支持細胞はよりストレスや免疫に偏ったプロファイルを示すようになりました。
将来の眼科治療への示唆
専門外の方への要点は、移植されたヒト神経前駆細胞が変性する網膜における“現場のファーストレスポンダー”のように機能し得るということです。これらは網膜を一から再構築するわけではありませんが、保護分子を放出し、代謝を調整し、有害な炎症を抑え、局所構造を保つのに寄与し、結果として視力低下を遅らせます。しかし、この保護効果は時間とともに薄れ、環境がより厳しくなり移植片と宿主細胞の対話が弱くなります。著者らは、MANFのような重要因子を強化し、移植片の遺伝子工学や併用療法によって宿主網膜の健康を改善することが、一時的な緩和を長期的な視力保存へとつなげるために重要である可能性があると示唆しています。
引用: Shahin, S., Bell, S., Lu, B. et al. Dynamic transcriptomic remodeling in grafted human neural progenitor cells uncovers mechanisms for vision preservation in a rat model of retinitis pigmentosa. Nat Commun 17, 2164 (2026). https://doi.org/10.1038/s41467-026-69776-4
キーワード: 網膜色素変性, 幹細胞療法, 網膜変性, 神経保護, 単一細胞RNAシーケンシング