Clear Sky Science · ja
GCN5はLXRα/SREBP1cシグナル経路を介した新規脂質合成によりMASLDの進行を促進する
この肝臓研究が重要な理由
代謝異常に関連する脂肪肝疾患(MASLD、旧称:非アルコール性脂肪性肝疾患)は、現在世界でおよそ4人に1人が影響を受けると推定されています。目立った症状がなく進行することが多いものの、線維化、肝がん、深刻な代謝合併症へと進展する可能性があります。本研究は肝臓内で有害な脂肪蓄積を促す分子的な“音量つまみ”を明らかにし、それを抑えることで肝臓を保護するとともに、既存の心血管治療戦略をより安全にする可能性を示しています。
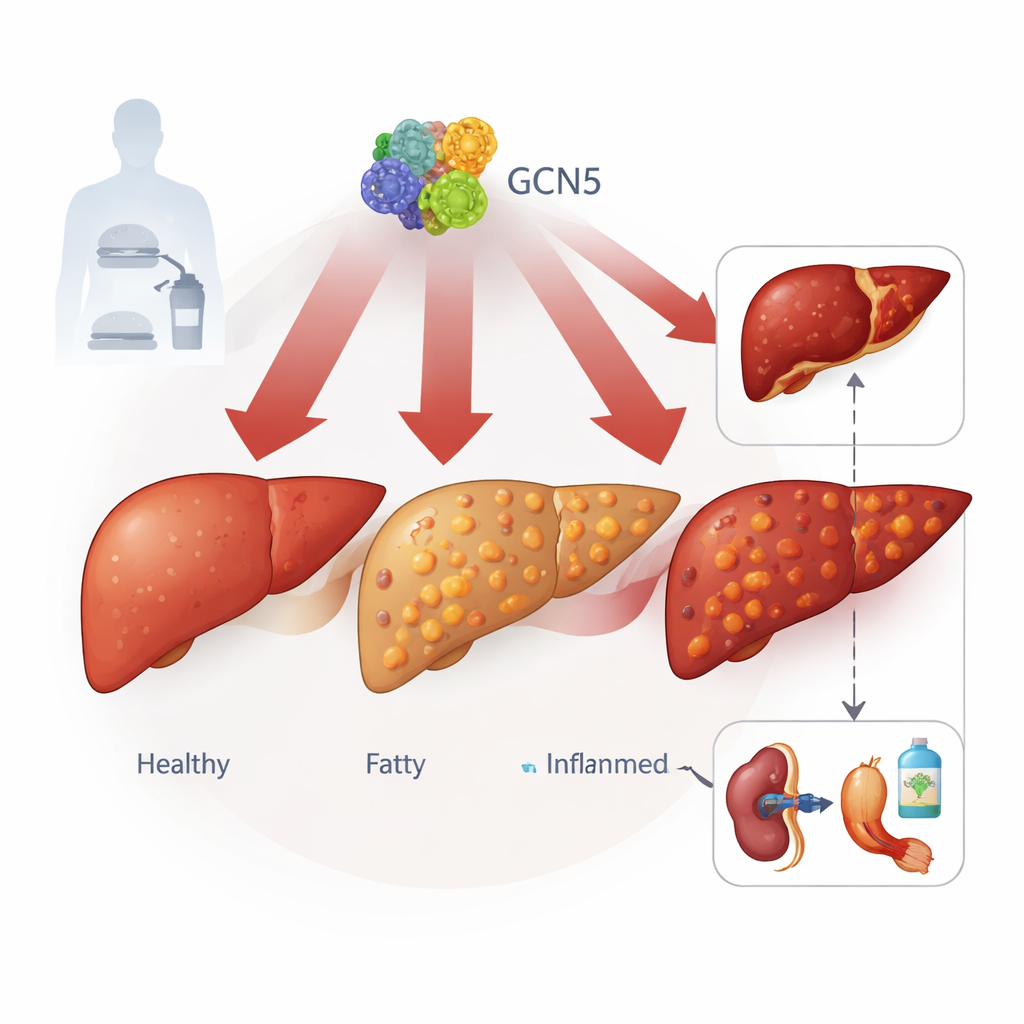
肝細胞内に潜むスイッチ
著者らはGCN5というタンパク質に注目しています。GCN5はDNAのパッケージング(クロマチン調節)を制御する因子としてよく知られています。健康から重度のMASLDまでの100人以上の肝組織と、食事誘導性の脂肪肝を示す複数のマウスモデルを解析したところ、疾患が悪化するにつれて肝細胞内のGCN5量が着実に増加していることが分かりました。これに対して密接に関連するPCAFは同様のパターンを示さず、GCN5が特別な役割を果たしていることが示唆されます。高いGCN5レベルは肝脂肪の増加、血中脂質の上昇、肝障害の強い指標と相関し、この分子スイッチが臨床的な疾患重症度と結び付くことを示しました。
動物でGCN5を上げたり下げたりする実験
因果関係を検証するため、研究チームはマウスの肝細胞に特異的にGCN5を遺伝学的に増強または欠失させました。GCN5を過剰にすると、高脂肪食を与えたマウスは摂食量や体重の増加がないにもかかわらず、肝臓がより大きく脂肪を多く蓄え、血中脂質や肝細胞障害の指標が上昇しました。培養した肝細胞でも同様の挙動が見られ、GCN5の過剰発現は脂滴の増大・増加をもたらしました。これに対して、肝細胞でのみGCN5を欠損させたマウスは強い保護効果を示しました。ヒトのMASLDやより重篤な炎症性型を模す複数の食餌モデルにおいて、これらのマウスは肝脂肪の蓄積が少なく、血中脂質や肝酵素が低く、炎症や線維化の発生も抑えられていました。
GCN5が肝臓の脂肪合成を促す仕組み
代謝に踏み込んだ解析では、研究者らは肝臓内の多くの脂肪酸とその前駆体を測定しました。GCN5の欠失は主に肝臓がゼロから合成する脂質(de novo脂質合成)を減少させ、食事由来の多価不飽和脂肪酸はほとんど変化しませんでした。遺伝子発現解析とアイソトープトレーシング実験により、GCN5は脂肪合成のマスターレギュレーターであるSREBP1cの上流に位置することが示されました。GCN5が活性化されると、脂肪酸を合成・修飾する遺伝子群がオンになり、肝臓内の脂肪合成速度が上昇しました。GCN5を除去または阻害するとこのプログラムは抑制され、糖から新たに合成される肝内脂肪への炭素流入が低下しました。
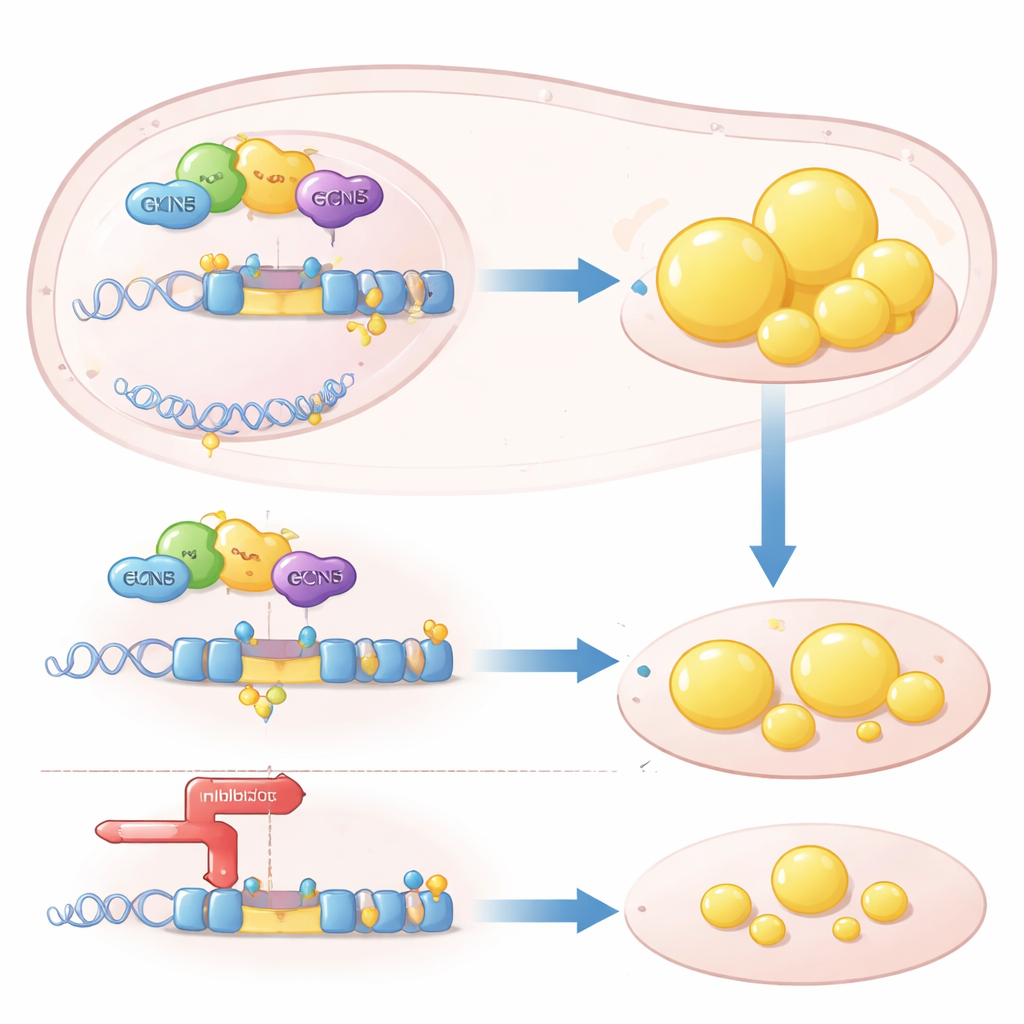
主要な脂肪遺伝子にかかるエピジェネティックなレバー
メカニズム的には、GCN5は「エピジェネティックな」レバーとして機能します:ヒストンタンパク質に化学修飾を加えて特定の遺伝子の翻訳を読みやすくします。著者らは、GCN5がコレステロール関連分子を感知する核内受容体LXRαとともにSREBP1c遺伝子の制御領域に動員されることを示しました。そこに到達すると、GCN5はヒストンH3にアセチル化マークを付加して局所的なクロマチンを緩め、SREBP1cの転写を高めます。この効果は高度に選択的で、GCN5はLXRαによるSREBP1cの活性化を増強しますが、組織からコレステロールを排出するのに重要な別のLXR標的遺伝子ABCA1には影響を与えません。GCN5がないとLXRαはSREBP1cプロモーターに効率的に働きかけられず、下流の脂肪合成プログラムは停滞しました。
創薬候補と有望な併用療法
研究チームは次に、肝臓に濃縮される小分子GCN5阻害剤CPTH2を検討しました。脂肪食で肥育したマウスモデルにおいて、CPTH2は肝臓のサイズ、脂肪含量、損傷マーカーを低下させ、副作用や摂食量の顕著な変化を伴いませんでした。ヒトおよびマウスの培養肝細胞では、CPTH2はGCN5が存在する場合にのみ脂滴や中性脂肪を低下させ、その作用が特異的であることを確認しました。重要なことに、コレステロール除去を改善して動脈硬化を抑える目的で用いられるLXR活性化化合物で処理した細胞およびマウスにおいて、CPTH2はSREBP1c駆動の望ましくない脂質合成の上昇を選択的に阻害しつつ、逆コレステロール輸送を促す遺伝子群は維持しました。高脂肪食を与えたマウスでLXRアゴニストと組み合わせると、CPTH2は有害な血中脂質と肝コレステロールをさらに低下させ、肝臓への余分な脂肪蓄積を防ぎました。
患者にとっての意味
本研究はGCN5を、食事由来やホルモン性のシグナルをSREBP1cによる脂肪生産スイッチへつなぐことでMASLDの肝脂肪蓄積を駆動する中心的因子として位置づけます。GCN5はLXRシグナルの有益なコレステロール除去経路には必須でないように見えるため、CPTH2のようなGCN5阻害薬やその改良版は、肝臓の脂肪と炎症を抑えつつ心血管保護効果を損なわずに済む可能性があります。脂肪肝と心血管疾患の両方のリスクを抱える人々にとって、このエピジェネティックなスイッチを標的にすることは、将来的にコレステロール処理の利点を犠牲にすることなく肝臓を守る方法を提供するかもしれません。
引用: Xiao, HT., Song, P., Jin, J. et al. GCN5 drives MASLD progression through LXRα/SREBP1c signaling pathway–mediated de novo lipogenesis. Nat Commun 17, 2821 (2026). https://doi.org/10.1038/s41467-026-69736-y
キーワード: 脂肪性肝疾患, エピジェネティクス, 脂質代謝, 肝代謝, 核内受容体