Clear Sky Science · ja
第14族アリルラトランを用いたα‑オキシケトンのアリル化における非配位制御
より精密に分子形状を作る
多くの医薬品や天然物は原子がちょうど正しい三次元配列になっているときだけ働きます。したがって化学者は、新しい断片を分子の一方の面からまたはもう一方の面から「押し込む」方法を学ぶのに大きな労力を費やします。本稿は、一般的な分子クラスにアリル基(短い3炭素鎖)を結合する新しい手法を説明し、これまで作るのが非常に困難だった鏡像(エナンチオマー/ジアステレオマー)構造へのアクセスを可能にします。
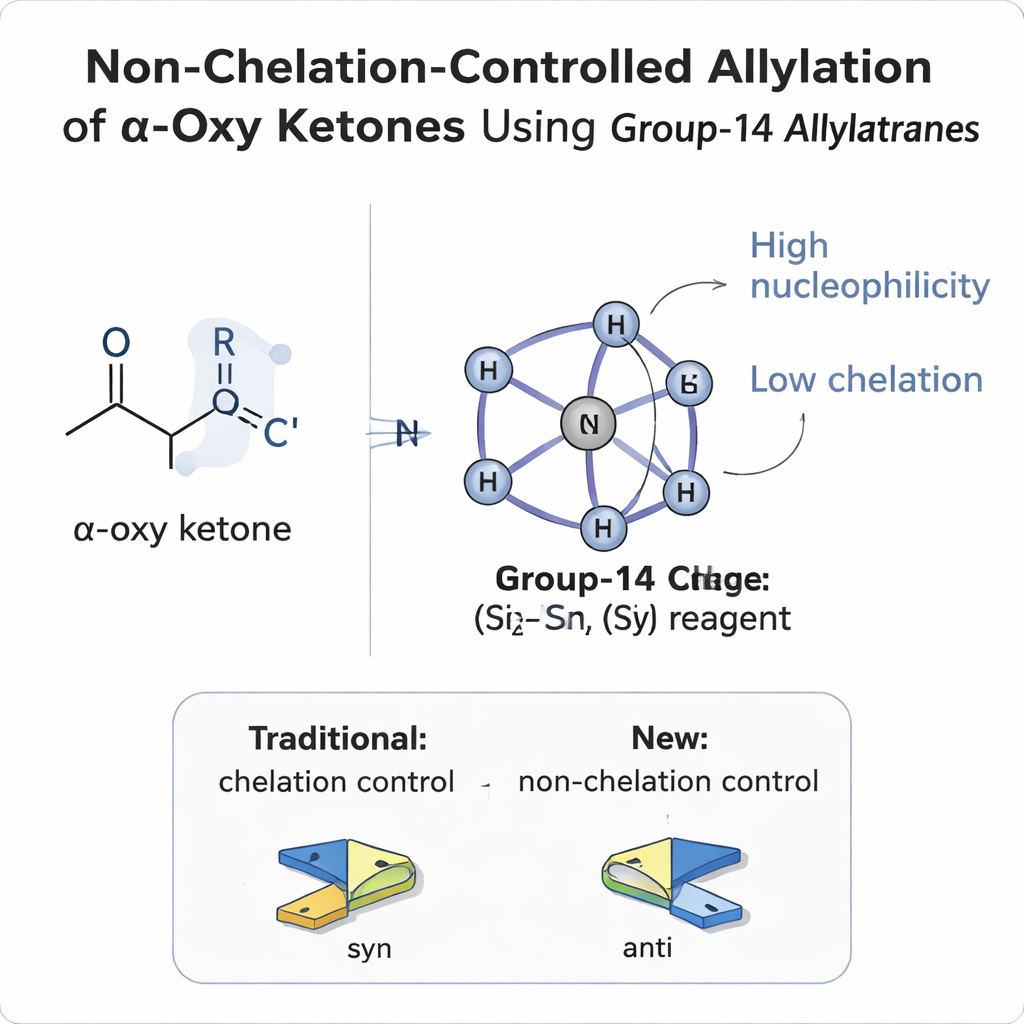
分子の側面を制御するのが難しい理由
平面状のカルボニル(炭素‑酸素二重結合)に新しい基が付くと、それは上面・下面のどちらの面からも攻撃できます。これはコインにボールが当たるようなものです。隣接する炭素(α位)に既に置換基があると、生成物として二つの三次元配置(ジアステレオマー)が生じます。数十年にわたり化学者はFelkin–Anh、極性Felkin–Anh、Cram、配位(キレート)モデルといった単純なモデルに頼ってどちらの面が好まれるかを予測してきました。α‑オキシカルボニル化合物では、隣接置換基がエーテルやエステルなど酸素含有基であるため、酸素が金属試薬をつかむ“爪”のように振る舞うことが多いです。この「配位」は分子を一つのコンフォメーションに固定し、通常は新しく生成されるアルコール基が同じ側に来るいわゆるsyn生成物をもたらします。
酸素隣接基が長年の問題である理由
配位経路は有用ですが制約も大きく、反応を強くsyn生成物へ偏らせ、反対のanti配置(二つのアルコール基が反対側を向く)を得るのを非常に難しくします。α‑オキシアルデヒド(カルボニル炭素が少なくとも一つの水素を持つ分子)では、特殊なシリコン試薬や適切に選んだルイス酸を用いた巧妙な手法によりanti生成物を得る例がいくつかあります。しかし、反応性が低く複雑な標的に多く存在するα‑オキシケトンでは課題はさらに大きくなります。より強い求核剤は一般によりルイス酸性を示し、それが化学者が避けたい配位を促進してしまいます。したがって「十分に反応性がある」ことと「酸素に対してべたつかない(配位しにくい)」ことのバランスを取るのが中心的かつ未解決の問題でした。
規則を破るかご状試薬
著者らはアリルラトランと呼ばれる新しい試薬群を導入しました。これは第14族元素(ケイ素、ゲルマニウム、スズ)を剛直なかご状骨格で保持したものです。これらの分子では、内部の窒素原子がかごを横切って中心原子に結合し、高い配位をしたほぼ被覆された金属中心を作ります。この設計は二つの重要な効果をもたらします。第一に、結合したアリル基の求核性を高め、新しい炭素−炭素結合を形成しやすくします。第二に、中心原子のルイス酸性を抑え、基質の酸素原子に強く結合する傾向を弱めます。量子化学計算と核磁気共鳴(NMR)データは電荷がアリル断片に局在し、ケイ素中心との電子的なやり取りが減少していることを示しており、試薬が強力でありながら配位を避ける理由を説明しています。
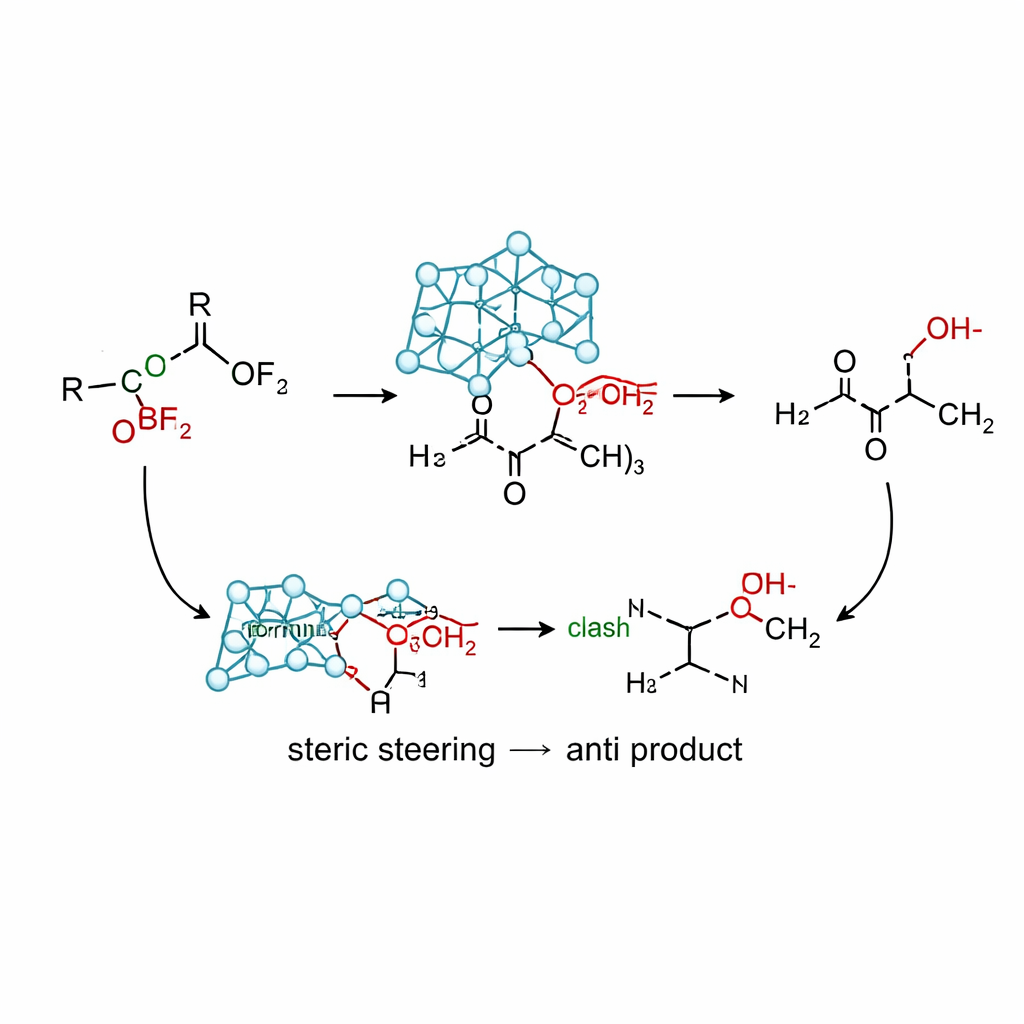
実際の反応の進行
このうちケイ素版の試薬であるアリルシラトランを、穏やかなルイス酸(トリフルオロ化ホウ素)と併用することで、幅広いα‑オキシケトンから高収率でanti‑ホモアリルアルコールを与える条件を開発しました。基準実験では、スズ、インジウム、マグネシウム、リチウム、単純なシランに基づく従来の多くのアリル供与体は、syn生成物を好むか混合物を与えるか分解することが示されました。これに対しアリルシラトランは、メトキシ、イソプロポキシ、フェノキシ、アセトキシ、シリルオキシ、アミノキシ基を有する基質や各種芳香環、環状ケトンを含む基質群で、anti/syn比を常に95:5以上で与えました。計算は、かご状のアトラン骨格がアリル基の進入方向をCramモデルに類似した配向へ導く非配位経路を示唆しています:酸素置換基はカルボニルと反対側に位置し、かごと近傍のフェニル環との立体反発がanti生成物につながる軌道を有利にします。
医薬品・天然物合成への含意
この方法は、より剛直な環状系にも適用でき、アリルシラトランのかさ高さがより障害の少ない位置からの攻撃を促します。また置換アリル基を高いanti選択性で転移する特殊誘導体にも働きます。ホモアリル断片を持つanti‑1,2‑ジオールは生物活性分子、特に酵素調節剤候補にしばしば見られるモチーフであるため、この変換は化学者にとって、従来は多段階の回り道を必要としたか実用的でなかった構造バリエーションへ信頼性の高いアクセスを提供します。重要な点として、同じ基質を配位性の高いスズ系に切り替えればsyn生成物も得られ、配位性の低いシラトラン系に切り替えればanti生成物が得られるため、分子形状を精密に制御できます。
簡潔に言うと何が変わるか
本質的には、研究者たちは「好まれない」側から標的炭素を叩く賢いアリル供与ツールを作り上げたということです。ケイ素の周囲にかごを精密に設計することで、強さ(結合形成能)と粘着性(近傍の酸素への配位しやすさ)を切り離しました。試薬は新しい結合を形成するのに十分強力でありながら、周囲の原子をつかんで望ましい立体配列を乱すほど粘着的ではありません。専門外の方にとっては、これは化学者が多くの医薬品や天然物の基盤となる三次元分子構造をより確実に彫刻できるようになり、将来の医薬品や複雑な合成分子の設計空間を広げることを意味します。
引用: Tsutsui, Y., Shiga, K., Konishi, A. et al. Non-chelation control in allylations of α-oxy ketones using group-14 allylatranes. Nat Commun 17, 2019 (2026). https://doi.org/10.1038/s41467-026-69732-2
キーワード: 立体選択的アリル化, α‑オキシケトン, アリルシラトラン, 非配位制御, ホモアリルアルコール