Clear Sky Science · ja
ペプチドプロファイリングとタンパク質同定のためのナノポアを用いた大規模並列センシング
タンパク質を一分子ずつ読み取る
タンパク質は細胞の働きを支える実働分子であり、どのタンパク質が存在するか、それらがどのように修飾され、どう相互作用するかを正確に把握することは健康や病気の理解に不可欠です。現在のタンパク質解析ツールは強力ですが、しばしば時間がかかり、コストが高く、スケールしにくいことがあります。本論文は、膜の小さな穴(ナノポア)を通過する個々のタンパク質断片の信号を捉え、人工知能でそれらを詳細なフィンガープリントに変換する新しい手法を説明します。このアプローチは、疾患マーカーの迅速で低コストな検出や、研究や診断で用いる抗体の性能確認をより簡便にする可能性があります。
タンパク質を読み取り可能な断片に変える
研究者らはもともとDNAシーケンス用に開発されたナノポア技術を基盤にしています。彼らのシステムでは、天然のタンパク質をまずペプチドと呼ばれる短い断片に切断し、各断片の両端が短いDNA断片と結合できるように穏やかに変換します。これにより「オリゴ–ペプチド–オリゴ(Oligo–Peptide–Oligo)」構造ができ、DNA向けに設計されたナノポア装置でも扱いやすくなります。チームは特定の切断酵素を用いており、多くの場合断片の末端にリシンというアミノ酸が残る傾向があるため、化学反応が予測しやすく多様なタンパク質に対応できます。結果として、数時間で多くのペプチド–DNAコンストラクトからなる精製ライブラリが得られます。
多数のナノポアで同時に「聴く」
これらのペプチド断片を感知するために、著者らは生物由来のナノポアアレイを使用します。ナノポアは膜に埋め込まれた微小なタンパク孔で、電極に接続されています。電圧をかけると、分子モーターによってDNA–ペプチド–DNA構造が一つずつ各孔へと引き込まれます。ペプチドが最も狭い部分を通過する際、イオンの流れが部分的に遮られて電流が変化します。本プラットフォームは256個の孔を並列で利用し、単一ライブラリから2時間以内に10万件を超えるイベントを収集できるため、各ペプチドがナノポアとどのように相互作用するかを捉えた大規模な一分子信号の流れを生み出します。 
雑音の多い信号から鮮明なフィンガープリントへ
表面上は、これらの電流トレースは雑音が多くばらつきがあり、同じペプチドでも異なる向きで入ることや異なる形をとることがあります。平均電流やイベントの持続時間といった従来の要約指標は、似たペプチド間で重なりが生じがちです。本研究の重要な進展は二段階の人工知能パイプラインにあります。まず、大量のトレースで畳み込みニューラルネットワーク(CNN)を訓練し、どのパターンがどのペプチドに対応するかを分類します。次に、信号がイベント中にどのように変動するかを要約する「密度行列(デンシティマトリクス)」を作成し、雑多なトレースの集合を安定した2次元フィンガープリントに変換します。詳細な時間パターンがこれらのフィンガープリントに一致する読み取りのみを保持します。このCNN+フィンガープリント戦略により、テストペプチドで約99%の精度を達成し、単一アミノ酸の差や特定の異性体、細胞内でタンパク質が受ける多くの一般的な化学修飾を確実に区別できます。
抗体の検査とタンパク質全体の同定
抗体は短いタンパク質配列を認識するため、著者らは自らのプラットフォームを使って市販抗体が実際にどの断片に結合するかをマッピングします。ホルモン前駆体から重複するペプチド断片を混合し、各抗体が結合した断片を濃縮してからナノポアで読み取ることで、好ましい結合領域を特定し、ベンダー推奨の抗体ペアが同じ部位を認識しているか、サンドイッチアッセイに適さない組合せになっているかを示せます。別のテストでは、よく使われるタグ配列とほぼ同一の4変異体を調べ、各ペプチドに対するナノポア読み取り数の相対比が抗体結合の強さをよく反映していることを示しました。最後にタンパク質同定も示しています:三つのヒトタンパク質から得たペプチドフィンガープリントでシステムを訓練し、その後未知サンプルとして全タンパク質を消化して読み取ったところ、分類されたペプチドの組合せパターンにより、曖昧や欠損があっても正しくどのタンパク質かを判定できました。 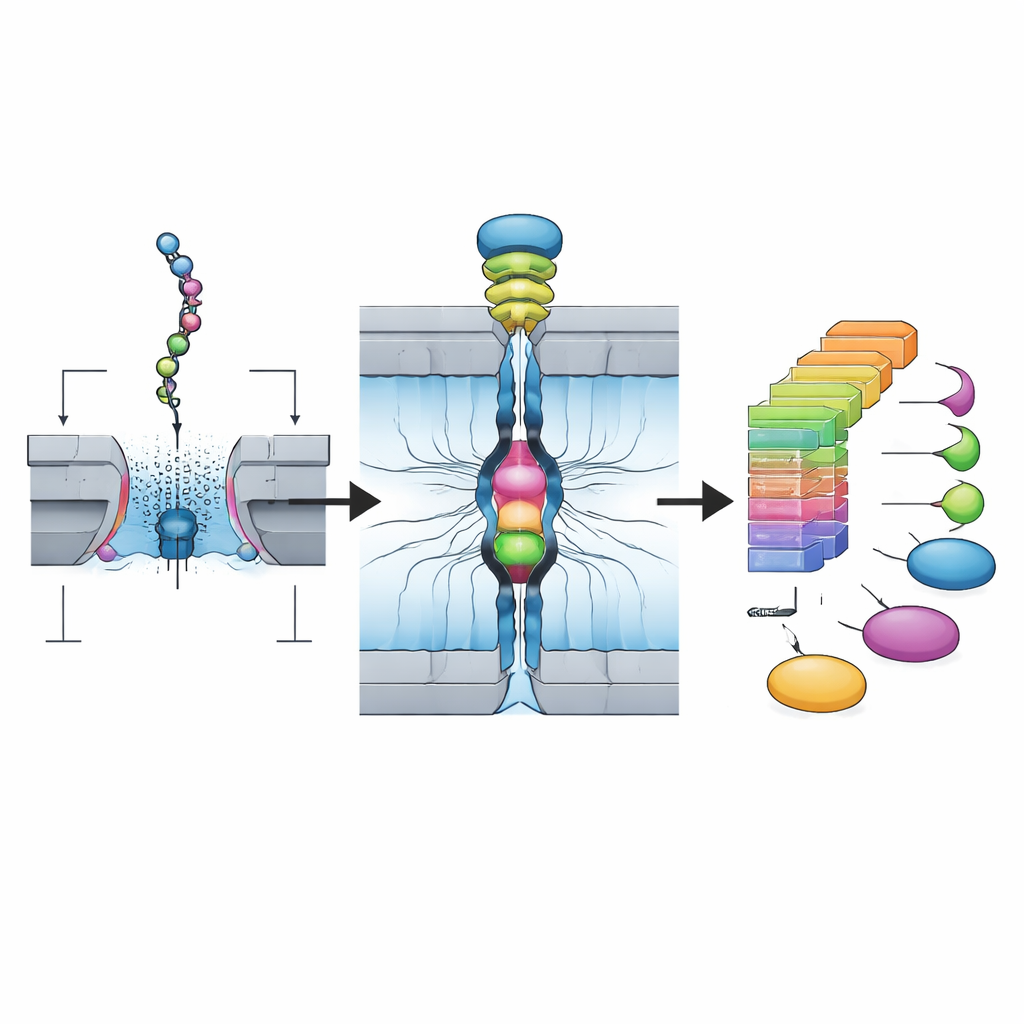
将来の検査にとっての意義
平たく言えば、この研究はDNA型ナノポアシーケンサーに巧妙な化学処理とAIを組み合わせることで、ペプチド断片に対する高並列の“聴診器”として機能させ得ることを示しています。各アミノ酸を順に読み取る必要があるのではなく、数千の一分子イベントから得られる豊富で統計的なフィンガープリントを利用して、電荷、サイズ、修飾といった微細な差異を識別します。これにより抗体品質の迅速かつ低コストな検査が可能になり、ペプチドパターンからタンパク質全体を認識する道筋が開けます。まだいくつかの制約—特定のペプチド種類の取り扱い困難さや良質な訓練データの必要性など—は残りますが、この研究は日常的な研究室や将来的には臨床診断における高スループットなタンパク質解析の実現に向けた端から端までのパイプラインを提示しています。
引用: Wang, J., Chen, J., Pan, H. et al. Nanopore-based massively parallel sensing for peptide profiling and protein identification. Nat Commun 17, 3058 (2026). https://doi.org/10.1038/s41467-026-69628-1
キーワード: ナノポアセンシング, プロテオミクス, ペプチドフィンガープリンティング, 抗体検証, タンパク質同定