Clear Sky Science · ja
薬を“ケージ”化して光で同時に一酸化窒素と麻酔薬を解放する光触媒型二重デケージングによる抗菌性鎮痛
菌と痛みを同時に攻める
細菌感染は健康を脅かすだけでなく、強い痛みを伴うことが多い。標準的な治療は通常、菌を標的にするが、患者は別途鎮痛薬に頼らざるを得ず、それらは効果が短時間で切れるか、副作用を引き起こすことがある。本研究は、光で制御できる薬剤を用いて、同時に菌を殺し痛みを和らげることを目指すもので、より賢く快適な感染治療の可能性を示している。
二役をこなす薬の発想
研究者らはアプローチの核に、皮膚や神経の局所麻酔によく使われるテトラカインを据えた。彼らは強力な抗菌・抗炎症作用を持つ小さな気体分子、一酸化窒素を化学的にテトラカインに結合させ、TTC-NOと名付けた“プロドラッグ”を作製した。TTC-NOは誘導されるまでほとんど不活性な状態にある。その後、TTC-NOは光に感受性の助剤分子とともに、血液や組織液のような水性環境を移動できる微小な高分子バブル(ミセル)に封入された。 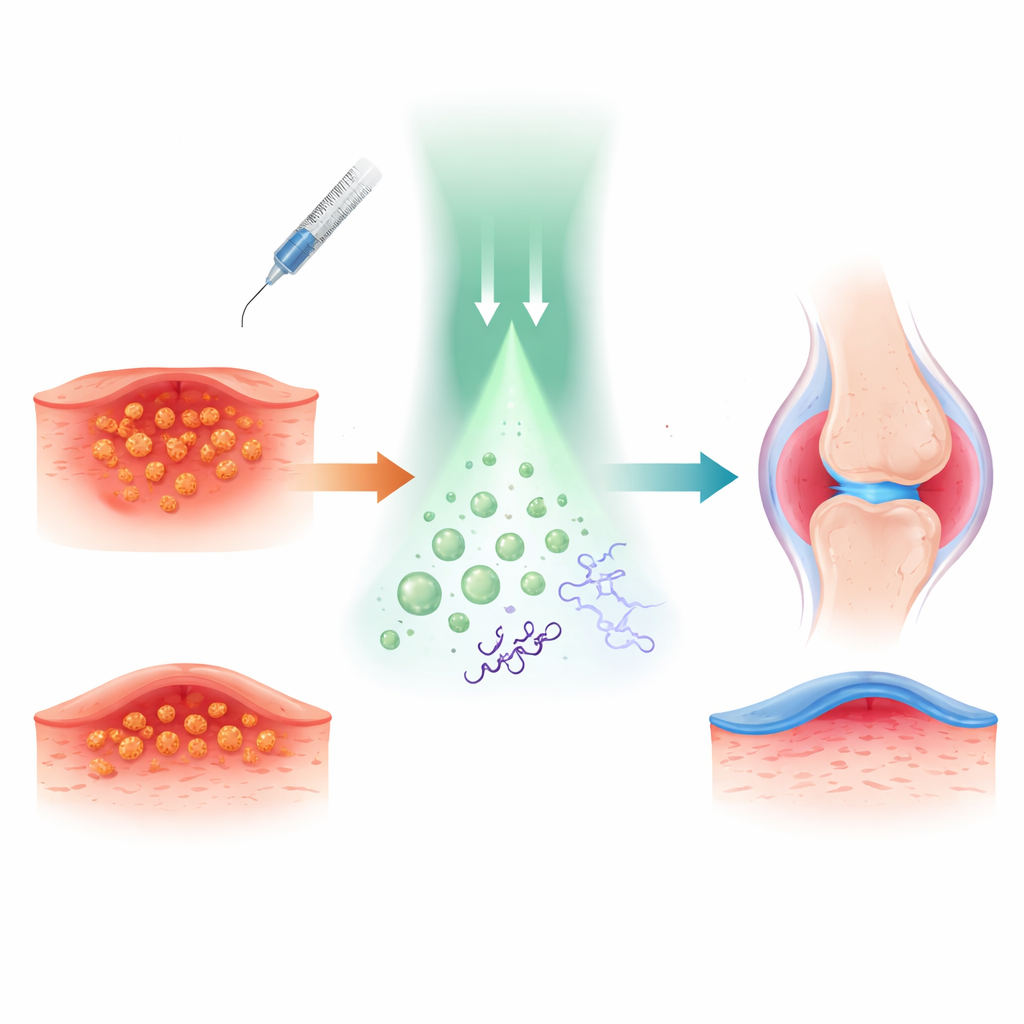
やさしい光で薬を起動する
この光スイッチの仕組みを理解するため、チームは溶液中の化学反応を調べた。緑色光で照らすとイリジウムを基盤とする光触媒がTTC-NOに電子を移すことを示し、それが特定の結合を弱めて一酸化窒素を遊離させ、テトラカインを活性形に戻すことが分かった。分光法やクロマトグラフィーによる測定で、これらの条件下でTTC-NOがほぼ完全にテトラカインと一酸化窒素に変換され、暗所ではほとんど変化しないことが確認された。二つの成分をミセルに封入した場合、粒子は直径約80ナノメートルで安定に保たれ、照射時にのみ内容物を放出した。これにより“薬をケージする薬”という概念が、体外からの光で制御可能であることが実証された。
感染創傷の治癒を促進する
次にチームは、耐性菌メチシリン耐性黄色ブドウ球菌(MRSA)で意図的に感染させたマウスの皮膚創傷モデルへ移行した。創傷の一部には抗生物質や成長因子といった標準治療が施され、他はTTC-NOミセルで処置され、光照射の有無で比較した。光を当てると、TTC-NOシステムは細菌数を急減させ、炎症を鎮め、新生血管の形成を促し、コラーゲンの沈着を促進した。これらはいずれも適切な修復に不可欠である。こうして治療された創傷は、テトラカイン単独や暗所に置いたミセルより速く、より完全に閉鎖し、その効果は第一選択の抗生物質と同等であった。重要なことに、安全性評価では主要臓器や血液化学において重大な損傷は認められなかった。
痛みの軽減と神経信号の抑制
感染と組織損傷は痛み経路を強く活性化するため、研究者らは同じ創傷モデルで痛みに関する行動を慎重に測定した。従来のテトラカインは痛み反応を引き起こす力を一時的に上げたが、数時間で効果が切れた。これに対して光で活性化したTTC-NOミセルは最大12時間にわたって鎮痛を提供した。脊髄近傍の神経群の微細構造観察や感覚皮質での活動記録は、複合治療が純粋なテトラカインの効果消失後も痛覚ニューロンの発火を長時間抑制することを示した。追加実験は、持続時間の延長が単に神経の麻痺だけでなく、一酸化窒素による細菌負荷と炎症の低下によることを示唆した。
痛みを伴う感染性関節炎の保護効果
研究者らはさらに、腫脹、骨吸収、激しい痛みを引き起こす重度の膝関節内MRSA感染である化膿性関節炎モデルでもシステムを試験した。光活性化したTTC-NOミセルは関節幅を縮小させ、細菌数を減らし、高解像度スキャンで見られる骨構造を保護した。血中の有害な炎症性分子は減少し、保護的なシグナル分子は上昇した。行動面では、処置を受けたマウスは患肢への機械的圧力に対する耐性が向上し、開放場での運動性も改善し、これもテトラカイン単独より長時間の鎮痛を示した。神経および脳の測定はこれら行動上の改善を反映しており、局所的または全身的な明らかな毒性を伴わない広範な痛み経路の抑制を示した。 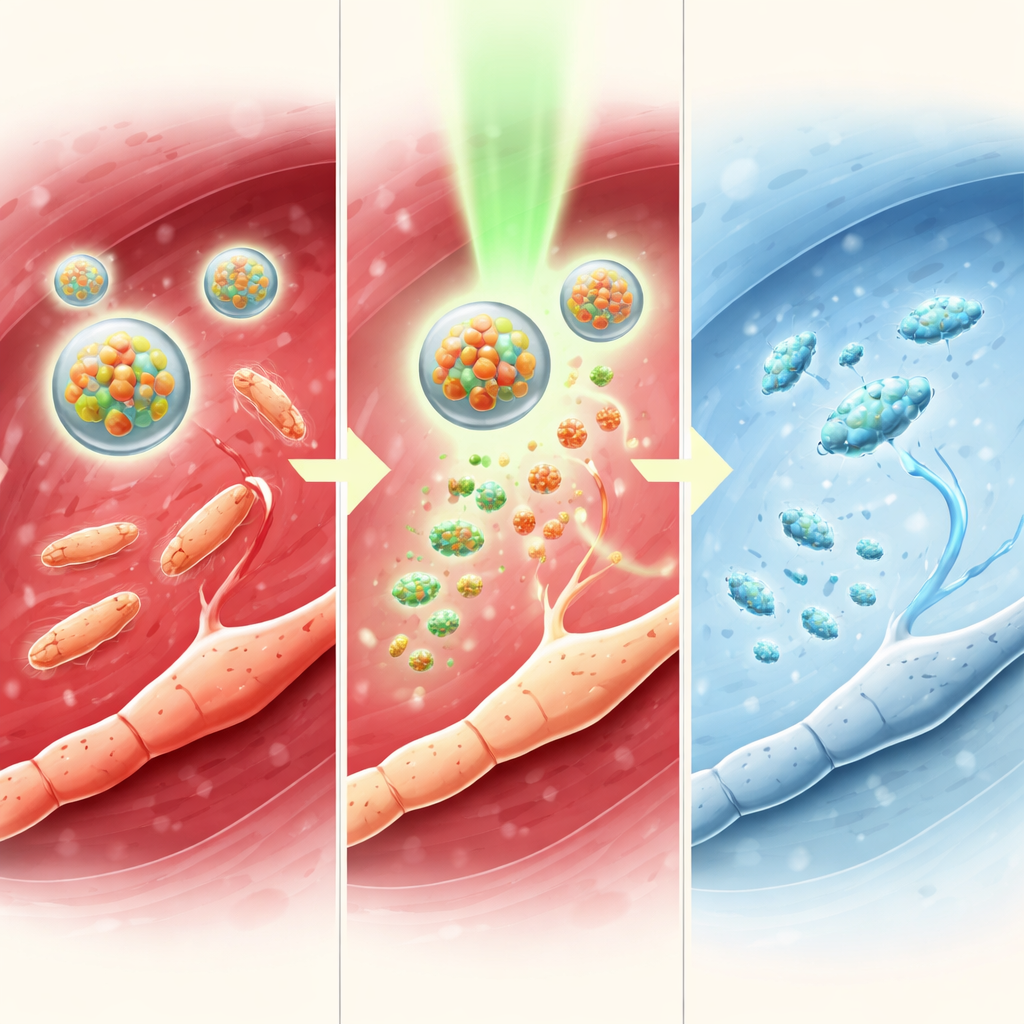
患者にとっての意味
まとめると、本研究は頑固な細菌感染を除去し関連する痛みを大幅に軽減できる、単一の光活性化ナノシステムを実証している。麻酔薬を一酸化窒素放出構造内に化学的に“ケージ”し、ミセルに包装することで、穏やかな可視光を用いて二つの有益成分をオンデマンドで局所的に放出できる。皮膚創傷や関節感染の動物モデルでは、この設計が治癒を早め、従来の局所麻酔薬を超える持続的な鎮痛をもたらした。ヒト使用に向けたさらなる試験は必要だが、切り替え可能なスマート薬剤が将来、感染治療をより効果的かつ快適なものにする可能性を示している。
引用: Zhang, J., Gan, G., Cao, C. et al. Drug-caged drugs enable photocatalytic dual decaging of nitric oxide and anesthetics for antibacterial analgesia. Nat Commun 17, 2843 (2026). https://doi.org/10.1038/s41467-026-69624-5
キーワード: 一酸化窒素療法, 光で作動する薬剤, 抗菌性鎮痛, ナノ医療, MRSA感染症