Clear Sky Science · ja
タンパク質シトルリン化ダイナミクスをプロファイリングする高スループット化学プロテオミクスワークフロー
タンパク質の構成要素が変わることの重要性
細胞はタンパク質合成後に小さな化学的修飾を加えることで、その挙動を微調整しています。その一つであるシトルリン化は、ある一般的なアミノ酸の電荷を変え、タンパク質の折りたたみ方、DNAへの結合、他分子との相互作用を変化させ得ます。こうした小さな変更は自己免疫疾患、感染、がん、脳機能と関連することが増えてきましたが、検出が非常に難しい修飾でもあります。本研究では、何千ものタンパク質にわたるシトルリン化をマッピングできる高スループットな実験ワークフローを提示し、組織や免疫細胞でいつどこに現れるかを明らかにします。
タンパク質上の隠れたスイッチ
シトルリン化はPADと呼ばれる酵素がアルギニンというアミノ酸を化学的に修飾し、その正の電荷を失わせることで起こります。一見小さな変化ですが、DNAの折りたたみをゆるめたり、構造タンパク質の剛性を変えたり、免疫系が自己組織を認識する仕方を変える可能性があります。異常なシトルリン化はリウマチ性関節炎、神経変性疾患、ウイルス感染、がんなどで報告されています。しかしシトルリン化タンパク質は稀であり、他のより一般的な修飾と混同されやすいため、標準的な質量分析法では見落とされがちです。その結果、研究者たちは身体の“シトルリノーム”――シトルリン化されたタンパク質の全体像――を断片的にしか把握できていませんでした。
二段階のタグ付け&捕捉戦略
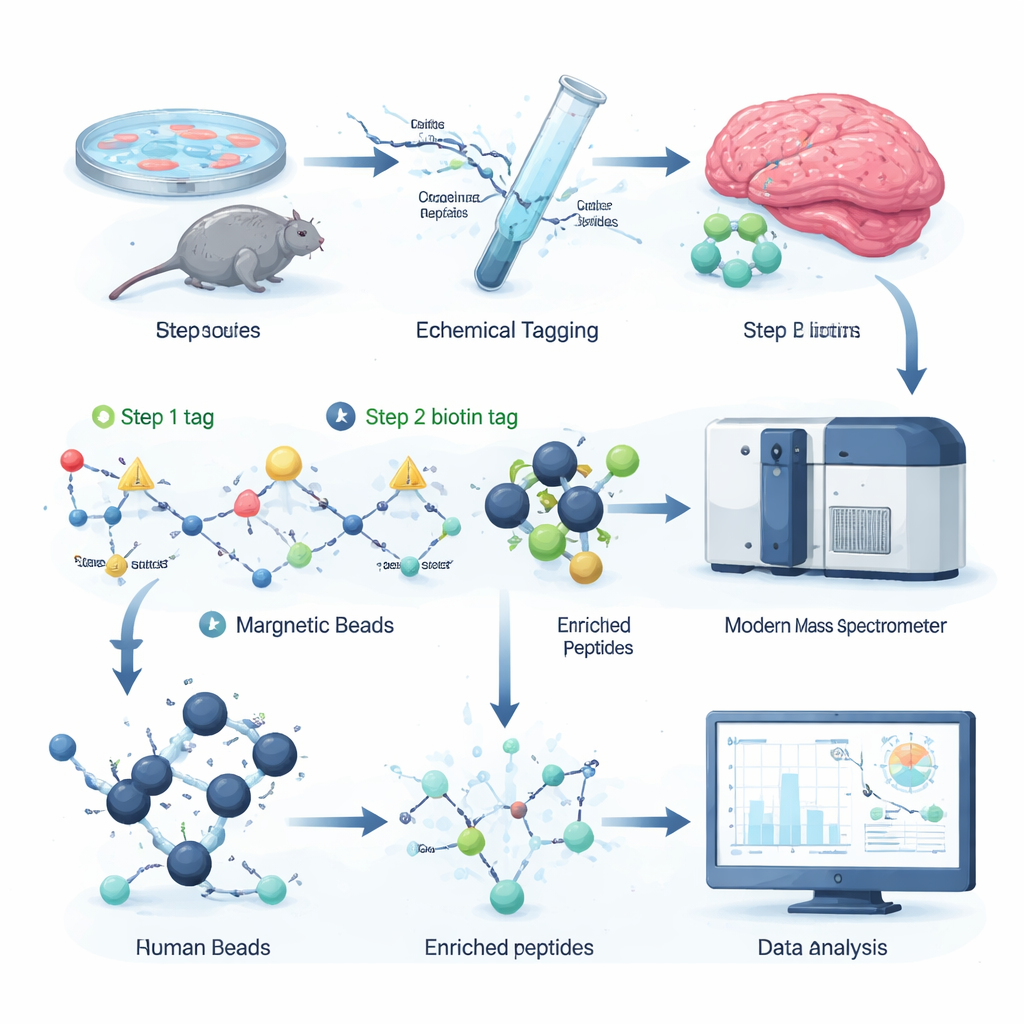
著者らはシトルリン化部位に選択的に可逆的な“取っ手”を付ける化学ラベリング戦略を考案しました。第一段階では、小さな反応性分子がシトルリンを認識して小さなタグを導入します。第二段階でより大きなビオチンタグをクリック化学で付加し、標識されたペプチドをストレプトアビジンビーズで混合物から回収できるようにします。優しい化学処理でタグのかさ高い部分を切り離すと、質量分析計で容易に検出できる小さく明確な質量移動が残ります。使用試薬は市販品でそろい、全プロトコルが96穴プレートに収まるため、このワークフローは迅速でスケーラブル、既存のプロテオミクス設備と互換性があります。
シトルリノームをより多く可視化する
既知のシトルリン化ペプチドを細胞抽出液にスパイクインし系統的に希釈する実験で、彼らの濃縮戦略はシトルリン化ペプチドのシグナルを千分の一以下の存在比でも十倍以上増強することを示しました。複雑なサンプルでは、濃縮後に検出されるシトルリン化部位の数と測定強度が劇的に増加しました。マウス脳組織に適用したところ、従来の最先端手法に比べて2~3倍多くの異なるシトルリン化部位を検出し、神経線維を絶縁するミエリン塩基性タンパク質やシナプス伝達に関わるタンパク質上の多くの部位が含まれていました。これらはシトルリン化が神経細胞のシグナル伝達や脳の配線維持に影響を与え得ることを示唆します。
粘着性のタンパク質の網を作る免疫細胞
好中球は前線の白血球で、DNAとタンパク質の粘着性の網(好中球外網:NETs)を放出して侵入者と戦うことがあります。NET形成はPAD4というシトルリン化酵素に依存しており、クロマチンを緩めてDNAが流出しやすくなります。新しいワークフローを用いて、研究者らは化学的活性化剤の用量を上げたときにヒト好中球でシトルリン化がどのように変化するかを追跡しました。580個のタンパク質にまたがり最大1,700のシトルリン化ペプチド断片を検出し、全体のタンパク質量は変わらない一方で、数百の部位が用量依存的に増減しました。ヒストン(DNAを包むタンパク質)は一部の古典的部位に限らず広範にシトルリン化され、リンカーヒストンH1のバリアントは特に修飾が目立ちました。アクチン制御因子や核膜の形を作るラミンBなどの構造タンパク質も強くシトルリン化され、NET放出時にクロマチンと細胞骨格の両方が協調して軟化することを示唆しています。
感染で見られるコアなシトルリン化署名
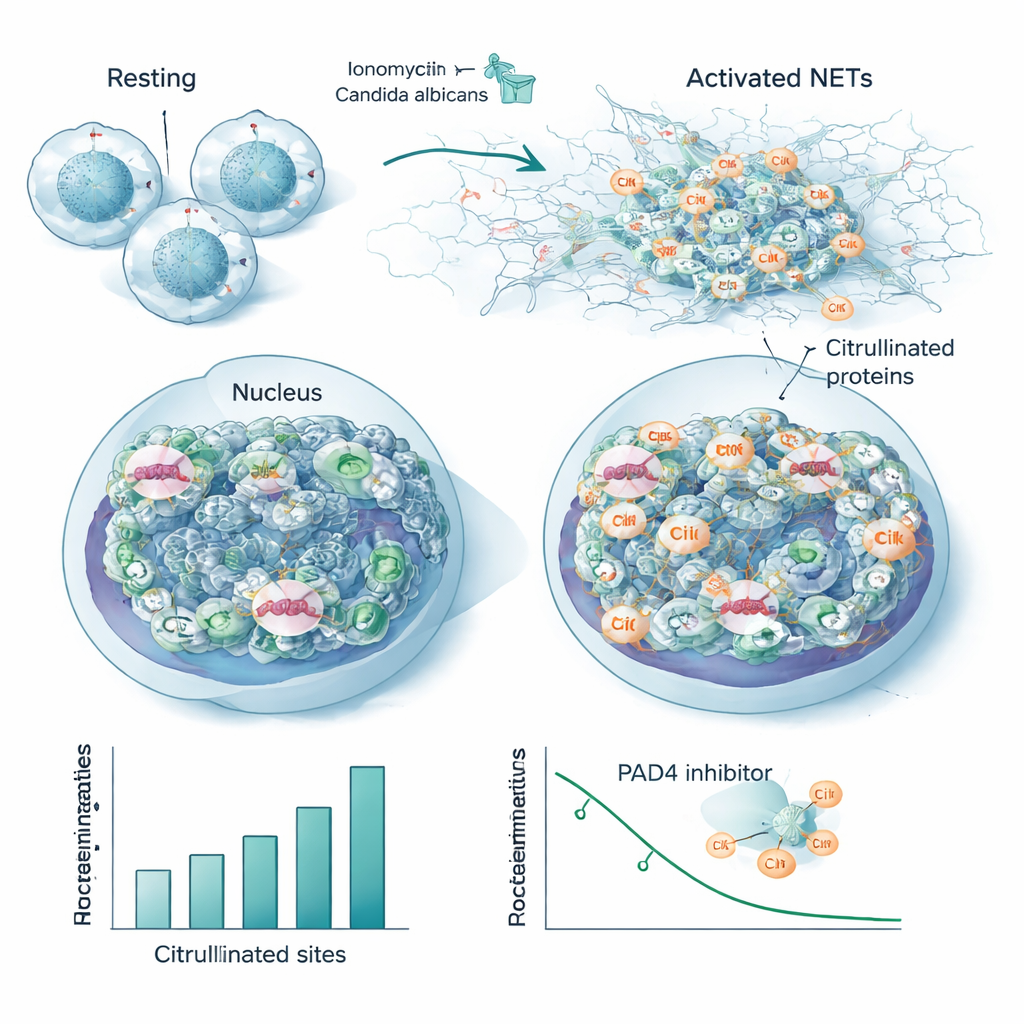
実際の感染を模すために、チームは好中球を熱殺菌したカンジダ・アルビカンスという一般的な真菌病原体で刺激しました。この刺激は強力な化学活性化剤より全体として修飾部位は少なかったものの、シトルリン化タンパク質とその位置の大部分は二つのトリガー間で重複していました。この重複がNET形成に関連する保存された“コア・シトルリノーム”を定義しており、多くの核タンパク質や細胞骨格タンパク質、自己免疫疾患で抗体の標的となる既知の自己抗原が含まれていました。研究者がPAD4を阻害する薬を添加すると、これらの多くの部位は用量依存的にシトルリン化を失い、これらが酵素の活性に直接結び付くこと、そしてPAD4阻害の感度の高い指標になり得ることを示しました。
健康と病気にとっての意味
捉えにくい修飾を測定可能なシグナルに変えることで、このワークフローは組織、免疫応答、疾患モデルにおいていつどこでシトルリン化が起こるかを描出できるようにします。専門外の読者に向けた要点は、シトルリン化はタンパク質に対する微妙な分子のディマー(明暗)スイッチのように働き、そのパターンを高解像度で見ることで自己免疫疾患の発症機構、感染による免疫細胞の再編、脳内タンパク質の変化を説明する手がかりが得られる可能性があるということです。方法がスケーラブルで標準的な実験器具に依存しているため、広く採用されやすく、新たな薬剤標的や精密診断の発見、そして小さな化学修飾が大きな生物学的影響をもたらす仕組みの深化につながる道を開きます。
引用: Meelker González, R., Laposchan, S., Riedel, E. et al. High-throughput chemical proteomics workflow for profiling protein citrullination dynamics. Nat Commun 17, 1982 (2026). https://doi.org/10.1038/s41467-026-69490-1
キーワード: シトルリン化, 自己免疫疾患, 好中球外網(NETs), 質量分析法, 翻訳後修飾