Clear Sky Science · ja
STING、TGF-β、PD-L1 の三重標的化が CXCL16–CXCR6 シグナルを強化し強力な抗腫瘍応答をもたらす
“コールド”腫瘍を“ホット”に変える
がん免疫療法は一部の患者にとって治療を変える成果をもたらしましたが、多くの腫瘍はこれら強力な薬剤に対して抵抗を示します。本研究は、なぜ一部のがんが現代の免疫チェックポイント薬に耐性を示すのかを探り、体の防御を目覚めさせ、精鋭の殺傷性 T 細胞を腫瘍内に呼び込み、そこに留めて活性を維持するという、より賢い三方向からの攻撃を提案します。
なぜ既存の免疫薬だけでは不十分か
承認されている多くの免疫療法は、PD-1/PD-L1 経路のような免疫細胞の単一のブレーキを標的にしています。より新しい薬剤群は、進行がんで免疫を強く抑制する分子である TGF-β も同時に阻害しようとするものです。YM101 は TGF-β と PD-L1 の阻害を一つの抗体に組み合わせた薬剤で、マウスで有望性を示しました。しかし、遺伝的に同一の動物でも、ある腫瘍はほとんど縮小しない場合がありました。反応性の高い腫瘍と耐性のある腫瘍を比較すると、治療成功は強い“自然免疫(innate)”の活性化、特に異常な DNA を感知して抗ウイルス様のアラーム信号を誘導する経路である STING を介したシグナルと相関していることがわかりました。
第三のレバーを加える:STING 経路
自然免疫の活性化不足が欠けている要素だと考えた研究チームは、YM101 に経口の STING アゴニスト MSA-2 を併用し、複数のマウス腫瘍モデル、特に通常は治療困難な“コールド”腫瘍で試しました。STING 活性化と TGF-β/PD-L1 阻害の三重アプローチは、腫瘍をより効果的に縮小させ、生存を延長し、再挑戦後の腫瘍再発からマウスをしばしば保護しており、長期の免疫記憶を示しました。これは STING アゴニストと PD-L1 阻害の組み合わせを上回り、TGF-β のみを阻害した場合でも STING アゴニスト療法を強化しました。つまり TGF-β は STING 駆動の免疫に対する主要なブレーキとして働いていることが示唆されます。 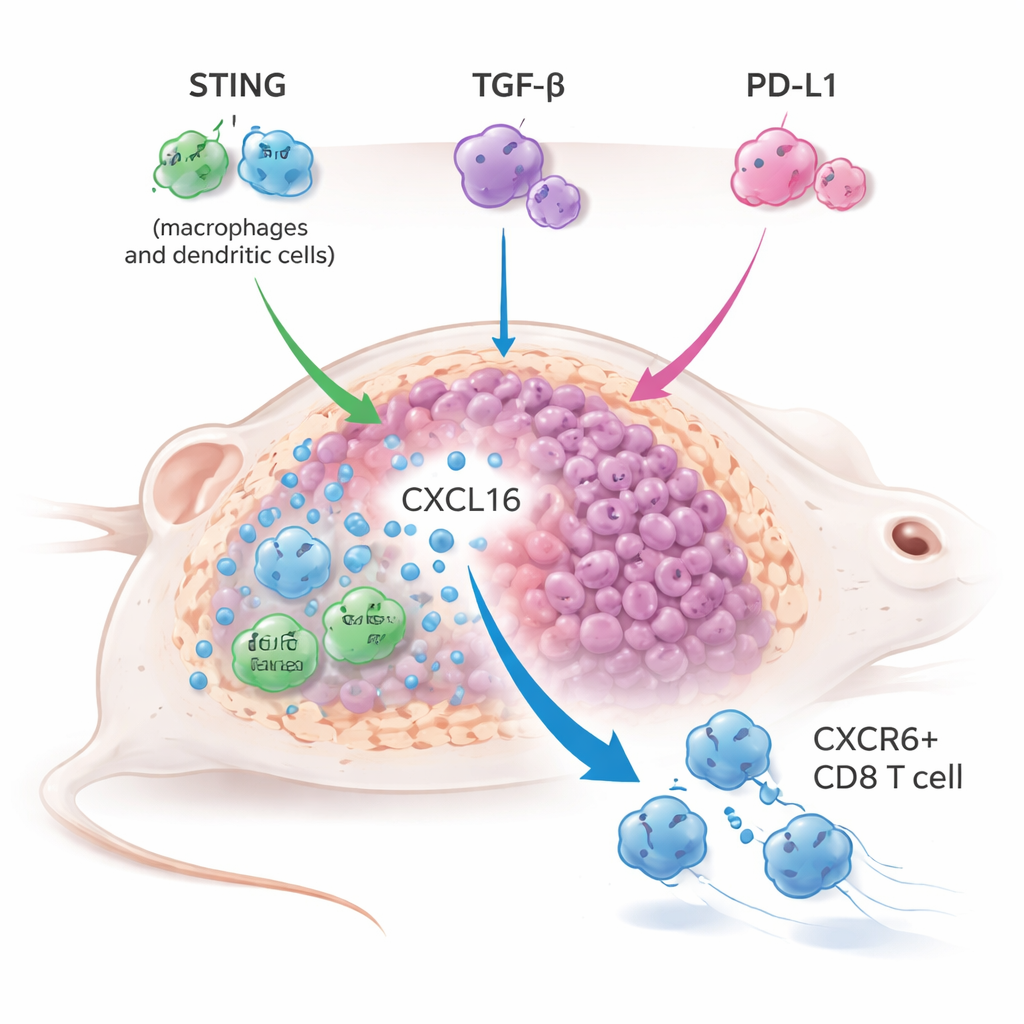
専門の殺傷部隊を呼び寄せる
この三重戦略がどのように機能するかを理解するため、研究者らは単一細胞 RNA シーケンシングと詳細な免疫プロファイリングを用いて治療された腫瘍を解析しました。その結果、受容体 CXCR6 によって特徴付けられる特定の殺傷性 T 細胞サブセットが著しく拡大していることが明らかになりました。これらの CXCR6+ CD8 T 細胞はグランザイム、パーフォリン、および炎症性分子を高発現し、強い活性化と増殖の兆候を示していました。同時に、腫瘍関連マクロファージや樹状細胞は、CXCR6 に結合してこれらの T 細胞を腫瘍内にとどめる化学走化因子 CXCL16 の産生を増加させました。CXCL16–CXCR6 結合が阻害された、あるいは T 細胞で CXCR6 が遺伝的に欠失された場合、併用治療の抗腫瘍効果は大きく失われ、この軸が治療成功の中心であることが証明されました。
シグナルカスケードはどのようにオンになるか
さらに掘り下げると、研究チームは STING 活性化と TGF-β 阻害がどのようにして CXCL16 を増強するかを問い直しました。ヒトおよびマウスの免疫細胞では、STING アゴニストは CXCL16 と抗ウイルス性サイトカイン IFN-β を強力に誘導し、TGF-β を付加するとこれらは鋭く抑えられました。研究者らは、STING が IFN‑I シグナルを誘導し、それが転写因子 STAT1 を活性化し、STAT1 が CXCL16 遺伝子の制御領域に直接結合して転写を開始することを示しました。TGF-β は HDAC4 や活性酸素種を介する可能性のある機構で STING シグナル中の重要なステップを妨げ、IRF3 の活性化および下流の IFN‑β と CXCL16 産生を鈍らせることでこの連鎖を遮断します。TGF-β を阻害するとこのブレーキが取り除かれ、STING アゴニストがミエロイド細胞内で STAT1–CXCL16 経路を完全に点火できるようになり、それによって CXCR6+ T 細胞に腫瘍内で維持・戦うためのシグナルを供給します。
ひとつの精密薬へまとめる
この複雑なレジメンをより実用的で腫瘍に集中したものにするため、研究者らは Y101S と呼ばれる単一の「免疫賦活抗体コンジュゲート」を設計しました。この分子は二重の TGF-β/PD-L1 阻害抗体に切断可能なリンカーで結ばれた STING アゴニストを結合させたものです。Y101S は腫瘍中の PD-L1 陽性ミエロイド細胞へ向かい取り込まれた後、これらの細胞内で STING 薬剤を放出します。複数のマウスがんモデルで、Y101S は高用量の遊離 STING アゴニストを併用した YM101 と同等かそれ以上の有効性を示しましたが、搭載している STING 用量はごくわずかでした。Y101S は CXCL16+ マクロファージと樹状細胞を増強し、CXCR6+ CD8 T 細胞を拡大させ、持続的な免疫記憶を誘導し、炎症シグナルを腫瘍に集中させつつ健常臓器を保護し、マウスで許容性の良好な安全性プロファイルを示しました。 
今後のがん治療に対する意味
専門外の読者に向けた要点は、がんを単一または二つの免疫スイッチだけで攻撃するのは不十分な場合がある、特に腫瘍が初期の警報システムを能動的に沈黙させているときです。本研究は、STING 活性化と TGF-β・PD-L1 の阻害を組み合わせることで腫瘍微小環境を書き換え、専門化した殺傷性 T 細胞群を強力に呼び寄せ維持し、前臨床モデルでより深く持続的な反応を達成できることを示しています。三重標的化した抗体薬物複合体 Y101S はこの戦略を単一の標的医薬品として体現しており、標準的なチェックポイント薬に現在抵抗する腫瘍を標的とする次世代免疫療法への道筋を示します。
引用: Yi, M., Li, T., Gu, Y. et al. Triple targeting of STING, TGF-β, and PD-L1 boosts CXCL16–CXCR6 signaling for potent antitumor response. Nat Commun 17, 1441 (2026). https://doi.org/10.1038/s41467-026-69456-3
キーワード: がん免疫療法, STING 経路, TGF-β 阻害, PD-L1 抗体, CXCL16 CXCR6 T 細胞