Clear Sky Science · ja
共存するクロマチン特徴上のDNAメチル化およびヒドロキシメチル化のシーケンシング
細胞が書き残す化学的メモを読む
体のすべての細胞は同じDNAを持ちながら、脳細胞、皮膚細胞、幹細胞は非常に異なる振る舞いをします。その一因は、DNAやそれを包むタンパク質に化学的な「メモ」が書き込まれ、遺伝子のオン・オフを助けることです。これまで、複数のメモが同じDNA断片上で同時に存在するかを読み取ることは困難であり、これらが連携して働く仕組みの理解に欠けがありました。本研究は、遺伝情報と主要な化学的マーキングを同時に読み取る新しい方法を示し、これらがどのように組み合わさってエンハンサーと呼ばれる重要なDNAスイッチを制御するかを明らかにします。
なぜDNAに鉛筆の跡が必要なのか
DNAは単独で働くわけではありません。ヒストンと呼ばれるタンパク質に巻き付いてクロマチンを形成し、DNAとヒストンの両方が小さな化学基で飾られます。DNA上の重要なマークの2つは、塩基C(シトシン)に付加されるメチル基とヒドロキシメチル基です。これらはDNAの巻き締まり方や近傍の遺伝子の活性に影響を与えます。大まかに言えば、メチル化は遺伝子のサイレンシング(不活化)と関連することが多く、ヒドロキシメチル化は遺伝子が活性な領域に現れる傾向があります。しかし、これらのマークの影響は局所的な状況、つまりゲノム上の正確な位置や隣接するヒストンマークによって左右されます。
別々の地図の問題点
既存のシーケンシング法は、ゲノム全体にわたるメチル化およびヒドロキシメチル化のマップを作成できますし、他の手法は活性または沈黙領域を示すヒストンマークをマップできます。しかし、これらは通常別々の実験で行われ、コンピュータ上で比較されます。それによりどの特徴が同じ近辺にあるかはわかりますが、単一の細胞内で同じDNA断片上に本当に共存しているかは分かりません。過去の統合的手法はDNAを損傷させるような過酷な化学処理を必要とし、重要な点として同一リード上でメチル化とヒドロキシメチル化を確実に区別できませんでした。その結果、マークの組み合わせがどのように協調するかの分子レベルの明確な図像が欠けていました。
多層読み取りの新手法
著者らは6-base-CUT&Tagと呼ばれる方法を開発し、DNAの4つの塩基に加えてシトシンの3つの化学状態—未修飾、メチル化、ヒドロキシメチル化—を、特定のクロマチン特徴に物理的に付随するDNA断片上で読み取れるようにしました。まず、分子フックのような抗体を使って、例えば活性クロマチンの標識を持つヒストンに巻きついたDNAを引き出します。次に、設計された酵素が特別なアダプターを差し込み、捕獲した各DNA断片を掃除工程で散逸する断片に対しても残存する小さなループに変えます。精練された化学および酵素処理が続き、各シトシンの状態を異なるシーケンス信号に変換し、最新のシーケンサーが読み取れるようにします。こうして単一のリードから、その断片がどこから来たか、どのヒストンマークを持っていたか、そしてその上のどのシトシンがメチル化またはヒドロキシメチル化されていたかが報告されます。
遺伝子スイッチを細部まで拡大して見る
マウス胚性幹細胞をテストケースとして、研究チームは6-base-CUT&Tagを用いて複数の重要なヒストンマークを調べ、異なる種類の調節DNAを区別しました。彼らはエンハンサー—遺伝子のオン・オフを制御するスイッチとして働くDNA領域—に着目しました。エンハンサーは特定のヒストンマークによって「活性」「プライム(準備)」「ポイズド(待機)」の状態に分類されます。研究者らは、H3K4me1と呼ばれるヒストンタグのみで標識されたエンハンサー(しばしば“プライム”と考えられる)が、特にH3K4me1に結合したヌクレオソーム上で直接検査した場合に、DNA上のメチル化およびヒドロキシメチル化の両方が最も高レベルで存在することを見出しました。対照的に、強い活性や抑制の追加のサインを持つエンハンサーでは、これらのDNAマークが少ないか、メチル化からヒドロキシメチル化への傾きが見られ、メチルマークの消去が進行していることを示唆しました。
より細かな情報でエンハンサー状態を解読する
すべてのエンハンサー型がH3K4me1マークを共有することから、チームはH3K4me1で標識されたDNA上のDNAマークの詳細なパターンだけで異なるエンハンサー状態を区別できるかを問いました。彼らは6-base-CUT&Tagデータを用いて機械学習モデルを訓練し、単一のヒストン特徴上でどれだけのメチル化とヒドロキシメチル化を有しているかに基づいてエンハンサーを活性、プライム、ポイズドに分類しました。このモデルは、特定のヒストンマークに限定されない標準的な全ゲノムデータで訓練した同等のモデルよりも高い性能を示しました。言い換えれば、マークが実際に発生する局所文脈でDNAマークを読むことは、細胞内のすべてのDNAを平均化して読むよりも鮮明な図を与えます。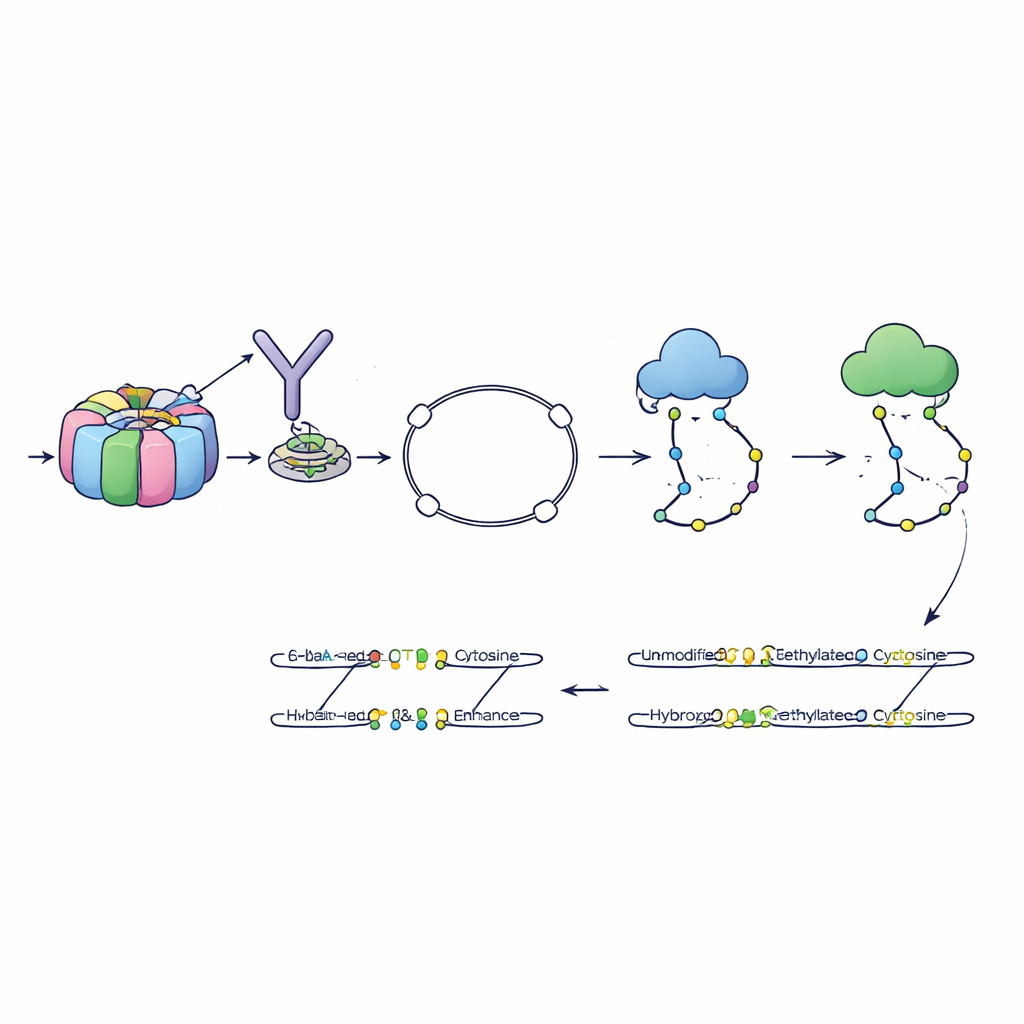
細胞の同一性理解への含意
専門外の読者にとっての要点は、この方法により遺伝配列、DNAマーク、ヒストンマークという複数の情報層を同一の分子上で読むことが可能になることです。この詳細な視点は、特定の化学タグの組み合わせが幹細胞における遺伝子スイッチの準備状態をどのように定義するかを明らかにします。6-base-CUT&Tagは従来法より効率的で損傷が少ないため、これまで隠れていた微妙なパターンを明らかにできます。長期的には、このクロマチンの多層読み取りが、細胞がどのように自らの同一性を記憶するか、発生や疾患の過程でどのように変化するか、そして規制コードをより正確に標的化する治療法の発展を助ける可能性があります。
引用: Araujo Tavares, R.d.C., Dhir, S., He, X. et al. Sequencing DNA methylation and hydroxymethylation at co-occurring chromatin features. Nat Commun 17, 2591 (2026). https://doi.org/10.1038/s41467-026-69429-6
キーワード: エピジェネティクス, DNAメチル化, クロマチン, エンハンサー, 幹細胞