Clear Sky Science · ja
ヒトホスホリボシルホルミルグリシナミジンアミド合成酵素のアロステリック制御と触媒結合の構造的・分子基盤
なぜこの酵素が健康に重要なのか
体内のすべての細胞は、反応を駆動し、エネルギーを貯蔵し、遺伝情報を担うプリンという小さな分子に依存しています。急速に分裂するがん細胞は特にプリンを大量に必要とし、それらの合成経路を再配線することが多い。本研究は、スクラッチからプリンを構築する上で重要な役割を果たすヒト酵素FGAMS(ホスホリボシルホルミルグリシナミジンアミド合成酵素)に焦点を当てています。FGAMSの三次元構造とその部位間の動きや通信の仕組みを明らかにすることで、酵素のオン・オフの切り替え方や腫瘍増殖を遅らせるための標的化の可能性が明らかになりました。
生命の構成要素を制御する仕組み
細胞は、エネルギーを消費し複数の酵素を使って複雑な環状構造を組み立てるデノボ経路と呼ばれる骨の折れる組立ラインでプリンを合成します。FGAMSはこの連続の第4段階を担い、基質を効率よく流すのを助ける「ピュリノソーム」と呼ばれる大きな酵素クラスターの中心に位置します。増殖の早いがん細胞はしばしばこの経路を強化するため、FGAMSのような酵素は魅力的な薬剤標的です:それらを阻害すると腫瘍が必要とするヌクレオチドを枯渇させる一方で、健康な細胞はリサイクル経路に頼ることができます。
形を変える分子機械
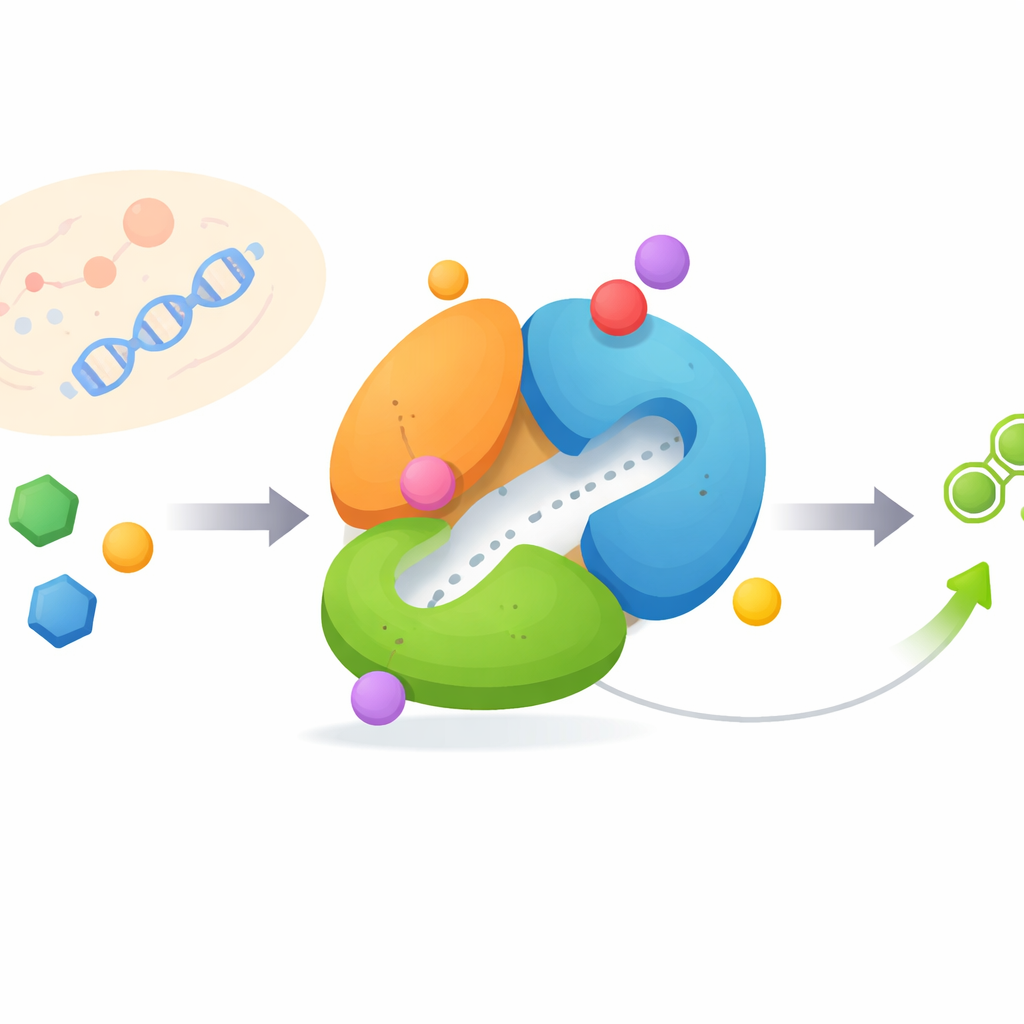
FGAMSはそれぞれ異なる役割を果たす三つの連結ドメインから構成され、順序立てて協調して働かなければなりません。あるドメインはグルタミンからアンモニアを切断し、別のドメインはそのアンモニアを用いて小さな糖由来分子を修飾し、三つ目のドメインは調節ハブとして機能します。高分解能のクライオ電子顕微鏡を用いて、研究者たちはエネルギー担体分子が結合した状態、短寿命の反応中間体が閉じ込められた状態、複数の基質や中間体が同時に存在する状態の三つの異なる作業状態でFGAMSを捉えました。これらの状態を比較すると、可塑的なループとN末端の“アーム”が劇的に動き、化学反応の進行に合わせて酵素の再構成が起きることが明らかになりました。
隠れたトンネルと分子ゲート
一つのドメインで放出されたアンモニアが、拡散して失われたり有害反応を引き起こしたりすることなく離れた利用部位へ安全に移動する仕組みは大きな謎でした。新しい構造は二つの部位を結ぶこれまで見えなかった内部トンネルと、特定のアミノ酸によって形成される一連の“ゲート”を明らかにします。適切な基質が結合して中間体が形成されると、中心ループが秩序立った位置にスナップし、N末端ドメインを引っ張り、触媒ドメイン近傍のループを再配置します。この協調運動により、グルタミンが処理されるための二つの入口ゲートが開き、高エネルギーの中間体を安定化する領域が一時的に再形成されます。
運動を介した化学反応の結合
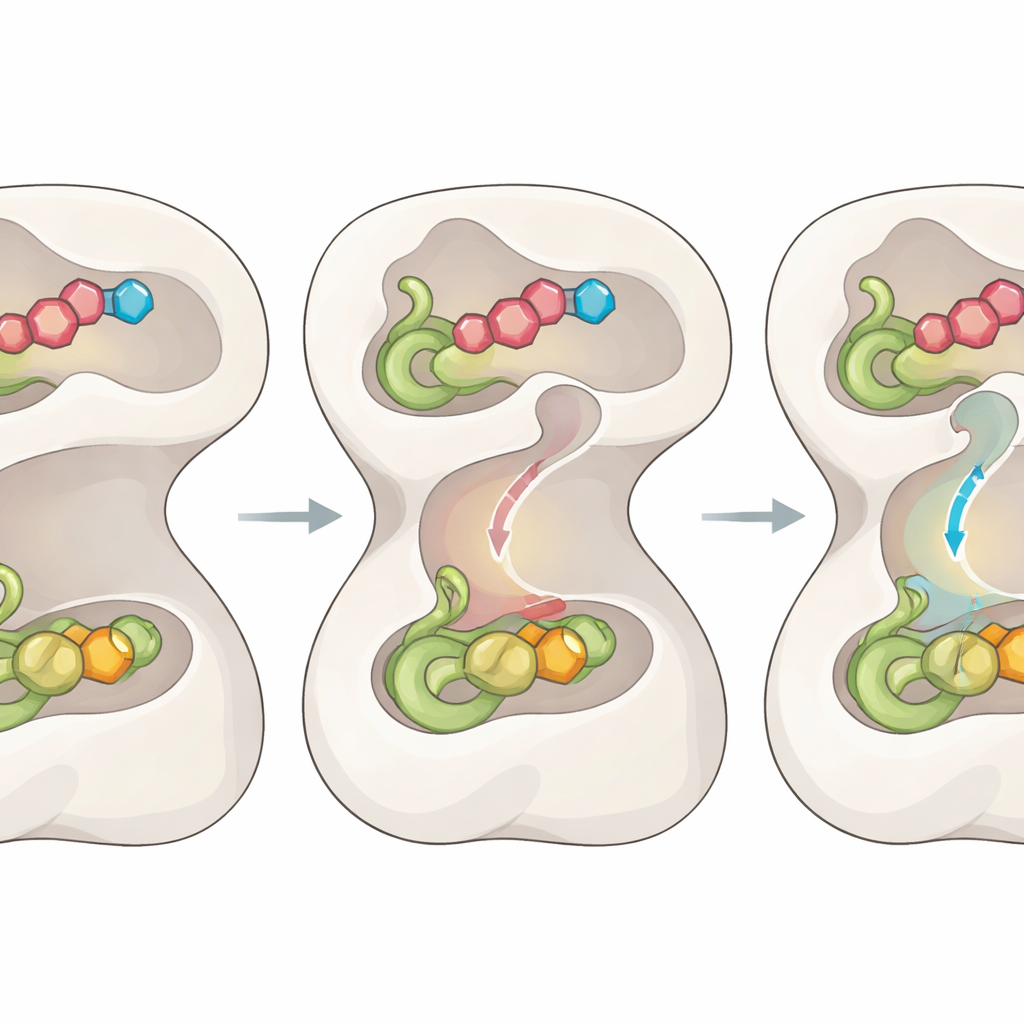
反応が進行するにつれて、酵素はただ待つのではなく、各化学ステップを信号として利用します。アンモニアを生成するドメインで共有結合的なチオエステル中間体が形成されると、先の動きは部分的に逆転します。これにより中心ループが弛緩し、ゲートが再配置されて逃げ道が閉じられ、トンネル両端にあるさらに二つのゲートが開きます。数個の“ボトルネック”残基の微妙なシフトが内部通路を拡げ、アンモニア分子がトンネルを通って直接第二の活性部位へ移動し、そこに閉じ込められた中間体と反応して最終生成物を生み出します。ゲート残基を変異させるとアンモニアが漏れたり反応の二つの半分が切り離されたりし、このゲーティングとチャネルのシステムが効率的な触媒には不可欠であることが確認されました。
構造知見から治療の道へ
FGAMSを触媒サイクルに沿って追うことで、ドメイン運動、可撓性ループ、内部ゲート、そして一時的なトンネルがどのように連携して化学を調整しているかの詳細な図が示されました。一般向けに言えば、酵素は小さなプログラム可能な工場のように振る舞い、すべての正しい部品がそろったときにだけ扉と内部コンベヤーを開くことで速度と安全性を確保しています。FGAMSはがん細胞のプリン生産を支え、肝臓腫瘍で予後不良と関連するため、今回の構造図や新たに特定された制御点は、トンネルを詰める、ゲートを固定する、あるいは重要な中間体を捕らえる薬を設計するための複数の足がかりを提供し、標的化された新しい種類の抗がん療法の可能性を示しています。
引用: Sharma, N., Zhou, W. & French, J.B. Structural and molecular basis for allosteric regulation and catalytic coupling of human phosphoribosylformylglycinamidine synthase. Nat Commun 17, 2732 (2026). https://doi.org/10.1038/s41467-026-69423-y
キーワード: プリン生合成, アロステリック制御, アンモニアチャネリング, がん代謝, クライオ電子顕微鏡構造