Clear Sky Science · ja
膵癌細胞固有のインフラマソーム蛋白質ASCは自然免疫とミトコンドリア代謝を結び付け、膵臓がんを促進する
この研究が重要な理由
膵臓がんは最も致命的ながんの一つであり、しばしば治療に十分な早期に発見されません。本研究は、膵腫瘍細胞内に存在する隠れた「配線」を明らかにし、一次防御としての免疫応答とこれらの細胞がエネルギーを生成・利用する仕組みを結び付けています。単一の免疫アダプター蛋白質であるASCが、細胞の代謝を書き換えることで腫瘍増殖を助けることを示すことで、この難治性がんに対する将来の治療法のための新しく極めて特異的な標的を示唆しています。 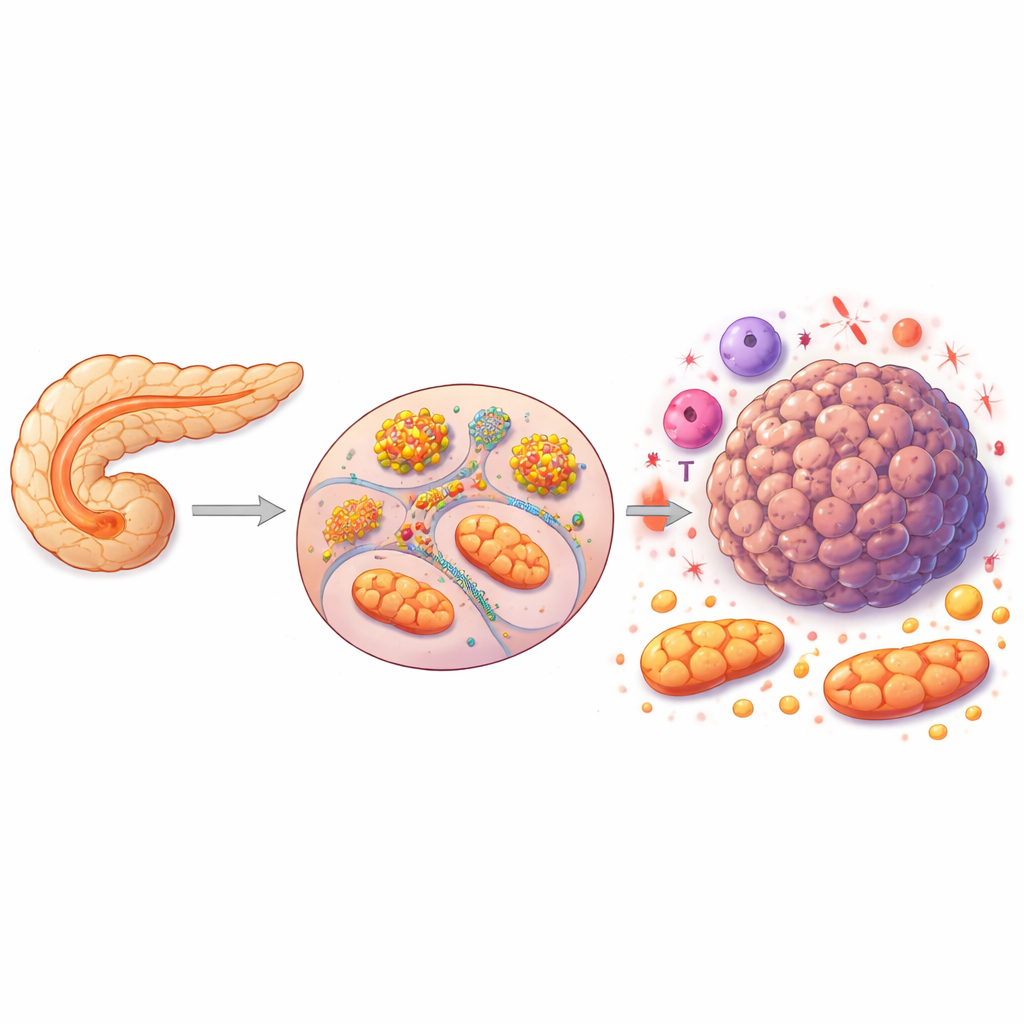
選択肢の少ない致死的ながん
大多数の膵臓がんは膵管上皮由来の膵管腺癌(PDAC)で、膵臓内の細い管を覆う細胞から発生します。これらの腫瘍は発見時に進行していることが多く、現行の化学療法や免疫療法はわずかな効果しか示しません。慢性炎症や免疫抑制的な腫瘍微小環境が膵臓がんの成長を助けることは知られていますが、異常な免疫と腫瘍挙動をつなぐ正確な分子は不明のままでした。こうした分子を同定できれば、がん内部の重要な「支援線」を断つことで病勢を抑える治療への道が開けます。
腫瘍細胞内に潜む免疫アダプター
著者らはASCに着目しました。ASCは通常、危険を感知して炎症シグナルを活性化するインフラマソームを組み立てる足場蛋白質です。複数の患者データセットを解析したところ、ASCをコードする遺伝子(PYCARD)は正常な膵臓と比べて膵腫瘍で一貫して高発現しており、疾患のさまざまな分子サブタイプで共通していました。ASCの高発現と、そのパートナー酵素であるカスパーゼ-1およびサイトカインIL-18の高値は、患者の生存率低下と関連していました。腫瘍生検を用いた高度な染色法により、ASCと活性化カスパーゼ-1は主にがん性の膵管細胞内に存在し、細胞内および周囲の組織に明るい点状の「スペック」を形成していることが示され、これは活性化したインフラマソーム複合体の存在を示す証拠です。 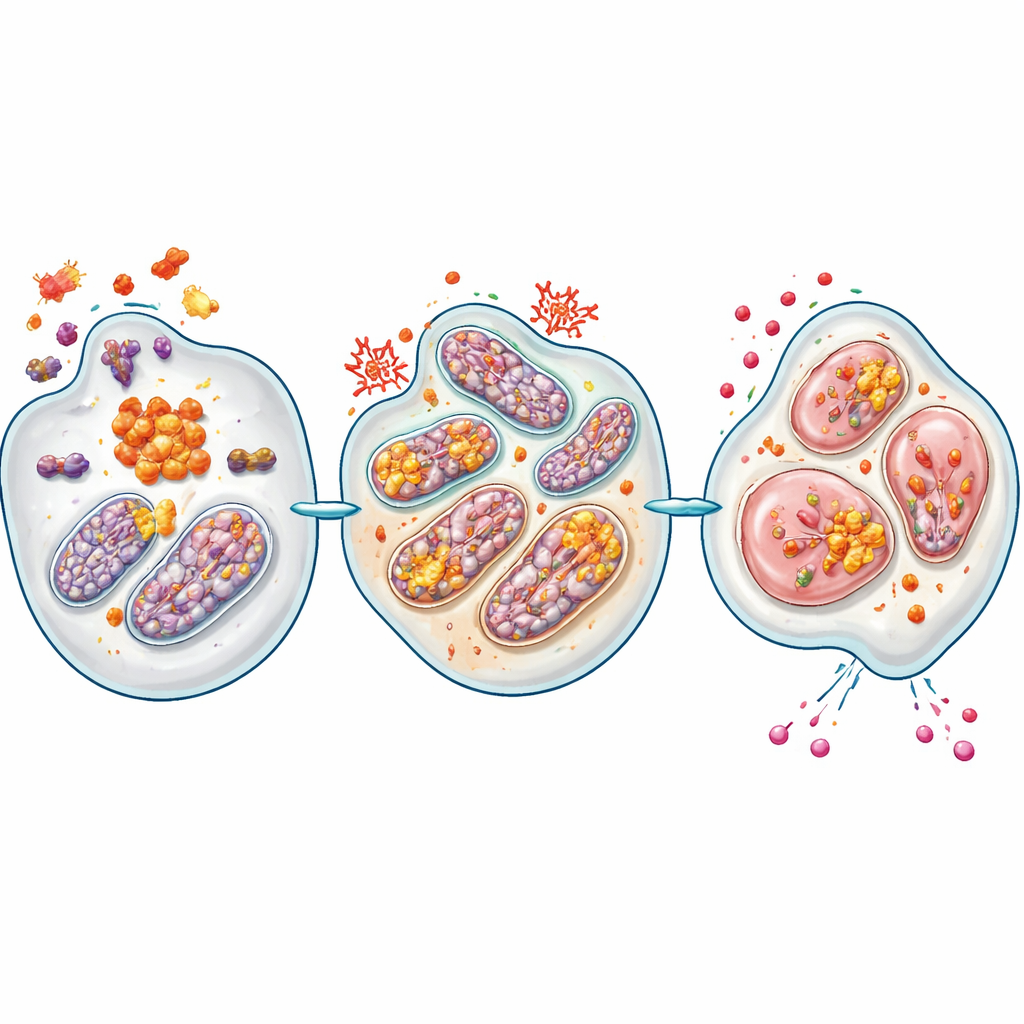
ASCを止めると腫瘍増殖が遅くなる
ASCが単に共存しているだけでなく膵臓がんの原因を助長しているかを検証するため、研究者たちは変異KrasおよびTrp53によって駆動される確立されたマウスモデルを用いました。これらのマウスでは膵臓内でASC、カスパーゼ-1、IL-18が上昇し、病変の進行に伴って循環するIL-18も増加しました。ASCを全身で欠失させると、マウスの膵臓ははるかに小さくなり、腫瘍の数と悪性度は大幅に減少し、肝転移は見られませんでした。膵管上皮に限定してASCを欠失させた場合でも強い(やや軽度な)保護効果が得られ、腫瘍細胞内のASCが主要な促進因子であることが強調されました。重要なのは、ASCの細胞外に存在する“スペック”を特異的なナノボディ薬で阻害しても腫瘍負荷と細胞増殖が低下したことで、ASCは細胞内外の両方で病勢を促進していることを示しています。
がん細胞の発電所を書き換える
さらに掘り下げるため、研究チームは全トランスクリプトーム解析を用いて、正常、腫瘍有り、ASC欠失の膵臓における遺伝子活性を比較しました。腫瘍を有するマウスでは免疫活性化に関連する遺伝子がオンになり、一方でミトコンドリア呼吸と酸化的リン酸化に関与する遺伝子(細胞の主要なエネルギー生産経路を担う)は抑制されていました。ASC欠失は概ねこのパターンを逆転させました。生化学的検査は、主要なミトコンドリア呼吸鎖蛋白質が腫瘍で減少しているが、ASCが欠失すると回復することを確認しました。腫瘍を有するマウスはミトコンドリアDNAコピー数が減少し、酸化的損傷が増え、乳酸値が上昇しており、酸素依存のエネルギー産生から“ワールブルク様”の好気的解糖への切り替えの兆候が見られました。ASCを除去するとミトコンドリアDNAコピー数が増加し、酸化ストレスと乳酸産生が低下しました。
マウスモデルからヒトがん細胞へ
これらの所見がヒト腫瘍にも直接当てはまるかを確認するため、著者らは小干渉RNAを用いて2つのヒト膵臓がん細胞株でASCレベルを低下させました。ASCを下げた細胞はカスパーゼ-1の活性化が減少し、増殖が遅く、コロニー形成能が低下し、乳酸とミトコンドリア由来スーパーオキシドの産生が減少しました。ミトコンドリア関連遺伝子とDNAコピー数は回復し、酸素消費量と予備呼吸能が増加して、より健全なミトコンドリア呼吸へのシフトを示しました。注目すべきは、これらのASC欠損細胞が解糖系を阻害する薬剤への感受性を低下させ、解糖依存性が減ったことと整合している点です。総じて、ASCは膵臓がん細胞を高速な増殖を支える高解糖・高酸化ストレス状態へ積極的に導くことが示されました。
今後の治療への意味
本研究は、ASCが自然免疫、慢性炎症、および膵臓がんを駆動する歪んだエネルギー代謝の間の中心的な“橋渡し”であることを明らかにしました。古典的な免疫細胞でのみ働くのではなく、膵管腫瘍細胞内のASCはインフラマソームを組み立ててIL-18の産生を促進し、ミトコンドリアの生合成を乱し、細胞を解糖へと駆り立てて攻撃的な増殖を助けます。マウスではASCを遺伝的に除去するか、細胞外スペックを中和することで病勢が遅延し、ASCやそのインフラマソーム複合体を標的とする薬剤が既存療法を補完する可能性が示唆されます。どの上流センサーがこの癌でASCに入力しているのか、IL-18を安全に阻害する最良の方法は何かといった未解決の課題は残りますが、本研究は膵管腺癌に対する新たな機序に基づく治療標的としてASCを追求する正当な根拠を提供します。
引用: Chey, Y.C.J., Kashgari, B., McLeod, L. et al. Cancer cell-intrinsic inflammasome protein ASC links innate immunity with mitochondrial metabolism in driving pancreatic cancer. Nat Commun 17, 2477 (2026). https://doi.org/10.1038/s41467-026-69398-w
キーワード: 膵臓がん, インフラマソーム, ミトコンドリア代謝, IL-18, がん免疫学