Clear Sky Science · ja
マクロファージ由来ラクトレートがMCT1で起動するヒストンH3リシン23ラクトリル化を介して真皮線維芽細胞の表現型再編を誘導し肥厚性瘢痕を生じさせる
なぜ一部の瘢痕は厚く盛り上がるのか
ほとんどの切り傷や火傷は最終的に薄く平らな瘢痕になります。しかし、かゆみや痛みを伴ったり可動域を制限したりする厚く盛り上がった組織の帯として治癒する創傷もあり、これが肥厚性瘢痕です。本研究は、これらの手ごわい瘢痕を生み出す予期しない駆動因子を明らかにします。それは、硬く治癒中の皮膚で免疫細胞が産生する一般的な代謝副産物であるラクトレートで、周囲の修復細胞をより攻撃的で瘢痕化しやすい挙動に再プログラムします。
正常な修復から問題となる瘢痕へ
健康な創傷治癒では、皮膚細胞が協調して傷を閉じ組織を再構築します。線維芽細胞は皮膚の深層にある主要な修復細胞で、一時的により強力な形態に切り替わりコラーゲン(皮膚のタンパク質足場)を産生します。傷が閉じるとこれらの細胞は再び静まります。しかし肥厚性瘢痕では、線維芽細胞がこの過剰活性状態に固着し、過剰なコラーゲンを厚く無秩序な束として沈着させます。著者らは正常皮膚と肥厚性瘢痕組織を比較して明確な代謝シフトを発見しました。瘢痕環境は高速な糖代謝を好み大量のラクトレートを生み、ラクトレートを細胞内に運ぶ輸送体MCT1の高発現も伴っていました。 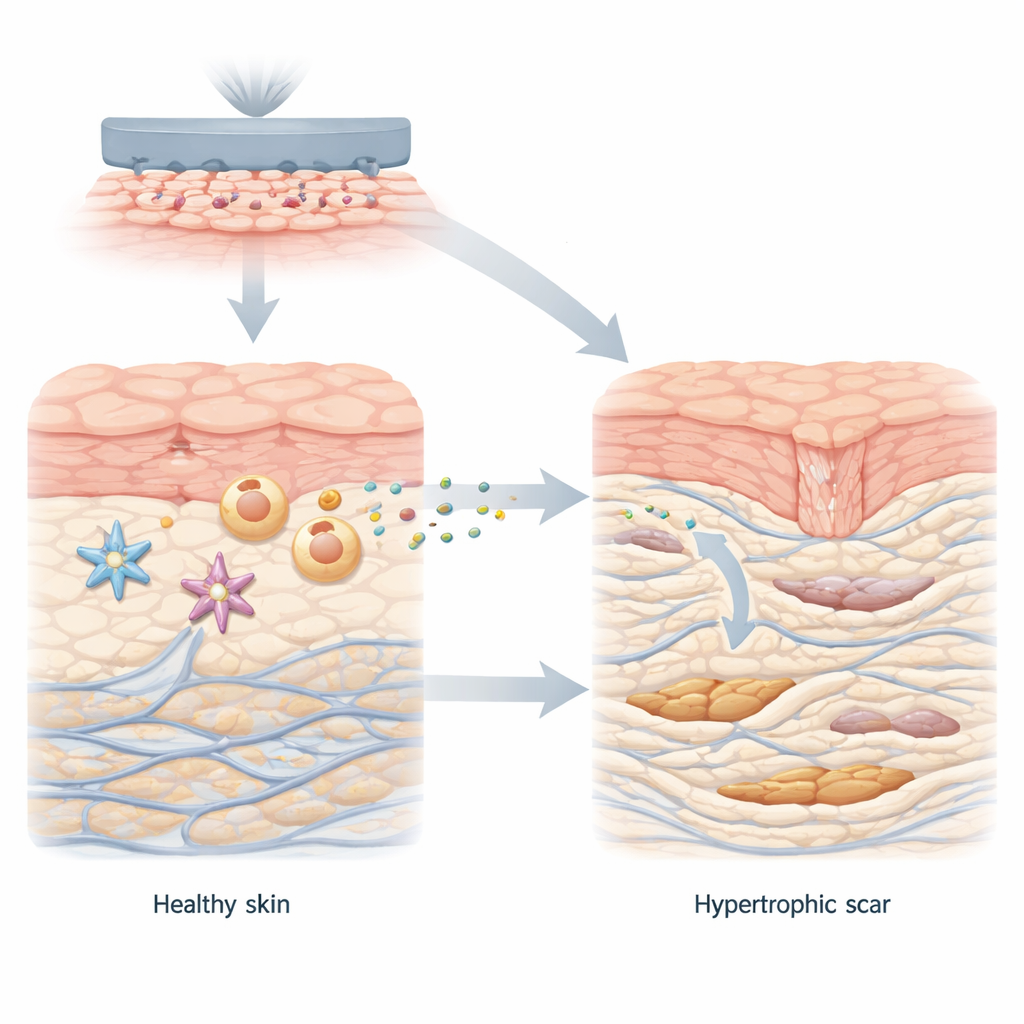
意外なラクトレート製造源としての免疫細胞
この大量のラクトレートがどこから来るのかを調べるために、研究チームはヒト皮膚およびマウスモデルから得たさまざまな細胞種、すなわちマクロファージ(破片を除去し治癒を調整する免疫細胞)、血管内皮細胞、線維芽細胞を解析しました。これらの細胞を、正常皮膚と瘢痕化した皮膚を模した柔らかい基材と硬い基材の上で培養しました。硬い表面では、マクロファージだけが高度に解糖性(糖を大量に消費する)モードに切り替わり、多量のラクトレートを放出しました。この現象は培養皿内でも実際の瘢痕組織でも観察されました。治癒中のマウス創傷からマクロファージを除去すると組織のラクトレート濃度が低下し瘢痕形成が軽減しました。これらの結果は、特に硬さを感知したマクロファージが瘢痕微小環境を形作る主要なラクトレート製造源であることを示しています。
線維芽細胞を書き換えるシグナルとしてのラクトレート
次に研究者たちは、この過剰なラクトレートが線維芽細胞にどのように影響するかを検討しました。硬い基材で培養したマクロファージ由来のラクトレート濃厚な培養上清で線維芽細胞を処理すると、細胞増殖が速くなり運動性が高まりコラーゲン産生が増加しました。これは攻撃的な筋線維芽細胞(myofibroblast)状態の特徴です。線維芽細胞上のMCT1輸送体を阻害するか、マクロファージのラクトレート産生を低下させると、これらの変化は大幅に抑えられました。線維芽細胞内では、取り込まれたラクトレートは単なるエネルギー源以上の役割を果たし、核内でDNAをパッケージするヒストンタンパク質に特異的な化学的標識を誘導しました。この標識はH3K23ラクトリル化と呼ばれ、瘢痕を形成する線維芽細胞で正常なものよりずっと高く、HEY2とCOL11A1という二つの主要な遺伝子をオンにするスイッチのように働き、瘢痕化シグナルを増幅しました。
自己強化する瘢痕化ループ
このヒストン標識によって駆動されるタンパク質群は強力なフィードバックループを形成します。HEY2はYAP1とSMAD2を含む経路の活性を高め、これは線維芽細胞をより収縮性が高くコラーゲンを産生する状態へ押しやることが知られています。COL11A1はコラーゲン関連の構造タンパク質で、線維芽細胞上のMCT1輸送体と物理的に相互作用してMCT1を安定化させ、ラクトレートの取り込みを効率化します。言い換えれば、細胞へ入るラクトレートが遺伝子制御を変え、さらにラクトレート取り込みとコラーゲン産生を促進して、線維芽細胞を瘢痕形成を促す恒常化した状態に固定してしまうのです。 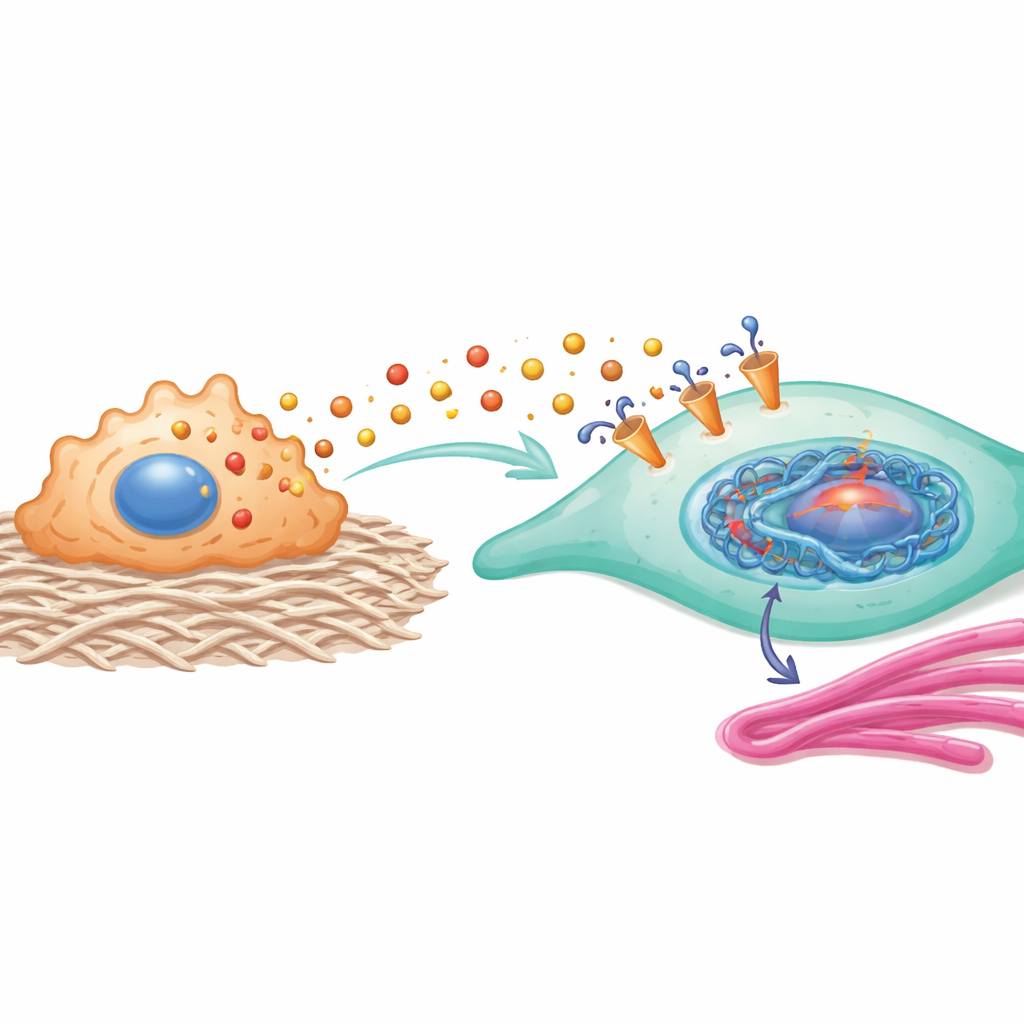
ループを弱めて治癒を改善する
このループを遮断すれば治癒が改善するかを検証するために、研究チームは線維芽細胞から選択的にMCT1を除去できるマウスと、MCT1を阻害する薬剤を用いました。いずれの場合も創傷はより速く閉じ、新しく形成された皮膚はより整然と見え、コラーゲン繊維は細く整列しており肥厚性瘢痕の特徴が減少しました。特異的なヒストン標識とその下流遺伝子の発現も低下しました。主要なラクトレート源であるマクロファージを枯渇させることや化学的にラクトレートを減らすことも同様に瘢痕抑制効果を示しました。これらの実験は、硬い創傷–マクロファージ–ラクトレート–線維芽細胞の連鎖が単なる相関ではなく病的瘢痕化の主要な駆動因子であることを示しています。
将来の瘢痕治療への示唆
この研究はラクトレートを単なる代謝の廃棄物から、力学、代謝、遺伝子制御を結びつける強力なメッセンジャーへと再定義します。マクロファージ由来ラクトレートがMCT1を介してヒストンを変化させ、線維芽細胞内で自己強化的な瘢痕化プログラムをスイッチオンする仕組みを示すことで、ラクトレート産生の調節、MCT1阻害、あるいは特定のヒストン修飾に干渉する薬剤といった有望な治療標的を浮かび上がらせます。将来的にはこれらの標的を利用して創傷がより速く、より平らで目立たない瘢痕で治るようにすることが期待されます。
引用: Yuan, Y., Xiao, Y., Zou, J. et al. Lactate derived from macrophages drives skin dermal fibroblasts phenotypic remodeling via MCT1-primed histone H3 lysine 23 lactylation in hypertrophic scar. Nat Commun 17, 2694 (2026). https://doi.org/10.1038/s41467-026-69388-y
キーワード: 肥厚性瘢痕, ラクトレートシグナル, マクロファージ–線維芽細胞クロストーク, ヒストンのラクトリル化, 創傷治癒療法