Clear Sky Science · ja
ミオフェルリンは被膜性RNAウイルスの後期vRNP輸送小胞の構成要素である
日常の健康にとっての重要性
季節性インフルエンザやその他の呼吸器感染症は日常的に感じられることが多いですが、世界では毎年何百万人もの命を奪っています。インフルエンザAや呼吸器合胞体ウイルス(RSV)を含む多くのウイルスは、急速に変異することでワクチンや抗ウイルス薬を回避します。本研究はウイルスが容易には変えられないもの、すなわち感染細胞からの脱出にウイルスが乗っ取るヒト細胞の仕組みに着目しました。その機構の共通の弱点を明らかにすることで、将来的に多様な呼吸器ウイルスを一度に抑える薬の可能性を示しています。
ウイルスが利用する細胞の輸送経路
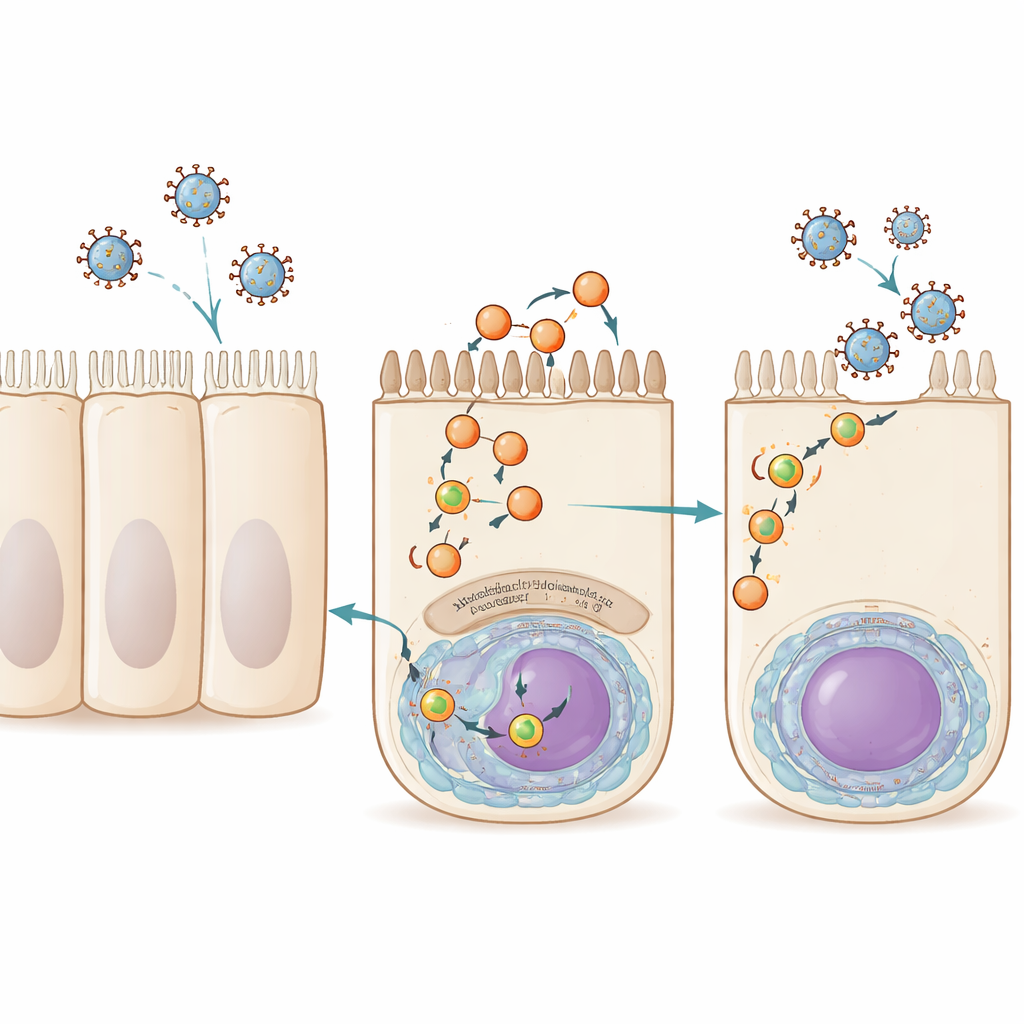
気道の細胞は外膜の断片をリサイクルする過程を絶えず行っています。小さな膜の泡(小胞)が細胞内の物質を細胞表面へ運び戻し、その輸送はRab11として総称されるタンパク質群によって導かれます。インフルエンザA、RSV、そしてセンダイウイルスに類するウイルスは、感染後期にこの経路を利用します。これらは自らの遺伝物質をリボ核タンパク質複合体としてRab11含有小胞に載せ、気道表面側の細胞頂端へ運び、そこで新しいウイルス粒子が芽生えて拡散します。これまで、これらの輸送小胞で明確に共有されている宿主因子はRab11だけであり、小胞がどのように形成され機能するのかについて大きな空白が残されていました。
新たな関与因子の発見:ミオフェルリン
研究者らはまず、感染の異なる時点でインフルエンザのゲノム包装機構に物理的に結合するヒトタンパク質が何かを問いかけました。ポリメラーゼに分子タグを付けたインフルエンザAウイルスを設計し、質量分析で感染の早期と後期にこの複合体に結合するヒトタンパク質をカタログ化しました。数百の候補の中で、後期に際立っていたのがミオフェルリンです。ミオフェルリンは筋肉発生、エンドサイトーシス、膜修復に関与するとされる大きな膜関連タンパク質です。肺由来細胞で小分子干渉RNAによりミオフェルリンの量を減らすか、小分子阻害剤で機能を妨げると、細胞はウイルスRNAやウイルスタンパク質を通常通り作っていましたが、感染性のあるインフルエンザ粒子の放出は大幅に減少しました。これはミオフェルリンがウイルスゲノムの複製には必要ないが、新しいウイルスが組み立てられ細胞を出る後期の段階で重要であることを示しています。
ウイルス輸送物質とともに移動するミオフェルリン
高解像度イメージングにより、感染時におけるミオフェルリンの局在が明らかになりました。非感染細胞ではミオフェルリンは主に核近傍から細胞縁に向かうRab11陽性のリサイクリング小胞と重なっており、いずれかのタンパク質の欠失はもう一方の正常な分布を乱します。インフルエンザ感染中、Rab11ネットワークはウイルスリボ核タンパク質を運ぶ拡大して不規則な小胞へと劇的に再編成されます。ミオフェルリンはこれらの再編成された小胞に保持され、ウイルスゲノムやRab11と強く共局在します。研究チームがウイルスゲノム複合体とそれを運ぶ小胞を凝集させる薬を使うと、ミオフェルリンも同じ凝集体に引き込まれ、後期の輸送構造の組み込み部品であり単なる付近の偶然の存在ではないことが確認されました。
複数の呼吸器ウイルスに共通するハブ
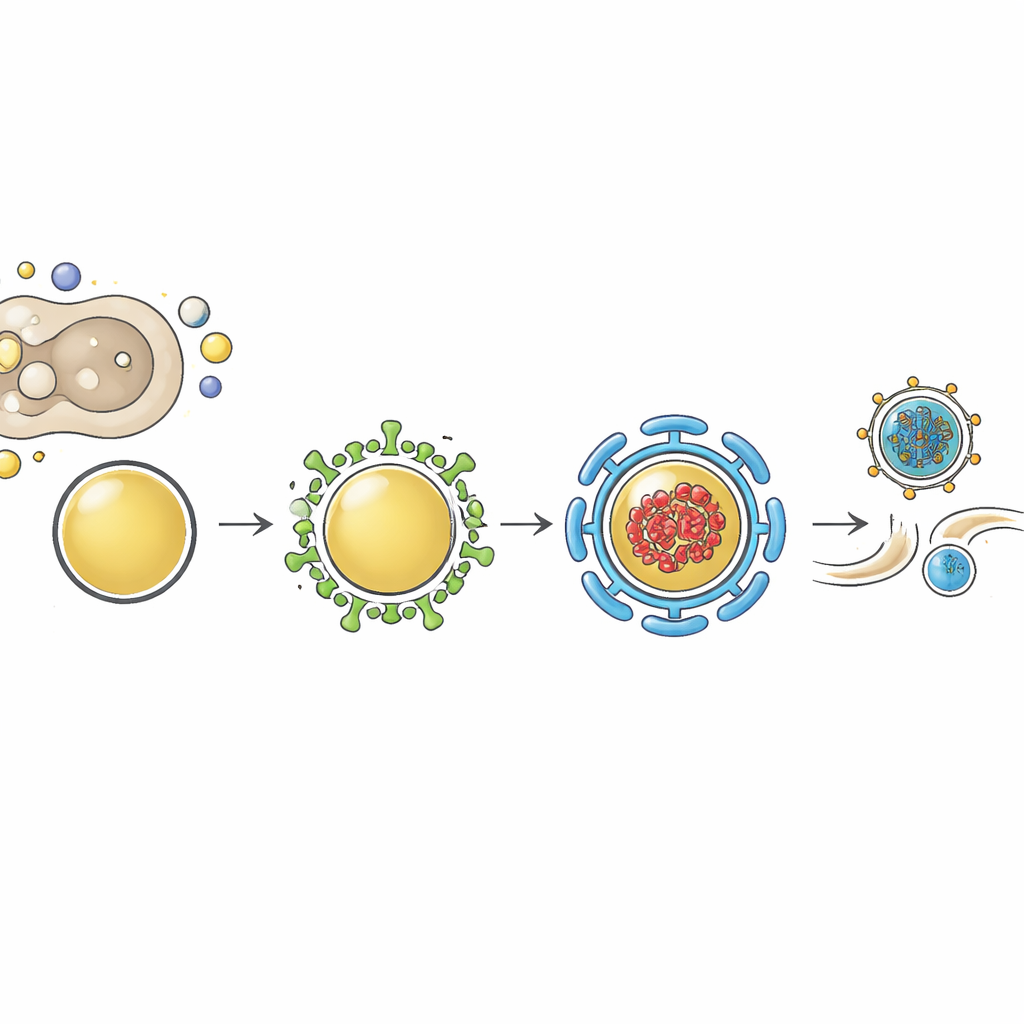
次に、ミオフェルリンへの依存性がインフルエンザに特有か、それとも広く共有されているかを調べました。肺細胞でミオフェルリンをノックダウンすると、RSVやセンダイウイルスに感染した場合でも感染性ウイルスの放出が大きく減少し、ウイルスRNAレベルは低下しませんでした。単一分子イメージングは、両ウイルスのゲノムがミオフェルリンとRab11とともに細胞質の点状スポットに集まっていることを示しました。これらは複製工場というより輸送ハブを表していると考えられます。このパターンは統一的な図を支持します:さまざまな生活様式を持つ被膜性呼吸器RNAウイルスは、完成したゲノムを細胞表面へ運んで被包・放出する時に同じRab11–ミオフェルリン小胞システムに収束します。
ミオフェルリンがウイルスを運ぶ小胞を形づくる仕組み
ミオフェルリンは膜やパートナータンパク質に結合できる複数の「C2」ドメインから構成されています。以前の研究はこれらのドメインの一つがEHDと呼ばれる膜再構築タンパク質群と関与することを示していました。本研究では、蛍光標識したEHD1およびEHD2がインフルエンザゲノムとRab11を運ぶ同じ再編成小胞内で検出され、とくにこれらの小胞が実験的に凝集されたときに顕著でした。EHD2の量を減らすことはミオフェルリンを減らすことと同様に、ゲノム複製に影響を与えずにインフルエンザの産生量を低下させました。さらに、ミオフェルリンを失うとEHD2タンパク質量が低下するため、ミオフェルリンはEHD2を膜上で安定化または正しく配置するのに寄与していると示唆されます。著者らは、ミオフェルリンがRab11陽性小胞上に位置しEHDタンパク質を呼び寄せて膜を造形し、ウイルス輸送に最適化された特殊な「不規則被覆小胞」の形成を完成させると提案しています。
将来の抗ウイルス戦略への示唆
総合すると、本研究はミオフェルリンを多くの被膜性呼吸器ウイルスが後期の重要な段階で依存する宿主のリサイクル経路の中心的な組織因子として位置づけます。ウイルスタンパク質のみを標的とするとしばしば急速な耐性が生じるため、複数のウイルスに共通して使われる宿主因子は魅力的な薬剤標的です。ミオフェルリンの機能、あるいはRab11やEHDタンパク質との協調を妨げることで、理論上はインフルエンザやRSVから、一部のコロナウイルスのようなRab11依存ウイルスに至るまで多様な病原体の拡散を遅らせたり阻止したりできる可能性があります。安全な治療法へと翻訳するには多くの作業が残されていますが、本研究は共有されるウイルスの脱出経路の詳細な地図を提供し、ミオフェルリンをその経路上の有望な絞扼点として浮かび上がらせています。
引用: Bonazza, S., Turkington, H.L., Sukumar, S. et al. Myoferlin is a component of late-stage vRNP trafficking vesicles for enveloped RNA viruses. Nat Commun 17, 2507 (2026). https://doi.org/10.1038/s41467-026-69386-0
キーワード: インフルエンザ, 呼吸器ウイルス, 小胞輸送, 宿主因子, ミオフェルリン