Clear Sky Science · ja
アミロイドβフィブリルの構造欠陥が二次核生成を駆動する
脳内タンパク質の小さな欠陥が重要な理由
アルツハイマー病や関連する脳疾患では、特定のタンパク質が長く糸状の構造、すなわちアミロイドフィブリルとして凝集します。これらのフィブリルは疾患の目印であるだけでなく、新たに生成される非常に毒性の高いタンパク質粒子(脳細胞を傷害する)を生み出す助長因子にもなります。本研究は単純だが強力な疑問を投げかけます:アミロイドフィブリル内部の稀な構造的「欠陥」が、新たな有害な成長を引き起こす主要なホットスポットとなっているのか?その答えは、タンパク質表面全体を狙うのではなく、いくつかの重要部位だけを標的にすることで、これらの疾患を遅らせたり阻止したりする新しい手法を示す可能性があります。 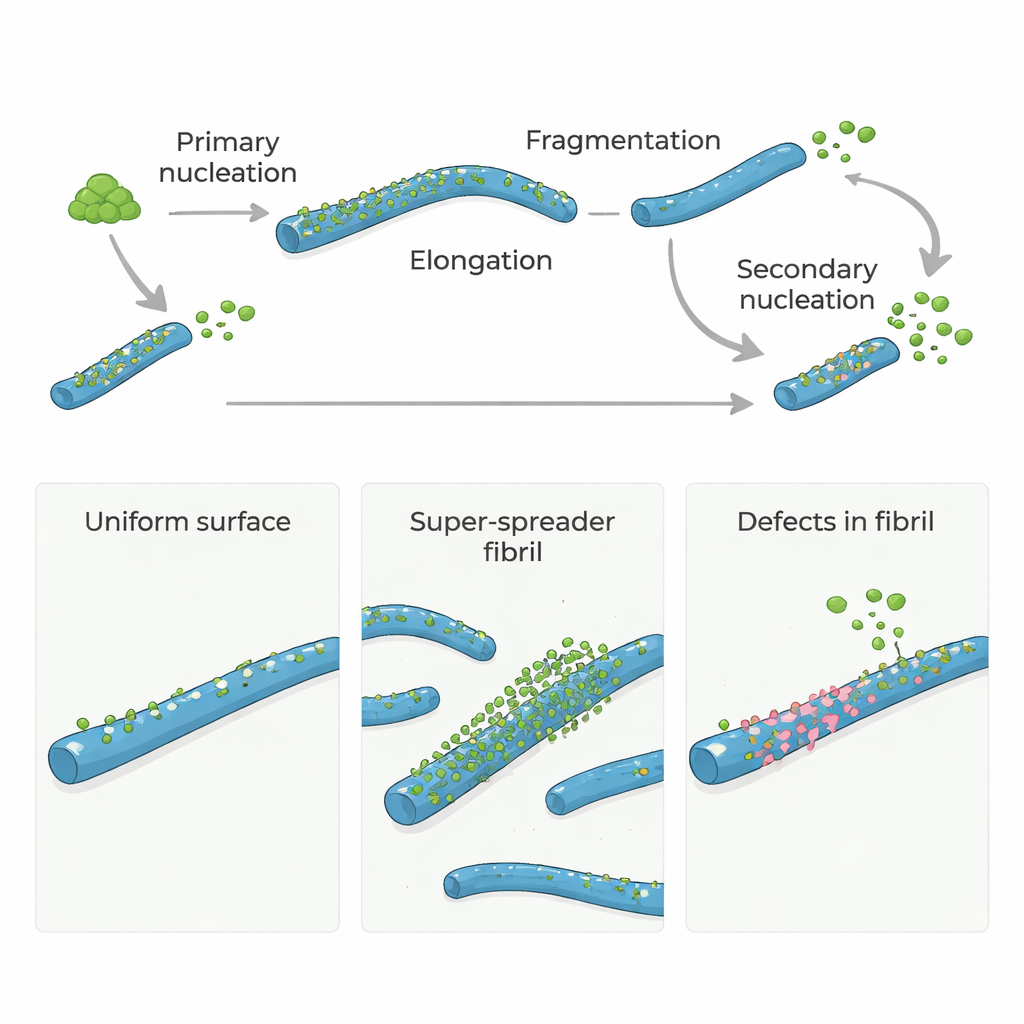
静かなタンパク質から暴走する連鎖反応へ
アルツハイロイドβ(Aβ)タンパク質はアルツハイマー病の中心にあるが、通常は自発的にすぐに凝集するわけではありません。始動するには、いくつかのモノマーがゆっくりと最初の小さなフィブリルに組み立てられる必要があり、これを一次核生成と呼びます。最初のフィブリルが存在すると、その末端により多くのモノマーが付加して急速に成長します。さらに重要なのは、既存のフィブリルが表面で新しいフィブリルを誘発する二次核生成です。この表面駆動型の過程は新たなフィブリルや小さな毒性オリゴマーを大量に生み出し、ゆっくりとした流れを暴走する連鎖反応へと変え得ます。
すべてのフィブリル表面が同じように危険か?
多くのモデルはアミロイドフィブリルの表面全体が二次核生成を触媒する能力において均一であると仮定してきました。しかし、最近の実験は表面のごく一部だけが実際に活性であることを示唆していました。この点を突き止めるために、著者らは天然の分子シャペロンであるBrichosを用いました。BrichosはAβ40およびAβ42(二つの主要なアミロイドβ形態)の二次核生成を阻害することが知られています。蛍光標識したBrichosがフィブリルにどれだけ結合するかを注意深く測定したところ、強く結合するものの結合数は非常に少なく、フィブリル中のおよそ100~150個のAβ分子につきBrichos分子が1つ程度でした。それでもこのまばらな被覆で二次核生成の90%以上を抑制でき、つまり稀で局所的な部位—表面全体ではなく—が新しい有毒集合体の生成を支配していることを示していました。
隠れた欠陥の役割を探る
これらの結果は、重要な核生成部位が構造的欠陥、すなわち成長過程で生じる小さな不整合(層のずれや部分的に露出した内部コアなど)である可能性を示唆しました。この仮説を直接検証するために、研究者らは二つの異なる条件下でAβ40フィブリルを成長させました。一方は「コントロール」フィブリルで、急速な成長と欠陥の動的トラップを促す強く過飽和した典型的条件で作られました。もう一方はゆっくりとした温度制御によるアニーリングプロトコールで作られ、溶解や修復が起こり得る低い駆動力、すなわち可溶性限界に近い条件で育てられました。高分解能クライオ電子顕微鏡解析では、両方のフィブリルは全体的な形状やねじれにおいて本質的に同じに見え、アニーリング過程が基本的な形態を変えていないことが示されました。 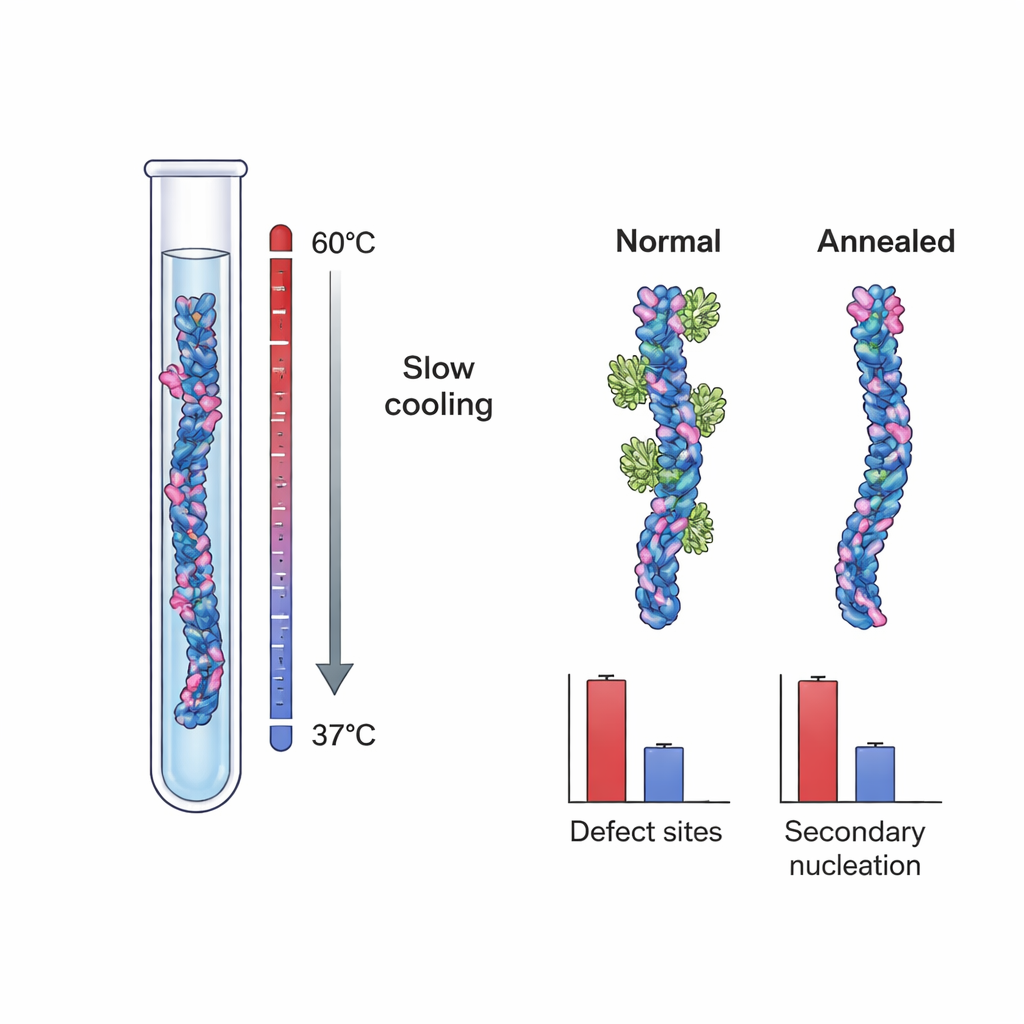
欠陥が少ないほど危険な成長部位も少ない
これら二種類のフィブリルに対するBrichos結合を測定したところ、顕著な差が明らかになりました。コントロールのAβ40フィブリルは約100モノマーにつき1つのBrichos結合部位を持ち、やはり稀だが重要な部位が存在しました。一方、アニーリングされたフィブリルでは約800モノマーにつき1つという非常に低い頻度で、部位頻度がほぼ90%減少していました。別の実験でこれらのフィブリルを“シード”として新しいAβ40溶液に加えたところ、アニーリングフィブリルは総質量をコントロールと揃えても新たな凝集を誘導する能力がはるかに低かったです。詳細な動力学モデル解析は、この種のシーディング力の低下が単にフィブリル長の違いだけでは説明できないことを示しました。代わりに、Brichos結合部位の数の減少と定量的に一致し、成長欠陥が二次核生成の主たる原動力であるという考えを強く支持しました。
治療的可能性を秘めた一般原理
熱力学的議論、過去の研究の再解析、複数のアミロイド形成タンパク質間の比較を総合すると、著者らは稀な成長欠陥がアルツハイマー関連のAβに限らず多くの系で二次核生成に中心的である可能性が高いと主張します。これらの欠陥はフィブリルの密に詰まった内部コアを部分的に露出させ、新しいオリゴマーやフィブリルが滑らかな表面上よりもはるかに容易に形成される足場を提供します。欠陥を主な犯人として認識することで創薬の新たな道が開けます。フィブリル表面のあらゆる相互作用を阻害するのではなく、これらの乏しい欠陥部位だけを覆う・修復する方向や、そもそも欠陥を生じにくくする条件を減らす方向を目指せます。実践的には、脳内のアミロイド形成タンパク質の実効濃度を下げることや、Brichosに着想を得た欠陥依存の核生成ホットスポットを認識して無力化する分子を設計することが挙げられます。もし成功すれば、こうした戦略は毒性オリゴマーの主要な供給源を断ち、アミロイド関連疾患の進行を遅らせる可能性があります。
引用: Hu, J., Scheidt, T., Thacker, D. et al. Structural defects in amyloid-β fibrils drive secondary nucleation. Nat Commun 17, 1933 (2026). https://doi.org/10.1038/s41467-026-69377-1
キーワード: アミロイドフィブリル, アルツハイマー病, 二次核生成, タンパク質凝集, Brichosシャペロン