Clear Sky Science · ja
STINGはTOXと協調してHO-1発現を抑制し、腫瘍浸潤CD8+ T細胞のフェロプトーシスと免疫療法抵抗性を引き起こす
がん治療にとってこの研究が重要な理由
現代のがん免疫療法は自己のキラーT細胞を解き放つことで働きますが、多くの腫瘍は依然としてこれらの細胞を無効化する手段を持っています。本研究は、腫瘍が利用するCD8+“キラー”T細胞内部の隠れた自己破壊スイッチを明らかにし、そのスイッチをオフにすることで免疫療法の効果を大きく高められることを示しています。
腫瘍と闘うT細胞内部の隠れた死の経路
腫瘍の中では、CD8+ T細胞は本来がん細胞を探して破壊する役割を担いますが、しばしば数が減り、鈍く、短命になります。著者らはT細胞内の二つの分子――DNA損傷を感知するSTINGと、T細胞疲弊に関連するタンパク質TOX――に注目しました。CD8+ T細胞でSTING、TOX、あるいは両方を欠損させたマウスを作成して複数の腫瘍を移植したところ、驚くべきことにいずれか一方を欠くT細胞を持つマウスは腫瘍の排除がはるかに良好でした。腫瘍の増殖は遅く、CD8+ T細胞の数は増え、これらのT細胞はインターフェロン-γやグランザイムBなどのがん細胞を殺す分子をより多く産生していました。これらは腫瘍内部で静かにT細胞を妨害する内部プログラムの存在を示しています。
鉄依存性の細胞死が免疫を弱める仕組み
腫瘍浸潤T細胞の遺伝子発現を調べると、腫瘍内の正常なT細胞はフェロプトーシスと呼ばれる特定の細胞死に備えていることが分かりました。アポトーシスとは異なり、フェロプトーシスは鉄過剰と細胞膜脂質の損傷の蓄積によって誘導されます。腫瘍細胞にさらされた通常のCD8+ T細胞では、鉄蓄積や脂質損傷を促進する遺伝子がオンになり、保護的な遺伝子は抑えられていました。これに対し、STING欠損またはTOX欠損のT細胞では逆のパターンが示されました:保護酵素であるHO-1やGPX4がより多く発現し、鉄レベルは低く、脂質過酸化は少なく、ミトコンドリアは健康でフェロプトーシスに抵抗していました。実験室での検証では、化学的にフェロプトーシスを阻害すると正常T細胞の生存が保たれ、STINGやTOXを除くことで自然に抵抗性が生じることが確認されました。
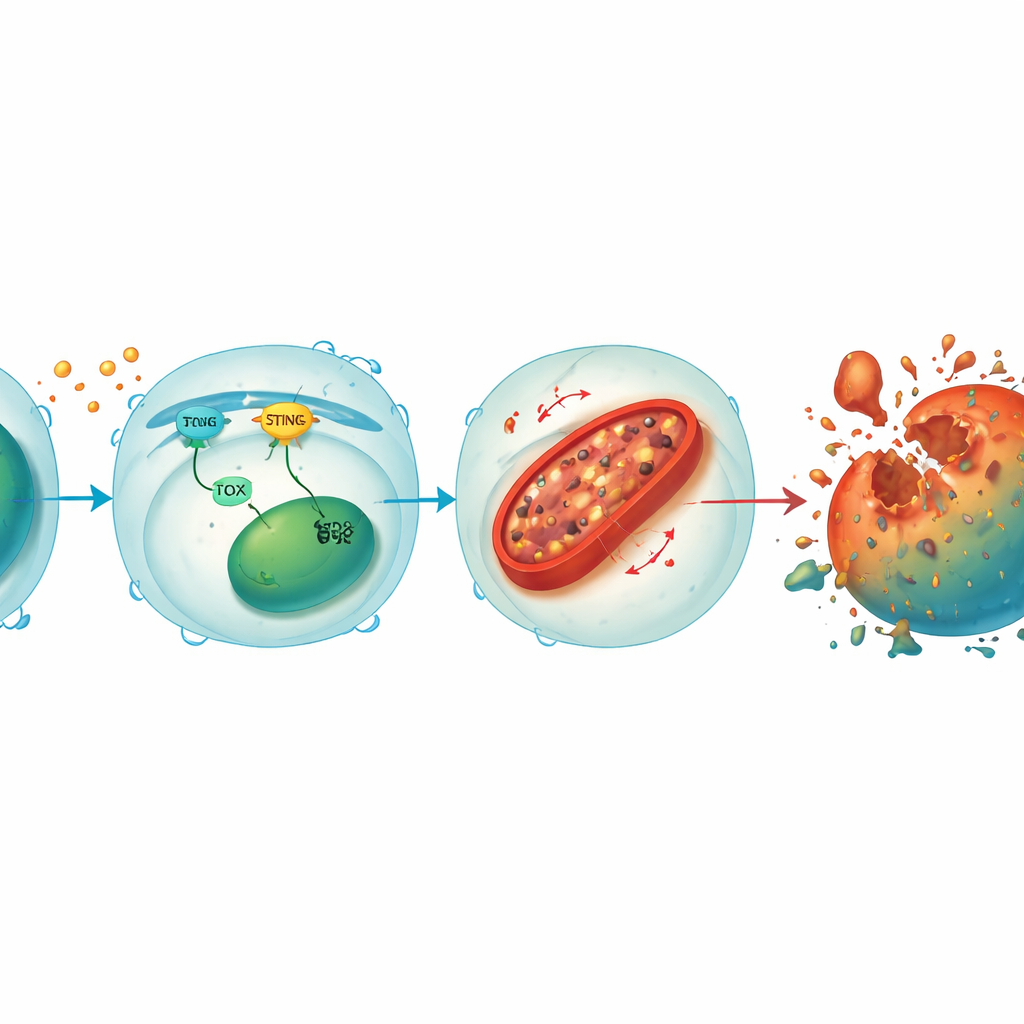
ストレス信号とミトコンドリア損傷をつなぐループ
さらに詳しく調べると、STINGとTOXはCD8+ T細胞内で自己増強するループを形成していることが分かりました。腫瘍やウイルスの信号がSTINGを活性化すると、それが下流因子を介してTOXを増強し、TOXは逆にSTING活性を維持する役割を果たします。両者は協調して通常は細胞内鉄を制御する酵素HO-1を抑えます。HO-1が抑制されるとミトコンドリアに鉄が蓄積し、活性酸素種の増加や膜脂質の酸化を引き起こします。このミトコンドリア損傷がエネルギー産生を枯渇させ、最終的にT細胞をフェロプトーシスに追い込みます。ノックアウトT細胞にSTINGやTOXを再導入すると鉄過負荷と細胞死が戻り、さらにHO-1を低下させると保護されたT細胞でさえ再び脆弱になったことから、HO-1がこの破壊的経路の中心的なブレーキであることが裏付けられました。
腫瘍由来ラクト酸が引き金を引く仕組み
腫瘍微小環境はがんの代謝変化に由来するラクト酸を豊富に含みます。本研究は、このラクト酸が単なる代謝廃棄物ではなく、T細胞のフェロプトーシススイッチを積極的に入れる役割を持つことを示しています。ほかの細胞と比べてCD8+ T細胞は特にラクト酸に敏感でした。特定の輸送体を通じてラクト酸が細胞内に入り込むと、鉄蓄積、ミトコンドリアの縮小、ミトコンドリアDNAの喪失、酸化損傷の増加を引き起こしました。同時にラクト酸はSTINGとTOXの活性を高め、さらにHO-1を抑制しました。STINGやTOXを欠くT細胞はラクト酸による障害に対してはるかに抵抗性がありました。主要なラクト酸輸送体を阻害する薬剤(AZD3965)でマウスのCD8+ T細胞を保護すると、腫瘍内でのT細胞存在が増え、腫瘍成長は遅くなり、T細胞でSTINGを遺伝学的に欠失させた場合と類似した利益が得られました。
脆弱性を治療上の利点に変える
これらの機構的知見は実用的な示唆を与えます。研究者らがアダプティブセル療法(実験室で活性化したT細胞を投与する手法)を用いたところ、STINGまたはTOXを欠損するように設計したT細胞は正常T細胞よりもはるかに強力に腫瘍を制御しました。さらに、これらの“フェロプトーシス耐性”T細胞をPD-1やTIM-3のチェックポイント阻害剤、シスプラチン化学療法、あるいはSTING活性化薬と組み合わせると、いずれか単独療法よりも著しく優れた腫瘍縮小が得られました。最後に、子宮頸がん患者の腫瘍検体では、腫瘍浸潤リンパ球におけるTOX高発現とHO-1低発現が予後不良と関連しており、この経路が臨床転帰にも影響を与えていることが示唆されました。
将来のがん治療に向けて
平たく言えば、本研究は腫瘍が鉄を燃料とする細胞死を誘導して私たちの最良の抗がんT細胞を内部から“さび付かせる”仕組みを明らかにしました。ラクト酸–STING–TOX回路はHO-1による保護を低下させ、ミトコンドリアを損傷しフェロプトーシスへと導き、効果的なCD8+ T細胞の戦力をそぎます。この回路を断つ――STINGやTOXを欠いたT細胞を設計すること、HO-1を高めること、あるいはラクト酸の流入を遮断すること――でT細胞を生存させ、活力を保ち攻撃態勢にさせることができます。本研究は代謝的・遺伝的調整を既存薬と組み合わせる次世代免疫療法の方向性を示し、抵抗性を克服してより持続的ながん制御をもたらす可能性を示しています。
引用: Zhu, Q., Zhang, Jb., Nie, Cp. et al. STING synergizes with TOX suppressing HO-1 expression to trigger ferroptosis in tumor-infiltrating CD8+ T cell and immunotherapy resistance. Nat Commun 17, 2543 (2026). https://doi.org/10.1038/s41467-026-69350-y
キーワード: がん免疫療法, CD8 T細胞, フェロプトーシス, 腫瘍微小環境, STING TOX HO-1 経路