Clear Sky Science · ja
Seq-Scope-eXpanded: 光学解像度を超える空間オミクス
細胞をより鮮明に見る
私たちの体は無数の小さな細胞で構成され、それぞれが活発に働いていますが、その内部の活動は強力な顕微鏡でも見えにくいことが多い。本論文はSeq-Scope-Xという技術を紹介します。これは組織内および細胞間の正確な座標でどの遺伝子やタンパク質が活性化しているかを前例のない鮮明さでマッピングできるもので、発生、免疫系、がんや肝損傷といった疾患の研究を変える可能性があります。
なぜ分子をその場でマップするのか?
細胞は孤立して働くわけではなく、近隣の細胞と関係を持ち、層を形成し、位置に応じて専門化します。従来の遺伝子解析は組織を分解してしまうため、この空間文脈を失います。近年の「空間オミクス」ツールは分子をその場に留めますが、トレードオフがありました。イメージングベースの方法は非常に細かな構造を可視化できますが、通常追跡できる遺伝子の数は限られます。一方でシーケンシングベースの方法はほぼすべての遺伝子を一度に読めますが、微細な特徴をぼかしてしまい、しばしば数マイクロメートルにわたって信号が拡散します—多くの亜細胞構造より大きいことがあるのです。著者らはこのギャップを埋めることを目指しました:シーケンシングの持つ偏りのない豊富な情報を保ちつつ、現代の顕微鏡に匹敵する、あるいはそれを超える解像度を達成することです。
光学的限界を超えるための組織の伸長
Seq-Scope-Xの核心は一見単純です:組織自体を優しく拡大して、元のナノメートル単位の構造を解像しやすくする。チームはまずRNA分子(または抗体に結合した特別なDNAタグ)を組織切片の周りに形成した軟らかいハイドロゲルに固定します。次に元の組織を消化して取り除き、塩溶液でゲルを膨張させ、相対位置をほぼ保ったまま物理的に約3倍に伸長します。この拡張されたゲルをキャプチャープローブでコーティングされた超高密度シーケンシングチップの上に載せます。温度管理を慎重に行うことで、固定された分子はゲルから放出されチップに再結合し、チップをシーケンスすることで各微小座標に存在した遺伝子やタンパク質が明らかになります。 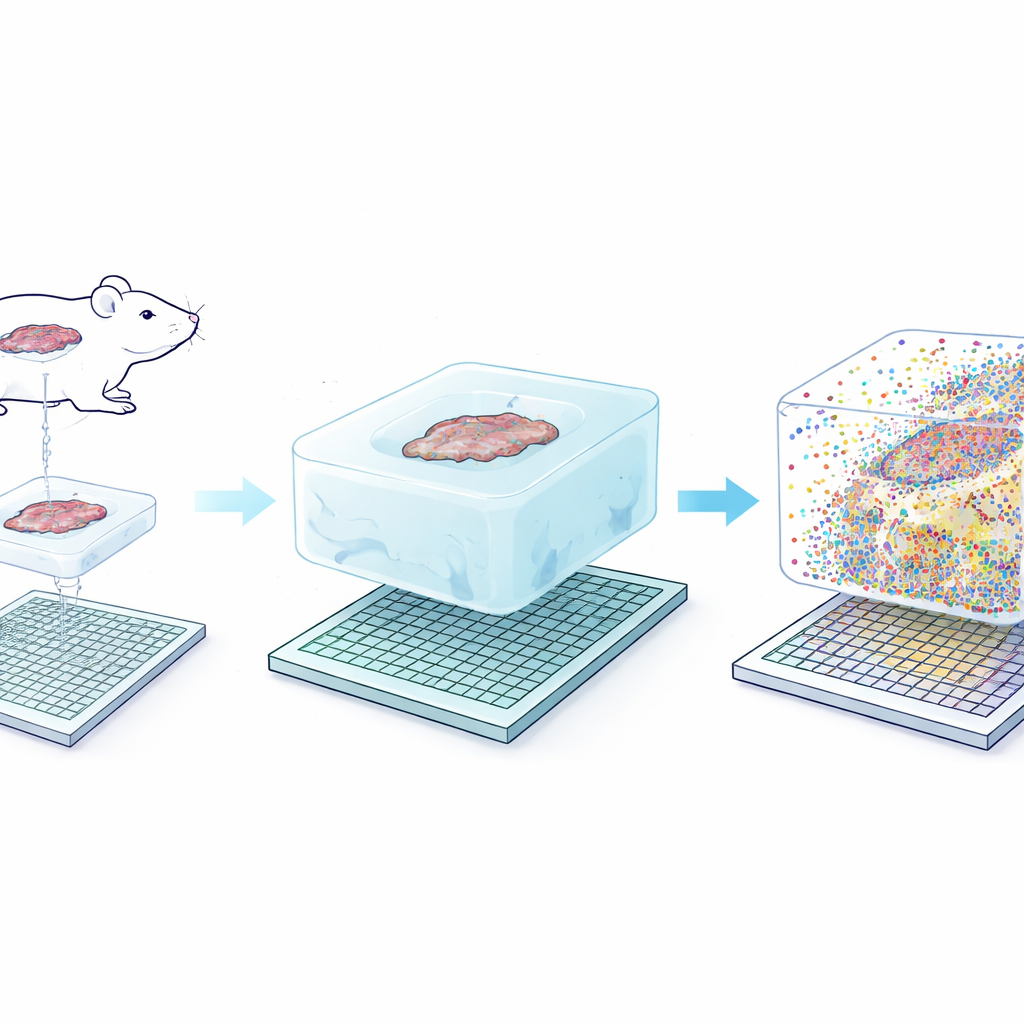
ぼんやりした細胞から亜細胞マップへ
研究者らがSeq-Scope-Xをマウス肝臓に適用したところ、空間解像度は約0.6マイクロメートルから約0.2マイクロメートルへと向上し、1平方ミリメートル当たりの測定可能な位置数はほぼ10倍に増えました。実際的には、以前はぼやけた信号の塊に見えたものが個々の細胞の鮮明な輪郭として分解されるようになりました。さらに注目すべきは、まだ完全に処理されていないRNA(未スプライス)が核の中心部にきっちりと並び、一方で成熟したRNA(スプライス後)は周囲の細胞質を描いていたことです。これにより著者らはRNAのみで細胞境界を描き、ほぼすべての肝細胞について核と細胞質の遺伝子発現を分離することができました。従来のシーケンシングベースの方法ではそこに到達するのは困難でした。
分裂した“個性”を持つ細胞
この新たな鮮明さにより、チームは肝細胞内に予期せぬ形の分子的な“二重生活”を発見しました。肝小葉の門脈側の血管から中心側の血管へと続くよく知られた勾配に沿って、肝細胞は異なる代謝タスクに特化します。Seq-Scope-Xは多くの細胞で核内の遺伝子パターンが周囲の細胞質のパターンと一致していないことを示しました。およそ3分の1の肝細胞は、核のプロファイルがあるゾーンに一致し、細胞質のプロファイルが隣接する別のゾーンに一致しているように見えました。MERFISHや単一分子RNA蛍光法を含む独立したイメージング法は、個々の転写産物が核または細胞質のいずれかに集中し得ることを確認しました。これらの発見を総合すると、肝細胞は代謝的役割を時間とともに動的に切り替え得ることが示唆され、核は将来の状態への準備を行い、細胞質は現在の状態を反映している可能性があります。 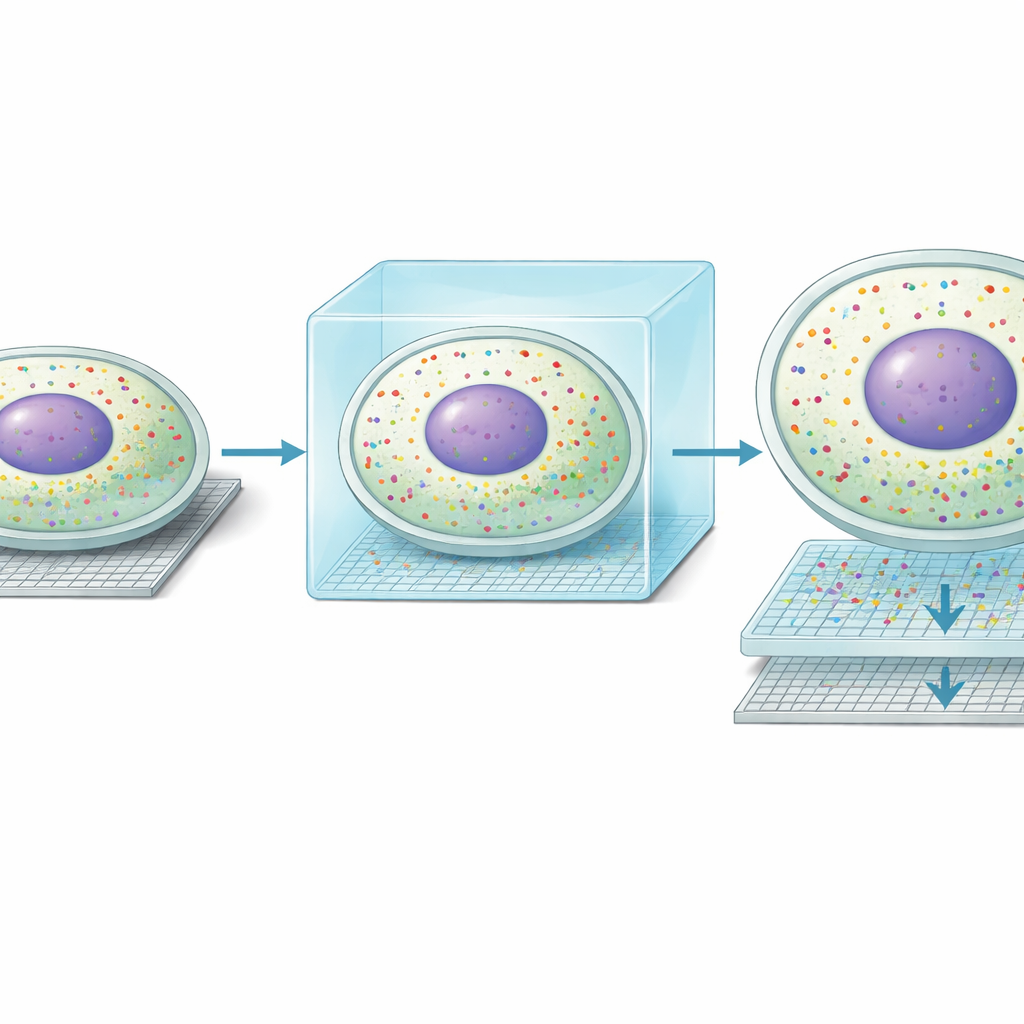
肝臓を超えて:脳、腸、免疫組織
著者らはSeq-Scope-Xが他の臓器でも機能するかを試しました。脳では、異なるニューロン型や支持細胞をきれいに分離し、核まわりのRNAの亜細胞パターンを明らかにしました。結腸では、杯細胞の異なるサブタイプやクリプトから表面への軸に沿った結腸上皮細胞の層を解像し、再び核特有のシグネチャを捉えました。おそらく最も劇的なのは、マウス脾臓とヒト扁桃でDNAバーコード化抗体を用いることでタンパク質へ手法を適用した点です。Seq-Scope-Xは100を超える細胞表面マーカーを単一細胞解像度で同時にマップでき、密に詰まったT細胞とB細胞のサブセットや髄系細胞を識別しました。より膨張可能なゲル化学へ切り替えることで、実効解像度を真のナノスケールへ近づけつつ、組織構造を十分に保持して詳細なマッピングを可能にしました。
今後の意義
Seq-Scope-Xは、シーケンスの前に組織を物理的に拡大することで長年の解像度の限界を克服できることを示し、顕微鏡レベルに近いほぼ同等の詳細を、同時に数千の遺伝子やタンパク質タグを読み出しながら提供します。一般の観察者にとっては、研究者がどの細胞がどこにあるかを示すだけでなく、各細胞のさまざまな部分で何が起きているかを明らかにする「分子アトラス」を構築できるようになったということです。こうしたマップは、組織が損傷にどう応答するか、免疫細胞がリンパ組織や腫瘍内でどのように組織化するか、あるいは細胞内部の微妙な変化がどのように疾患を予告するかを説明する助けになるでしょう。カバレッジを拡大し、いくつかの染色パネルを改善するためのさらなる改良は必要ですが、Seq-Scope-Xは健康と病気の基盤となる微視的風景を覗く強力な新たな窓を開きます。
引用: Anacleto, A., Cheng, W., Feng, Q. et al. Seq-Scope-eXpanded: spatial omics beyond optical resolution. Nat Commun 17, 2564 (2026). https://doi.org/10.1038/s41467-026-69346-8
キーワード: 空間トランスクリプトミクス, 組織膨張, シングルセルオミクス, 空間プロテオミクス, 肝臓のゾーネーション