Clear Sky Science · ja
腸内微生物由来のIPAは、腸内HMGCS2を介したケトジェネシスを制御して粘膜修復を促進し、潰瘍性大腸炎を防護する
傷ついた腸において腸内細菌が重要な理由
炎症性腸疾患(IBD)や強力な医療処置後のように腸の内層が損なわれると、有害物質が血流に漏れ出すのを防ぐためにこの内側の「皮膚」を迅速に修復する必要があります。本研究は、腸内の共生細菌が作る単一の分子が腸の自己修復を助ける仕組みを明らかにし、免疫系を広範に抑えることなく慢性腸疾患を治療する新しい方策を示唆します。
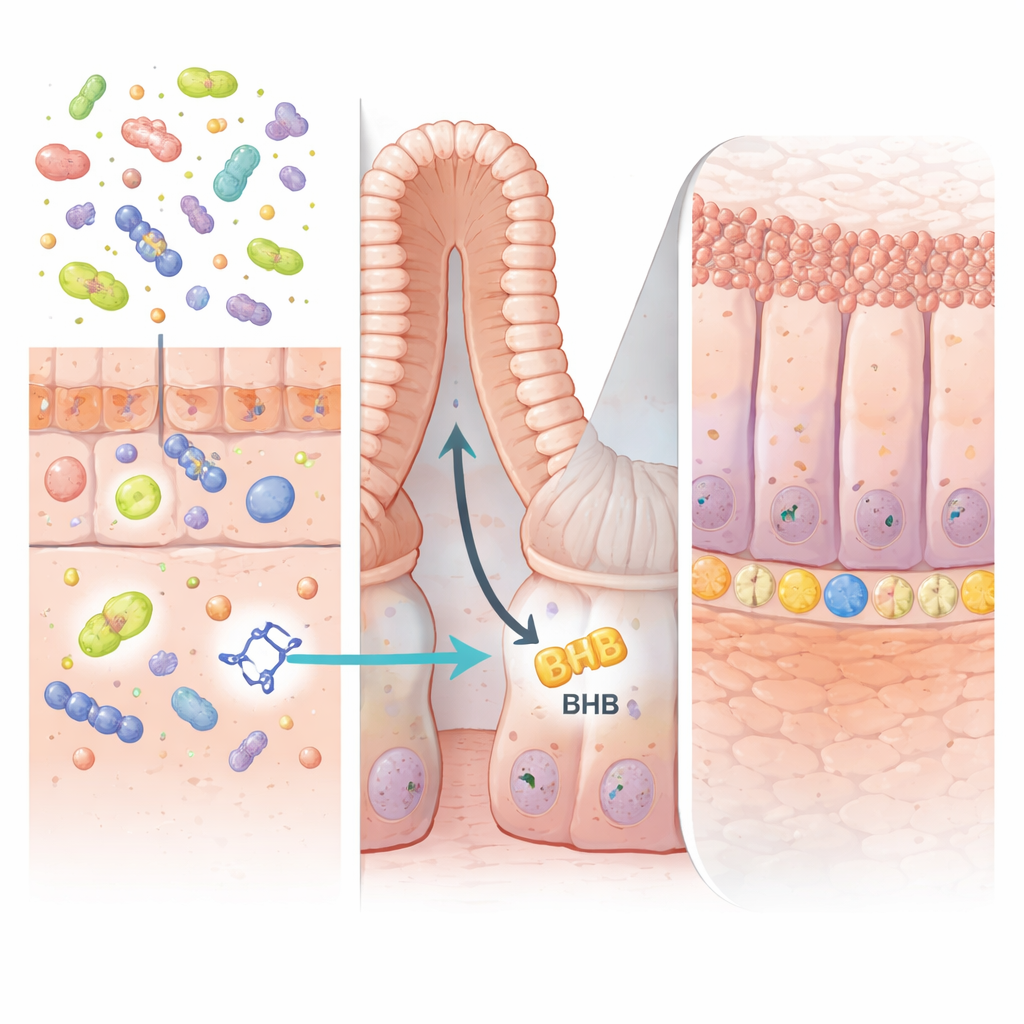
有益な微生物からのシグナル
研究者らはまず、IBD患者と健常者の糞便サンプル、ならびに複数のマウス結腸炎モデルから化学的フィンガープリントを比較しました。数百もの分子の中でひとつが際立っていました:インドール-3-プロピオン酸(IPA)で、必須アミノ酸トリプトファンの分解産物を一部の腸内細菌が生成します。IPAのレベルはクローン病患者や結腸炎マウスで一貫して低く、健常対照よりも減少していました。これはIPAの喪失が腸内層が炎症を起こして修復に失敗するときに生じる問題の一部であることを示唆します。
腸の防御壁を強化する
IPAが単に病気の指標でなく防御的に働くかを検証するため、研究チームは化学性結腸炎や放射線損傷を含む複数の腸損傷を誘発する前にマウスにIPAを投与しました。十分な量のIPAを受けたマウスは、結腸がより長く健康的で、顕微鏡的に見て炎症性変化が少なく、粘液層が厚く細胞間接着が強固でした。炎症性マーカーの漏出は減り、保護的粘液を産生する杯細胞が増加しました。重要なのは、これらの効果は常在微生物を持たない無菌マウスでも観察され、IPAが存在すれば他の微生物を必要とせずに腸粘膜に直接作用し得ることを示した点です。
幹細胞に特別なエネルギーを供給する
IPAの作用の鍵は、幹細胞が存在して絶えず上皮を更新する腸の「クリプト」と呼ばれる微小ポケットの奥深くにありました。著者らは、IPAが腸上皮細胞でPPARαというタンパク質を活性化することを示しました。これがHMGCS2という酵素の産生を促進し、ケトジェネシス—高エネルギー分子であるβ-ヒドロキシ酪酸(BHB)を生成する過程—を駆動します。腸壁内でのBHBの上昇はLGR5陽性の幹細胞を刺激して拡張・再生を促進し、損傷組織をより速く修復しました。マウスの腸上皮細胞からHMGCS2やPPARαを選択的に欠失させると、IPAはもはや幹細胞活性を高めたり結腸炎から保護したりできなくなり、このケトン産生経路が不可欠であることが確認されました。
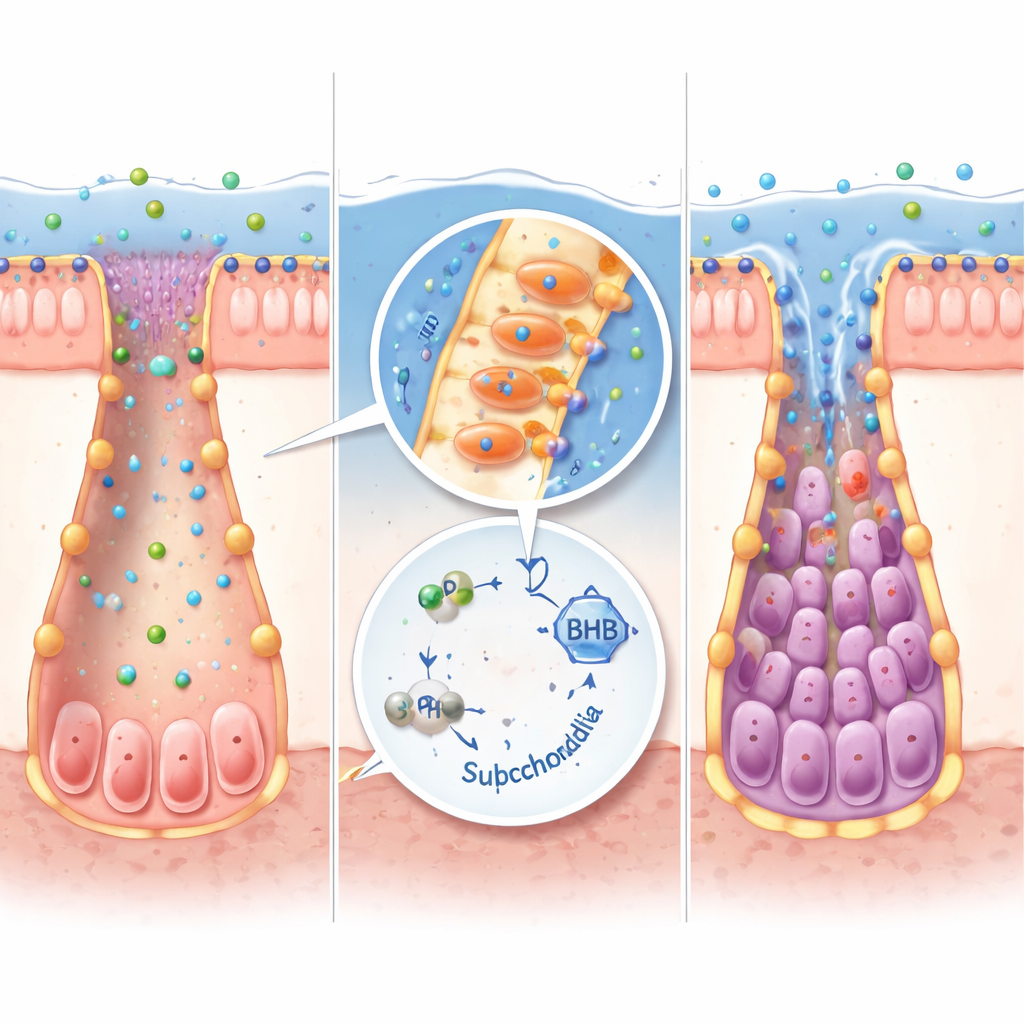
細菌の工場から人の組織へ
すべての腸内細菌がIPAを作れるわけではありません。大規模なマイクロバイオームデータセットを再解析した結果、Peptostreptococcus russelliiがIPAの主要な産生菌として特定され、複数のIBDコホートで減少していることが分かりました。培養実験ではこの細菌がトリプトファンを効率よくIPAに変換しました。無菌マウスにP. russelliiを定着させるとIPAレベルが上昇し、ケトン産生関連遺伝子が活性化され、幹細胞マーカーが増加し、一般的な微生物移植を受けたマウスと比べて結腸炎の重症度が低下しました。同じIPA–ケトン経路は、マウスとヒト由来の小型腸オルガノイドでも機能し、IPAまたはBHBを添加すると幹細胞が炎症性損傷後に回復しやすくなり、同時に炎症性シグナルが抑えられました。
将来の治療に向けて意味するところ
総合すると、本研究は単純だが強力な事象の連鎖を示します:特定の腸内細菌が食事由来のトリプトファンをIPAに変換する;IPAが腸細胞内の代謝スイッチを活性化する;そのスイッチがBHBの産生を高める;BHBは腸粘膜を再建する幹細胞を再活性化する。IBDや腸のバリアを損なう他の状態に苦しむ人々にとって、食事、標的型プロバイオティクス、または設計薬剤を通じてIPAを回復させるかその作用を安全に模倣する治療は、広範な免疫抑制を伴わずに真の粘膜修復を促進する可能性があります。患者でのさらなる研究は必要ですが、この微生物–代謝産物–幹細胞軸は腸を内側から修復する有望な新たな視点を提供します。
引用: Zhang, Y., Tu, S., Shao, X. et al. Microbiota-derived IPA protects against colitis by regulating intestinal HMGCS2-mediated ketogenesis to facilitate mucosal healing. Nat Commun 17, 2437 (2026). https://doi.org/10.1038/s41467-026-69341-z
キーワード: 腸内マイクロバイオーム, 腸管幹細胞, 炎症性腸疾患, 微生物代謝産物, 粘膜修復