Clear Sky Science · ja
CD38はミトファジーを介してMAVSを分解し、鼻咽頭がん細胞のⅠ型インターフェロン分泌を抑制してCD8+T細胞による抗腫瘍免疫を損なう
がん治療にとっての重要性
鼻咽頭がんは鼻の奥に発生するがんで、特に東アジアや東南アジアで多く見られます。自己のT細胞を解き放つ免疫療法は一部の患者の予後を変えましたが、多くの患者は恩恵を受けられていません。本研究は腫瘍細胞内に潜むブレーキを明らかにします。CD38と呼ばれる分子が内部の警報システムを静かに遮断し、がんを攻撃するCD8 T細胞の働きを弱めているのです。このブレーキの仕組みを理解し解除することで、既存の免疫療法がより多くの患者に効く可能性があります。
腫瘍細胞上の隠れたスイッチ
研究者たちはCD38に注目しました。CD38は多くの免疫細胞に見られるタンパク質ですが、鼻咽頭がん細胞にも発現します。これまでの研究でCD38はPD-1/PD-L1を標的とするチェックポイント阻害薬に対する抵抗性と関連付けられていました。本研究では、腫瘍細胞内のCD38がCD8 T細胞の認識および破壊能を直接変えるかを問いました。ヒト腫瘍細胞をCD38のあるものとないものに分け、活性化したヒトCD8 T細胞と共培養すると、腫瘍細胞からCD38を除くとT細胞の攻撃力は格段に高まりました:主要な攻撃分子の分泌が増え、生存率が向上し、より多くの腫瘍細胞を殺しました。CD38を再導入するとT細胞機能は低下し、CD38が腫瘍内在の免疫抑制因子であることが示されました。
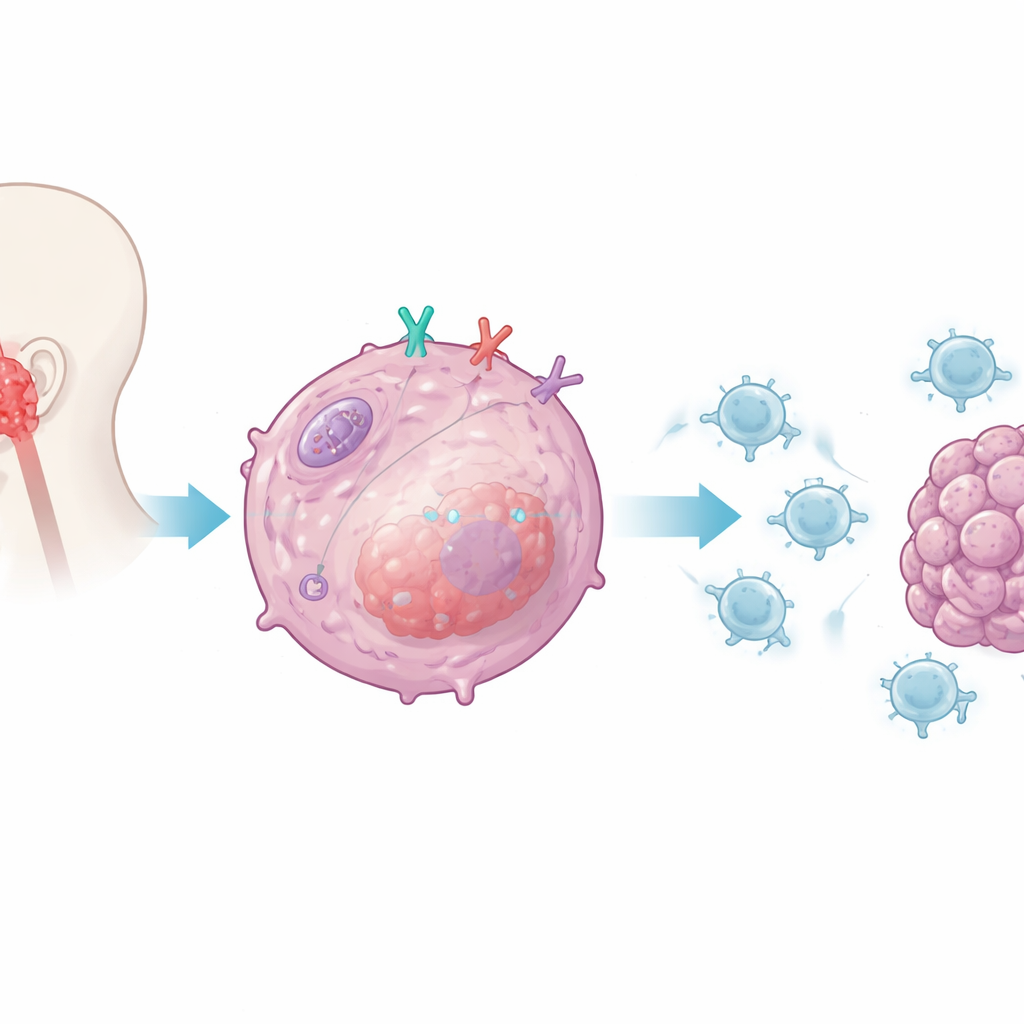
細胞内部の警報を沈める
次に研究チームはCD38がどのように抑制シグナルを送るかを調べました。焦点を当てたのは腫瘍細胞の自然免疫的警報系で、通常はウイルス様の核酸を検出してⅠ型インターフェロンを誘導し、強力な免疫刺激を行います。CD38欠損の腫瘍細胞では、インターフェロンβやCD8 T細胞を呼び込むケモカインが強く上昇しました。CD38は内部センサーRIG-Iとそのアダプタータンパク質MAVS(ミトコンドリア上に局在)で制御される経路を選択的に抑えることが示されました。CD38が存在するとこの経路と下流のシグナル伝達分子の活性化は抑えられ、CD38を除くとシグナル伝達とインターフェロン産生が急増して腫瘍の免疫可視性が高まりました。
CD38が重要なシグナルハブを破壊する仕組み
さらに掘り下げると、CD38はミトコンドリア上のMAVSと物理的に結合し、MAVSとRIG-Iの結合を妨げてシグナル伝達を弱めることがわかりました。さらに注目すべきは、CD38の高発現がMAVSタンパク質量を減少させる一方でMAVSの遺伝子発現を変えないことから、能動的な分解が起きていることを示唆します。各種阻害剤を用いた実験で、このMAVSの喪失はオートファジーと呼ばれる細胞のリサイクル機構、特にミトコンドリアを標的とする形(ミトファジー)に依存することが示されました。CD38はミトコンドリアの“自己貪食”のマーカーを増やし、いくつかのミトコンドリアタンパク質を減少させ、MAVSがオートファゴソーム構造に取り込まれて分解される過程を促進しました。ミトファジーを阻害するとMAVSは保持され、インターフェロンシグナルは回復したため、CD38はMAVSを廃棄経路へ導くことで警報を無効化していると結論づけられます。
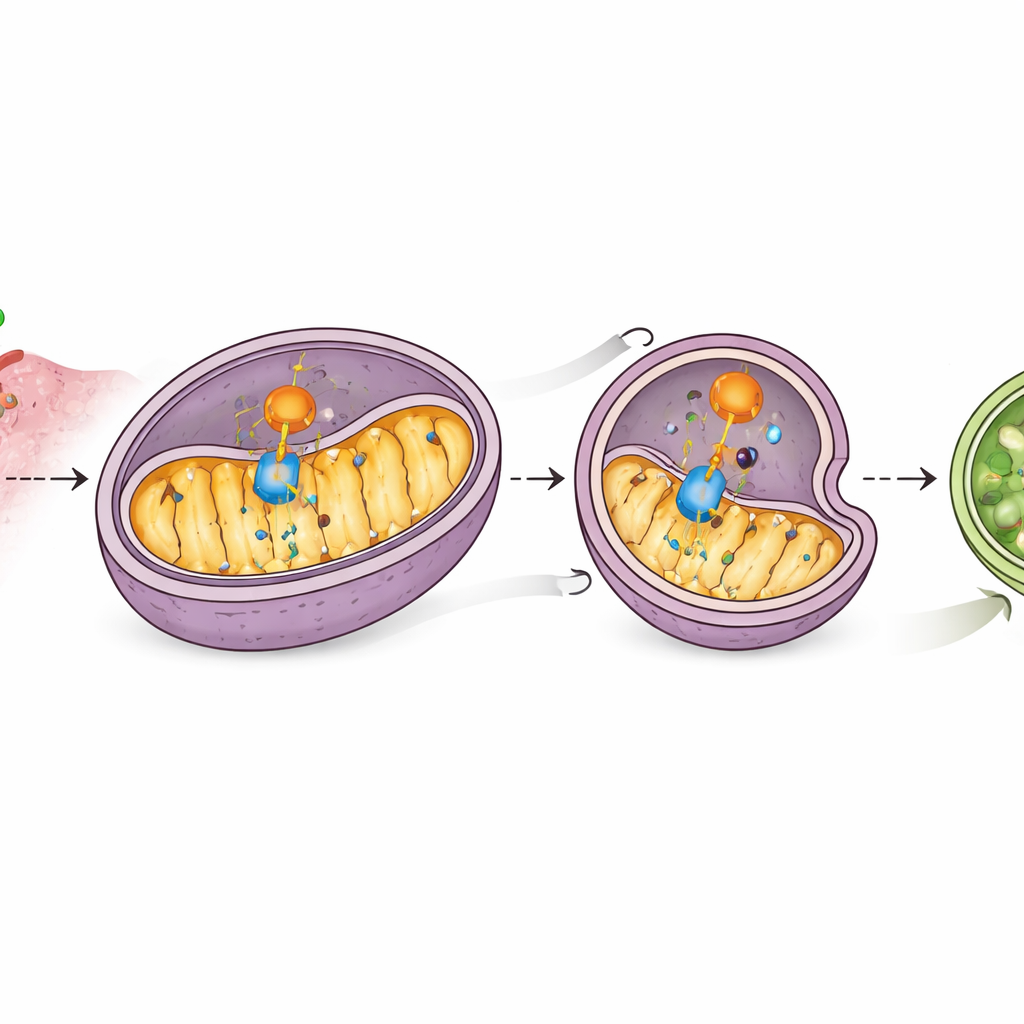
ミトコンドリアの自己破壊を導く補助因子
研究はさらに、内在性のミトコンドリア除去の受容体として働くPHB2というタンパク質を同定しました。質量分析と結合実験は、CD38がPHB2と相互作用し、PHB2のミトコンドリア局在を増強することを示しました。PHB2はコアのオートファジー機構を呼び込み、またMAVSにも結合します。CD38はこの結合を強めます。PHB2を減らすとCD38はもはや効果的にミトファジーを誘導できず、MAVS量は回復し、インターフェロン関連遺伝子の発現が再活性化しました。つまり一連の流れはこうです:CD38がPHB2に働きかけ、PHB2がMAVSに働きかけ、両者が協力してMAVSを分解へと導き、インターフェロン警報を沈黙させるのです。
動物モデルからの証拠
生体内での影響を検証するため、研究者らはCD38を欠くよう改変したマウス腫瘍を用いました。免疫能を持つマウスでは、これらの腫瘍は成長が遅く、CD8 T細胞がより多く浸潤し、抗腫瘍応答の指標であるインターフェロンγを産生する細胞の割合が高まりました。Ⅰ型インターフェロン受容体を遮断するとこの優位性は失われ、増強された免疫にはインターフェロンシグナルが不可欠であることが確認されました。ヒト化マウスに移植した鼻咽頭腫瘍でもCD38を減らすと同様に増殖が遅くなりCD8 T細胞浸潤が増えましたが、腫瘍細胞で同時にMAVSを低下させるとこの利益は消えました。これらの生体内データは、腫瘍細胞内のCD38–PHB2–MAVS軸がT細胞応答の強さを左右することを裏付けます。
将来の治療への示唆
総じて、本研究は鼻咽頭がん細胞内のCD38が抗腫瘍免疫の内部からの破壊者として働くことを示しています。CD38は選択的なミトコンドリアリサイクルを駆動してMAVSを枯渇させ、Ⅰ型インターフェロン産生を弱め、抗原提示を低下させ、最終的にCD8 T細胞の攻撃を鈍らせます。現在のCD38阻害薬は主に酵素活性を標的としており、タンパク質自体を除去したりMAVSを回復させたりはしません。著者らはCD38量を減らすか、CD38とPHB2やMAVSとの結合を阻害する新たな戦略が腫瘍内のインターフェロン警報を再活性化しうると論じています。既存のチェックポイント阻害剤と組み合わせれば、鼻咽頭がん――あるいは他のがんでも――免疫的に“コールド”な状態を“レスポンシブ”に変える可能性があるでしょう。
引用: Liang, L., Li, W., Liu, S. et al. CD38 degrades MAVS through mitophagy to inhibit type I interferon secretion in nasopharyngeal carcinoma cells and impairs CD8+T cell-mediated anti-tumor immunity. Nat Commun 17, 2544 (2026). https://doi.org/10.1038/s41467-026-69339-7
キーワード: 鼻咽頭がん, 腫瘍免疫療法, Ⅰ型インターフェロン, CD8 T細胞, ミトファジー