Clear Sky Science · ja
リン酸化プロテオミクスとキナーゼ–基質相互作用を用いたEGFシグナル経路推論のベンチマーク
研究室を超えて重要な理由
私たちの細胞は周囲からの信号を常に受け取り反応しています。その中でも表皮成長因子(EGF)は、細胞の増殖、分裂、生存を制御する上で非常に重要な信号です。この通信が壊れると、がんや他の病気の原因になります。本研究は一見単純だが重要な問いを投げかけます。現在の強力な測定技術と計算モデルを用いれば、教科書に載っている図よりもどれだけ正確にEGFシグナル経路を理解できるようになるのか、という点です。
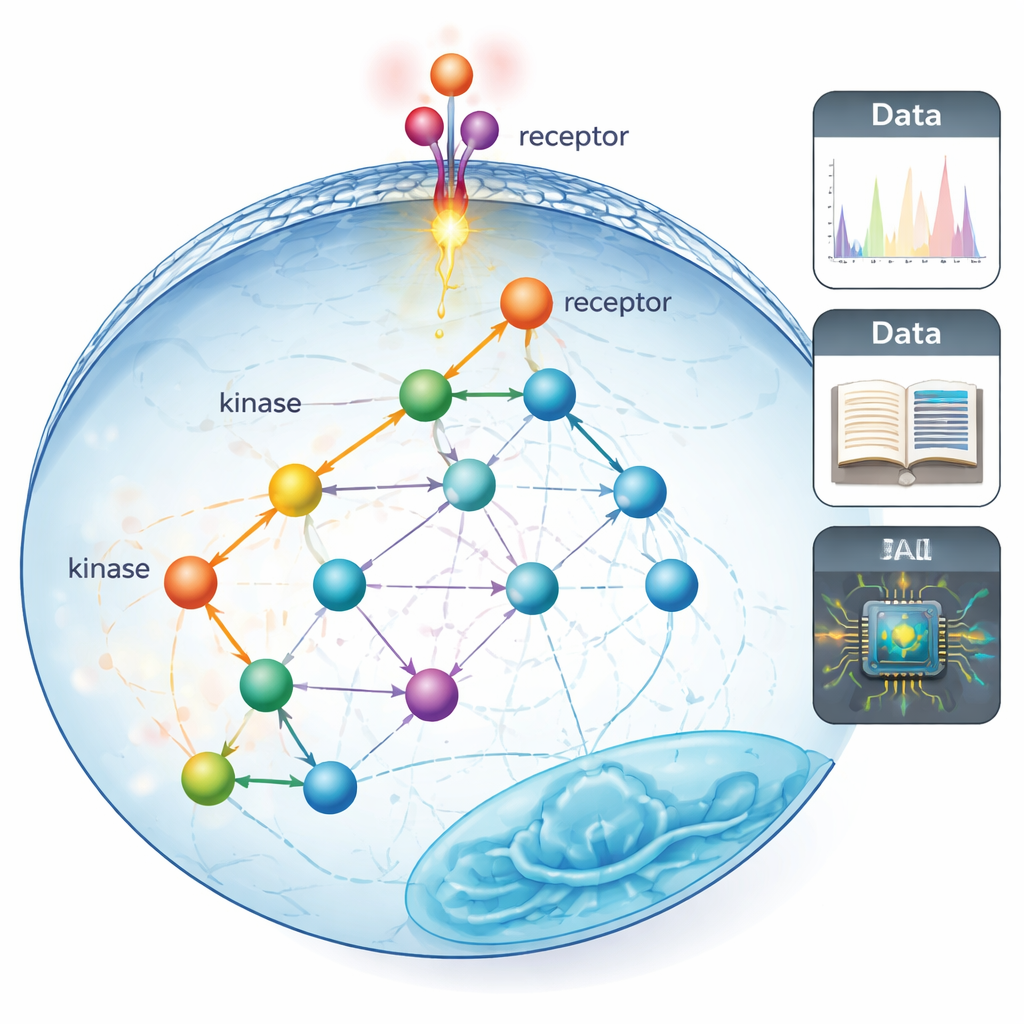
単純な直線図から現実の配線図へ
従来の「シグナル経路」は、しばしば細胞表面から核へメッセージを伝える整然としたほぼ直線的なタンパク質の連鎖として描かれます。これらの地図は、少数のタンパク質しか同時に観測できない遅いターゲット実験を数十年かけて積み重ねた結果です。著者らは、これにより街灯の下だけを照らすような偏った見方が残されていると主張します。すなわち、研究しやすかった少数のタンパク質については詳しく知っている一方で、実際の細胞に存在するであろうより広い結び付きについてははるかに少ない情報しか持っていない、ということです。
何千もの分子スイッチを同時に“傍受”する
その限定的な見方を越えるために、研究チームはリン酸化プロテオミクスを用いました。これは質量分析で一度の実験で何万ものタンパク質上のリン酸基という小さな化学タグを追跡できる手法です。これらのタグはキナーゼと呼ばれる酵素によって付けられ、シグナルの高速なオン/オフスイッチとして機能します。研究者らはまず、文献の精査結果、タンパク質配列を読み取る人工知能モデルの予測、キナーゼの嗜好性を調べた大規模実験スクリーニング、という三種類の情報を統合して、これまでで最も包括的な「誰が誰をリン酸化できるか」マップを構築しました。これにより、計測可能な部位の既知または推定されるキナーゼ–基質関係のカバー率は約5%から70〜80%にまで大幅に拡大しました。
多数の実験でEGF応答を耐性試験する
次に彼らは、肺・乳房・皮膚・脳のがんで重要な役割を果たす古典的経路であるEGF応答に注目しました。グループは、公開された三つの最先端データセットと、腎由来細胞で行った時間分解能の高い三つの新規深層測定、さらに異なる刺激で行った二つの対照研究を組み合わせました。これらの実験はそれぞれで4万以上のリン酸化部位を計測し、EGF刺激後の数分間でそれらが上昇・低下する様子を追跡しました。全体的なパターンは細胞型や技術ごとにやや異なりましたが、EGF経路の主要なリン酸化部位は繰り返し活性化され、コアのシグナルが多様な実験間でも頑強であることが確認されました。
キナーゼ間の隠れた会話を再構築する
どのキナーゼがより活性化または抑制されたかを推定した後、著者らはそれらの間でどのような「会話」が行われているか、すなわちどのキナーゼが他を活性化または影響する可能性が高いかを再構築しようとしました。彼らはキナーゼ–基質マップをキナーゼ–キナーゼネットワークに変換し、単純なランキング法からEGF受容体を根とする有向木構造に見えるよう結果を強制するより複雑なアプローチまで、三つの計算戦略を適用しました。得られた推定経路は、データベースから慎重にキュレーションされたEGFマップ、単一キナーゼを過剰発現した大規模実験、時間的に強く相関したキナーゼ部位のペア、といった複数の「基準真理」と比較されました。
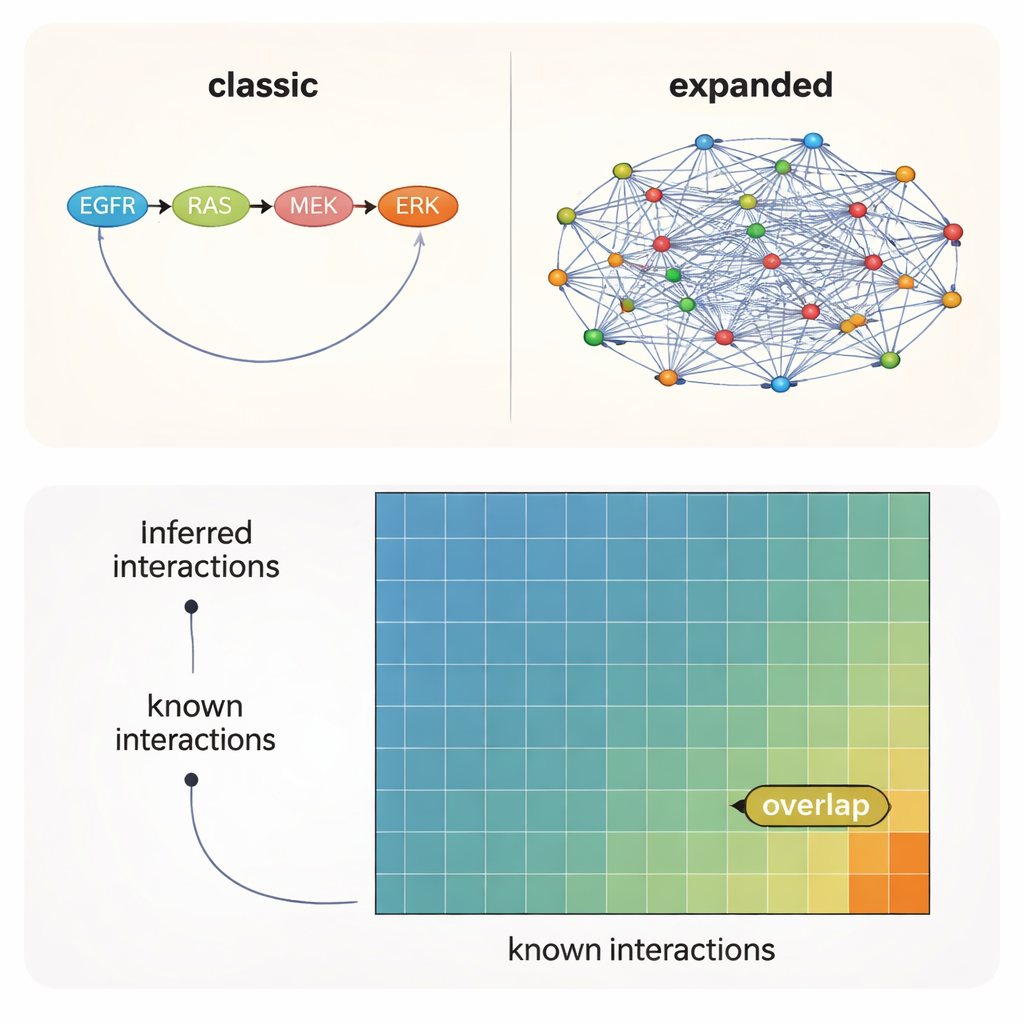
もっとも筋の通る結び付きの多くは公式地図にない
すべてのテストを通じて明確だったのは、アルゴリズムに与える出発ネットワーク、すなわち事前知識の選択が、特定の手法や実験コンテキストよりも結果に影響を与えたということです。文献に基づくネットワークは既知の相互作用の最大数を再現しましたが、より広範な予測資源はまだ正式に記述されていない多くの追加で妥当な結び付きを示しました。しかし最良の条件下でも、データとモデルが示唆する相互作用のうち参照セットに含まれているのは約10〜12%にすぎません。言い換えれば、支持されるキナーゼ–キナーゼ結び付きの約90%は未踏の領域に位置しています。
将来の治療への意味
専門外の読者への要点は、教科書に載っているよく知られたEGF経路図はおそらく氷山の一角に過ぎないということです。現代のリン酸化プロテオミクスと高度な計算手法を組み合わせると、はるかに豊かで複雑なシグナル伝達ネットワークが明らかになります。これらの新たに示唆された多くの結び付きは、がん細胞が薬剤を回避するために信号を迂回させる見落とされてきた手段や、より賢い薬物併用を設計するための新たな機会を表す可能性があります。本研究がすべての新規結び付きの実在を証明するわけではありませんが、研究者がこれらの仮説を検証するためのロードマップと公開ツールを提供しており、最終的にはEGFシグナルが中心的役割を果たす疾患に対するより精密で効果的な治療を目指すものです。
引用: Garrido-Rodriguez, M., Potel, C., Burtscher, M.L. et al. Benchmarking EGF signaling pathway inference using phosphoproteomics and kinase-substrate interactions. Nat Commun 17, 2071 (2026). https://doi.org/10.1038/s41467-026-69332-0
キーワード: EGFシグナル, リン酸化プロテオミクス, タンパク質キナーゼ, 細胞シグナル伝達ネットワーク, がん生物学