Clear Sky Science · ja
ヒストンのラクトリル化は膵臓がんにおける好中球浸潤と免疫回避のためにCXCL1発現を増加させる
このがん研究が重要な理由
膵臓がんは最も致死率の高いがんの一つであり、その一因は他の腫瘍で有効な最新の免疫療法に抵抗しやすい点にあります。本研究は、膵臓腫瘍が自身の糖代謝を書き換えて免疫系をひそかに無力化する仕組みを明らかにし、その過程を遮断することで体の防御—および既存の薬剤—が再び働く道を開ける可能性を示しています。
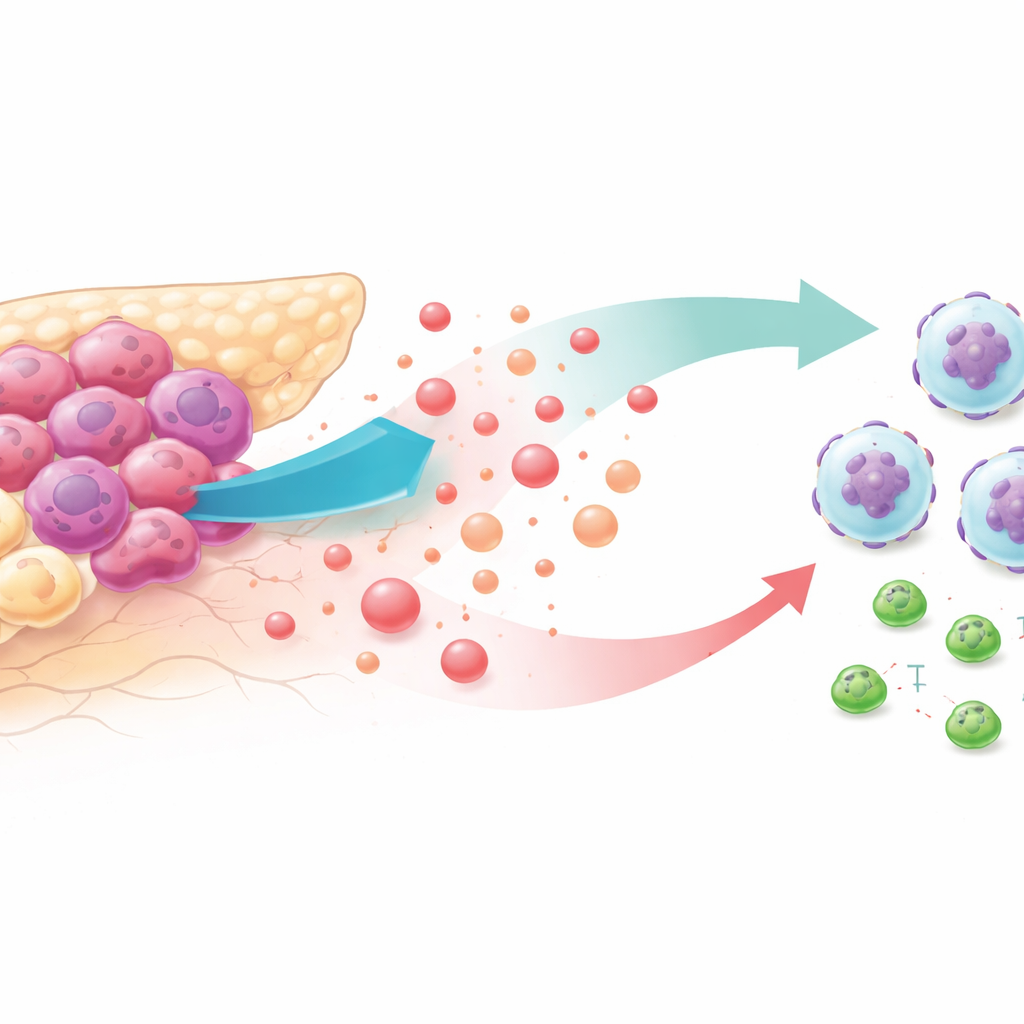
糖を貪る腫瘍と敵対的な近隣環境
がん細胞は酸素が十分にある場合でも激しくグルコースを消費することで知られています。この「高い解糖」ライフスタイルは、かつて代謝廃棄物と見なされた乳酸で腫瘍周辺環境を満たします。患者腫瘍データベースとマウスモデルの解析により、最も強い解糖を示す膵臓がんは好中球で溢れており(この文脈では腫瘍を助ける白血球)、がんを殺すCD8陽性T細胞は少ないことが分かりました。このようなプロファイルを持つ患者は生存期間が短くなる傾向があり、代謝の変化と免疫回避が密接に結びついていることが示唆されます。
腫瘍が乳酸を使って間違った援軍を呼ぶ仕組み
解糖がどのようにして好中球を引き寄せるかを理解するため、研究チームは膵臓がん細胞株とマウスで薬剤や遺伝学的手法により腫瘍の解糖を抑えました。糖分解が阻害されると、腫瘍細胞はCXCL1という化学シグナルの放出を大幅に減らし、マウスおよび患者サンプルの循環中のこのシグナル濃度も低下しました。培養条件の走化性実験では、高解糖性のがん細胞由来の培地に好中球が積極的に移動したのに対し、解糖を抑えた細胞由来の培地には移動しませんでした—研究者が純化したCXCL1を追加すると移動は回復しました。生体マウスでは、解糖を低下させた腫瘍にCXCL1を戻すと好中球数が回復し、解糖阻害による抗腫瘍効果が弱まることが確認されました。
乳酸が駆動する新しいエピジェネティック・スイッチ
研究はさらにDNAのパッキング(クロマチン)レベルに注目しました。遺伝子はヒストンと呼ばれる糸巻き状タンパク質の周りに巻かれており、ヒストンの化学的なタグが遺伝子のオン/オフを制御します。著者らは、膵臓がんでは解糖で生じた乳酸が特定のヒストン部位、H3K18に「ラクトリル」タグを付与することを示しました。この修飾、すなわちヒストンH3K18ラクトリル化は正常膵臓よりも腫瘍組織で著しく高かったのです。解糖が抑制されるとH3K18のラクトリル化は低下し、特にCXCL1遺伝子の制御領域近傍で顕著に減少し、CXCL1産生も落ちました。乳酸を再添加すると、ヒストンのタグとCXCL1発現は回復しました。患者サンプルを横断的に見ると、H3K18ラクトリル化が多い腫瘍はCXCL1も高く、分子マーカーとプロ腫瘍的な免疫景観が結びついています。
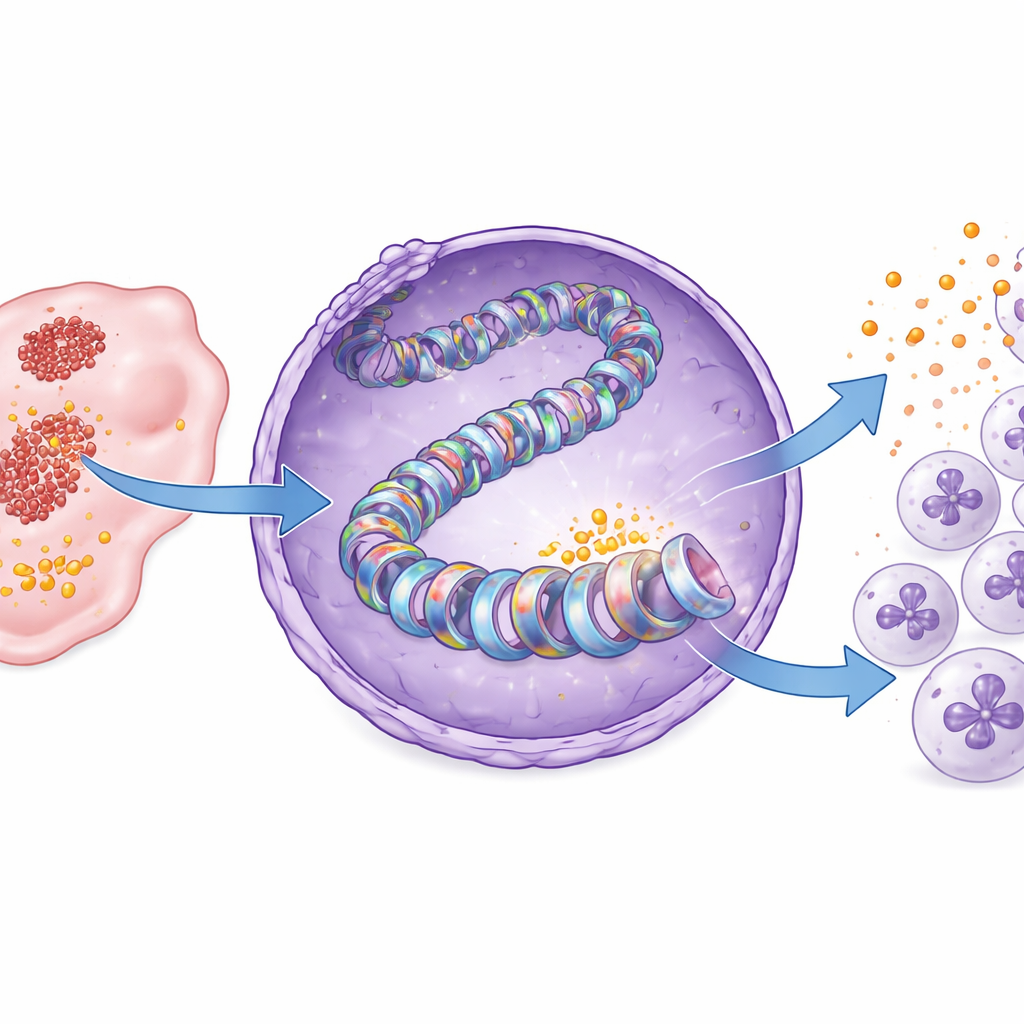
この酵素の同定と薬で狙える弱点
ヒストンのタグは専門の酵素によって書き込まれます。既知のヒストン修飾酵素の阻害剤をスクリーニングすることで、研究者らはPCAFと呼ばれる酵素を膵臓がんにおけるH3K18ラクトリル化の主要なライターとして特定しました。構造モデルはPCAFがラクト酸の活性化型であるラクトイル-CoAを結合できることを示唆し、生化学的アッセイは精製したPCAFが直接ヒストンH3にラクトリル基を付加できることを確認しました。小分子ブロモスポリンでPCAFを阻害すると、がん細胞およびマウス腫瘍でH3K18ラクトリル化とCXCL1産生が低下しました。その結果、腫瘍への好中球浸潤は減り、CD8陽性T細胞は増加し、腫瘍成長は抑制されました。マウスに明らかな体重減少や毒性は認められませんでした。
併用療法で“冷たい”腫瘍を“熱く”する
抗PD-1抗体などの標準的な免疫チェックポイント阻害薬は膵臓がんで効果が限定的であるため、チームは乳酸–PCAF–CXCL1経路の解体がこれらの腫瘍をより反応しやすくするかを試しました。皮下および膵臓原発マウスモデルの双方で、ブロモスポリンと抗PD-1療法の併用は単独治療よりも腫瘍をより縮小させ、好中球浸潤を減らし、活性化したCD8陽性T細胞を増やし、生存を有意に延長しました。これは、腫瘍の好中球を呼ぶ代謝的“サイレン”を断つことが、免疫学的に“冷たい”腫瘍をチェックポイント療法がより働きかけやすい“より熱い”状態に変える手助けをすることを示唆します。
今後の治療に向けての意義
平たく言えば、本研究は一連の連鎖反応を明らかにしました:膵臓腫瘍は糖を燃やし、乳酸を放出し、その乳酸を使ってDNAを包むタンパク質にエピジェネティックなスイッチを入れ、CXCL1を増やし、その結果キラーT細胞から身を隠すのを助ける好中球を招きます。PCAF段階でこの連鎖を薬で断つことは、腫瘍の成長を遅らせるだけでなく、マウスでは既存の免疫療法の効果を高めました。安全性の評価や人で標的化する最良の方法を見つけるためのさらなる研究は必要ですが、これらの発見は有望な戦略を示しています:腫瘍の代謝と遺伝子スイッチを再プログラムして免疫系に戦う機会を与えることです。
引用: Zhang, P., Ma, J., Wan, Y. et al. Histone lactylation increases CXCL1 expression for neutrophil infiltration and immune escape in pancreatic cancer. Nat Commun 17, 2526 (2026). https://doi.org/10.1038/s41467-026-69311-5
キーワード: 膵臓がん, 腫瘍代謝, ヒストンのラクトリル化, 腫瘍微小環境, がん免疫療法