Clear Sky Science · ja
解釈可能で生成的な深層学習モデルが相分離する本質的に変性したモチーフを解明する
なぜ小さなタンパク質断片が重要なのか
私たちの細胞内では、重要な分子がしばしば液滴状の塊、いわゆる生体分子コンデンセートとして集まります。これらの液滴は膜という壁を使わずに化学反応を整理し、遺伝子のオン/オフ、シグナル伝達、細胞のストレス応答などを形作ります。多くのこうした液滴は、本質的に変性した領域として知られる折りたためないタンパク質の柔らかい領域によって形成されます。しかし、生物学者はどの短い配列断片が実際に液滴形成を駆動するのかを特定するのに苦労しています。本研究は、これらの重要な断片を検出し新たに設計することのできる深層学習フレームワーク、PhaSeMotifを紹介し、細胞内の液滴を調べ書き換える強力な手段を研究者に提供します。
乱雑なタンパク質末端から検証可能な仮説へ
多くのタンパク質は特定の形に折り畳まらない長く柔軟な末端を持ちます。これらの変性領域は特定のアミノ酸に富み、繰り返しパターンや短いモチーフを含むことが多いです。近年の研究は、このようなモチーフが多数の弱い相互作用を同時に可能にすることで凝縮を促進することを示しています。しかし、プロテオーム全体を走査してどの短い伸びが重要か、そしてその理由を明らかにすることは大きなボトルネックでした。既存の計算ツールは通常、全タンパク質や大きな領域にスコアを与えるだけで、どこを変異させるべきか、実験で何を検証すべきかの具体的な指針をほとんど提供しません。著者らは、変性領域が液滴を作るかどうかを予測するだけでなく、どの正確な部分配列が主要な役割を果たしているかも示すモデルを構築することを目指しました。
液滴駆動モチーフの深層学習マップ
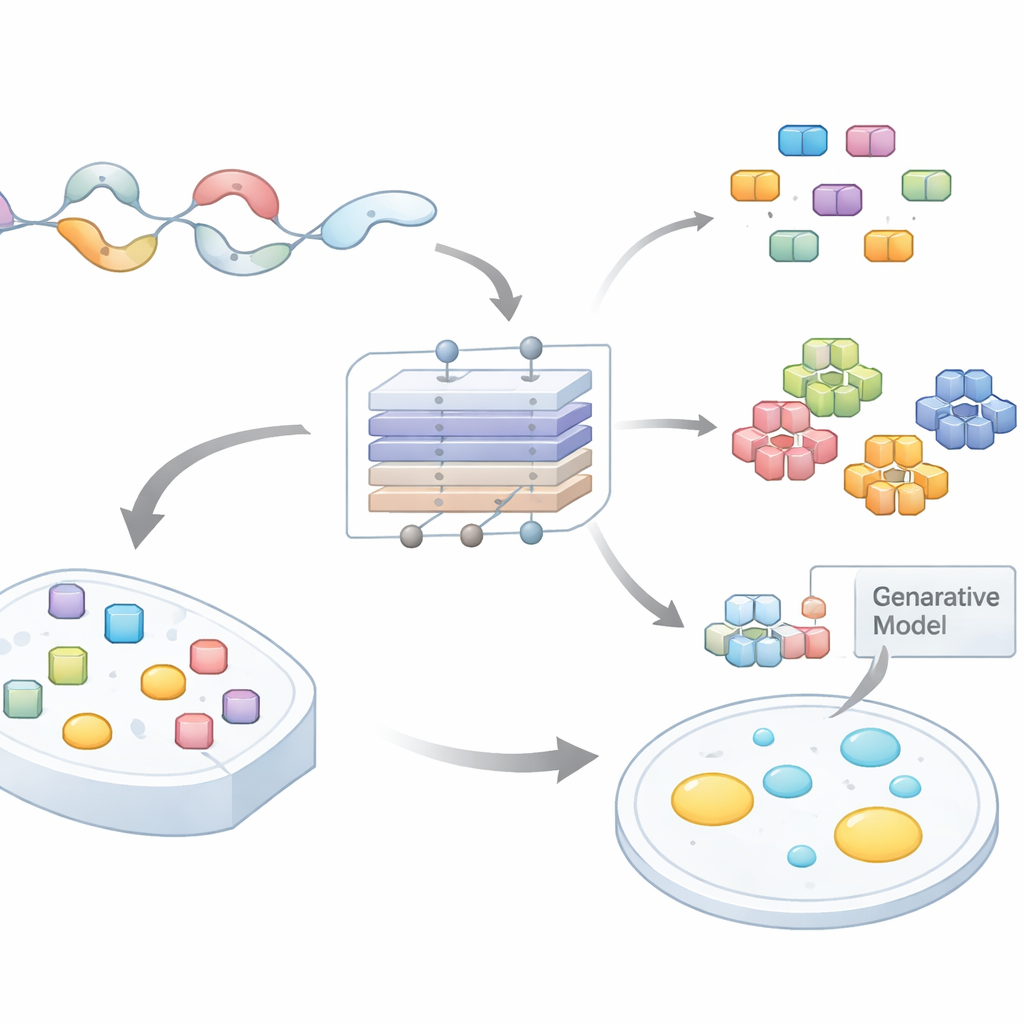
研究チームは複数の種にわたる変性領域の大規模データセットを集め、宿主タンパク質が相分離しやすいかどうかに応じてラベル付けしました。次に、配列の長さにかかわらずアミノ酸配列を入力として液滴形成スコアを出力する注意機構ベースのニューラルネットワーク、PhaSeMotifを訓練しました。重要なのは、ネットワークが畳み込み層と注意機構を組み合わせて、配列の短いウィンドウがスコアにどの程度寄与しているかを評価する点です。モデルをトレースバックすることで(ガイド付き逆伝播に似た手法を用いて)、著者らはモデルが液滴形成に不可欠とみなした重要度の高い短いパッチ—通常20残基未満のモチーフ—を抽出しました。
生細胞での予測の検証
これらのモチーフが本当に重要かどうかを確かめるために、研究者らはヒト細胞の光活性化システムを用いました。彼らは予測された液滴形成性変性領域を光感受性のオリゴマー化モジュールと蛍光タグに融合しました。青色光下でこれらの構築体は急速に明るい点として凝縮し、相分離をリアルタイムで報告しました。続いて、チームは個々のモチーフを同長の中性で柔軟なリンカーに置換して外科的に除去しました。テストした17配列のうち82%で、液滴形成は著しく弱まるか完全に消失し、PhaSeMotif領域外の対照的な変異はしばしばほとんど影響を与えませんでした。重要なのは、多くの重要モチーフが病気関連変異が凝縮を乱すことで知られている部位と重なっており、その生物学的意義を裏付けている点です。
モチーフタイプの語彙を明らかにする
17,000以上のモチーフを得た著者らは、次に液滴駆動断片に共通する「傾向」があるかどうかを調べました。彼らはアミノ酸組成と配列パターンを解析し、モチーフを9つのクラスターに分類しました。あるクラスターは芳香族残基とグリシンに富み、疎着性のπ–πやカチオン–π相互作用と整合します。別のクラスターは正負の電荷が分離したパッチを含み、静電的引力や特定のコンデンセートへの選択的な分配を促します。さらに、プロリンとグリシンが支配的で柔軟性を支持するクラスターや、密な水素結合ネットワークを形成しうるグルタミンの長い連続領域に特徴づけられるクラスターもありました。細胞区画やコンデンセートの種類ごとにこれらのモチーフクラスの特性ある混合が見られ、モチーフの組成がどこでどの相手とタンパク質が凝縮するかを決めるのに寄与していることを示唆します。
ルールを証明するための新規モチーフ設計
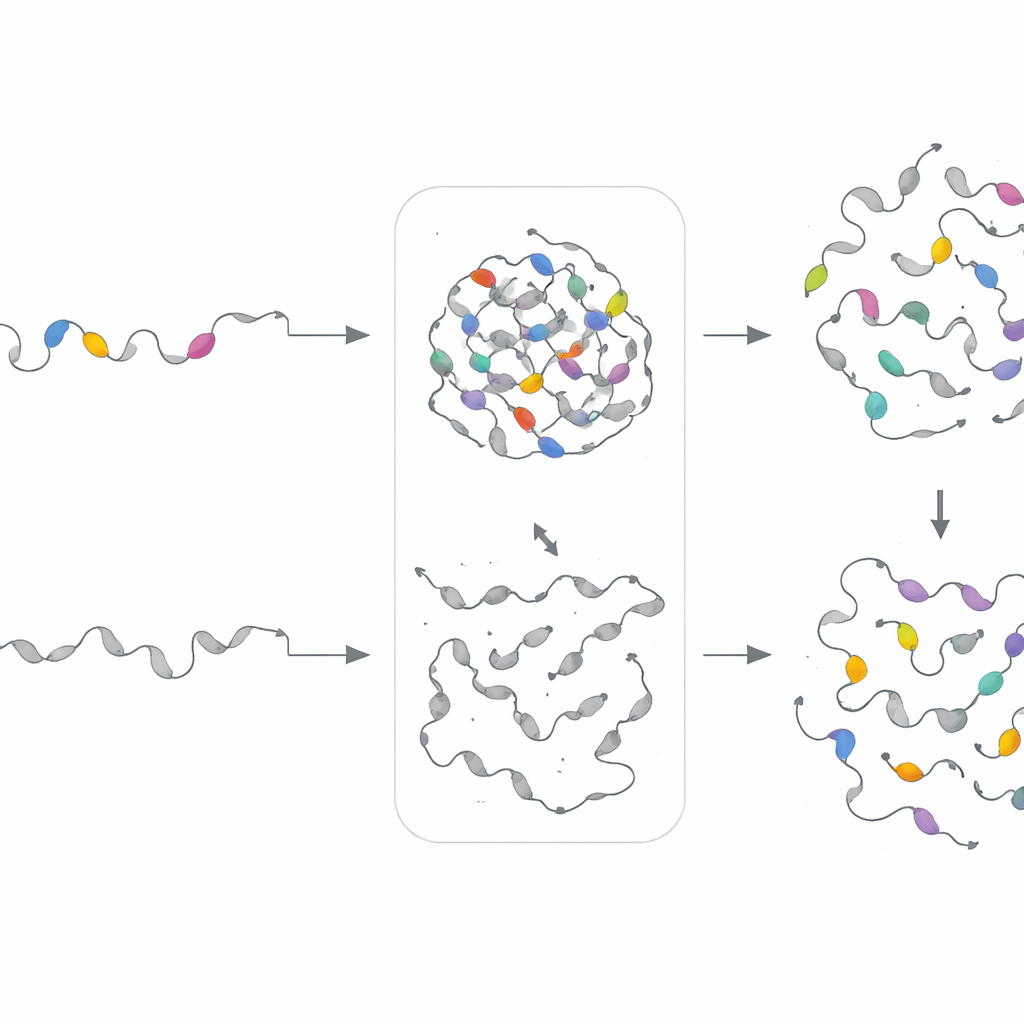
モチーフの「レシピ」――正確な配列ではなくその統計的特徴が液滴の振る舞いを支配するかを検証するために、チームは各モチーフクラスターごとに個別の生成モデルを構築しました。これらの変分オートエンコーダは特定クラスターの統計パターンを学習し、同じ組成的指紋を共有しながら配列の並びは異なる新しい人工配列を生成しました。研究者らはこれらの合成モチーフを、元の断片を削除したタンパク質に実験的に挿入しました。驚くべきことに、21例中18例で設計したモチーフが細胞内で相分離を回復し、時には液滴形成の速度や濃度を調節することさえありました。これはPhaSeMotifが再利用可能な基礎的設計規則を捉え、液滴形成領域を構築・修復できることを示しています。
生物学と疾患にとっての意義
解釈可能な深層学習と生成的設計、直接的な細胞実験を結びつけることで、本研究は「変性した液滴形成領域」という漠然とした概念を、短く組み合わせ可能なモチーフの具体的な集合へと変えます。非専門家への要点は、科学者が細胞内液滴の組み立て、混合、異常を制御する小さなタンパク質断片を読み書きできるようになったということです。これにより、これらの断片における疾患原因変異の迅速な発見、コンデンセートが細胞生理をどう組織するかの明確な機構研究、さらには治療や合成生物学の応用のために液滴を制御するタンパク質を合理的に設計する道が開かれます。
引用: Yang, H., You, K., Ma, L. et al. Interpretable and generative deep learning models explicate phase separating intrinsically disordered motifs. Nat Commun 17, 2571 (2026). https://doi.org/10.1038/s41467-026-69252-z
キーワード: 生体分子コンデンセート, 本質的に変性したタンパク質, 相分離, 深層学習, タンパク質モチーフ