Clear Sky Science · ja
相分離と線維化の切り離しが生体分子濃縮体の機能を保持する
脳の健康にとってなぜ重要か
アルツハイマー病を含む多くの脳疾患では、タンパク質が時間とともに硬く繊維状に絡み合うことが関与します。同じタンパク質は、細胞内で柔らかい液滴状の構造を作り、化学反応を整理する小さな液体作業場のように働くこともあります。本研究は重要な問いを投げかけます:これらの液滴が有害な線維に硬化するのを防ぎつつ、有用な日常的機能を壊さずに済むのか?著者らは、アミノ酸である一般的な細胞代謝物L-アルギニンが、アルツハイマーに関連する主要なタンパク質Tauに対してまさにそれを可能にすることを示しています。
遊離タンパク質から小さな液滴へ
細胞内では、特定のタンパク質が常に流体状の内部に均一に混ざったままでいるわけではありません。代わりに、それらは生体分子濃縮体と呼ばれる液滴に集まり、非常に柔らかいゲルや粘性の高い液体のように振る舞います。研究チームは、通常は微小管を構築・安定化する働きのあるタンパク質Tauに注目しました—微小管は神経細胞内の道路のように機能する中空のフィラメントです。Tauはまた、神経変性疾患で見られるもつれの中に存在する剛直なアミロイド線維を形成することで悪名高いです。Tau液滴が時間とともにどのように変化するかを研究するために、研究者たちはSynTag‑Tauと名付けた改変版を作り出しました。これは実験に適した時間スケールで活性な濃縮体を形成し、添加剤を多用せずにアミロイド線維へと老化します。
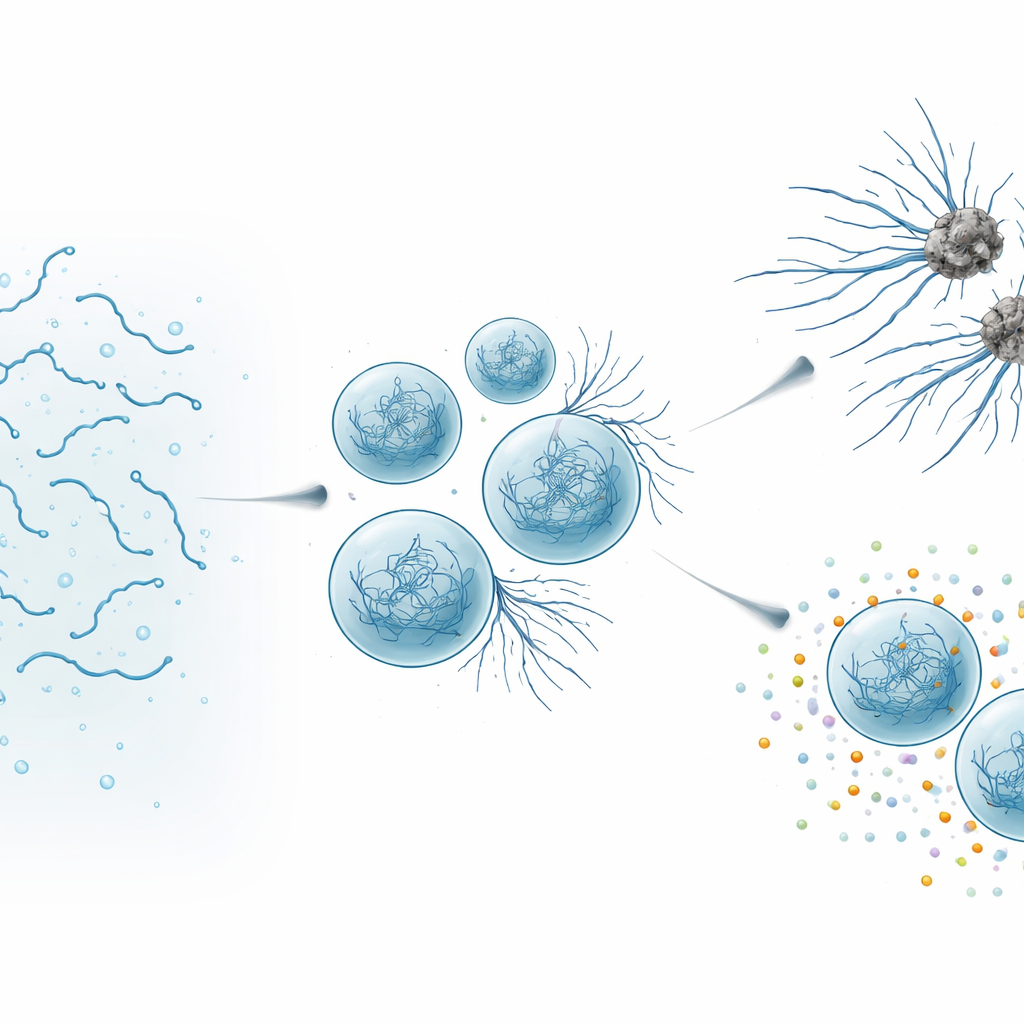
役立つ液滴が有害になるとき
高解像度顕微鏡と物理生物学的測定を用いて、著者らはSynTag‑Tau液滴が数時間でどのように変化するかを観察しました。新しい液滴は液体のように振る舞い:容易に融合し、分子は速やかに動き、秩序だった構造の兆候はありませんでした。時間が経つにつれて液滴は動きが鈍くなり硬化し、薄い繊維が表面から周囲の溶液に向かって伸び始めました。感度の高い光学的手法は、これらの繊維がアミロイドに特徴的な密に詰まった“クロスβ”構造を含んでいることを示しました。重要なのは、濃縮体の界面―濃密な液滴と周囲の流体との境界―が線維が最初に現れるホットスポットとして働いたことです。液滴が老化しさらに繊維を伸ばすにつれて、Tauの本来の働きは損なわれました:濃縮体は微小管の構成要素であるチューブリンを引き寄せる能力が低下し、最終的には微小管の組み立てを支える能力を完全に失いました。
バランスを傾ける小分子
研究者らは次に、単純な代謝物が液体から線維への移行を遅らせたり防いだりできるか、しかし液滴自体は維持できるかを問いかけました。いくつかの天然に存在する小分子をスクリーニングしたところ、正に帯電したアミノ酸であるL-アルギニンとL-リジンが、SynTag‑Tau液滴からのアミロイド線維形成を強く遅らせるか阻止した一方で、現実的な低ミリモル濃度では液滴形成を止めませんでした。対照的に、グルタミン酸やアスパラギン酸などの負に帯電したアミノ酸は線維形成を促進し、一般的なタンパク質を撹乱する化学物質は役立たなかったか液滴自体を乱しました。L-アルギニンの蛍光類似体は、この分子が外側よりもTau濃縮体の内部に好んで存在することを示し、必要な場所で作用していることを示唆しました。
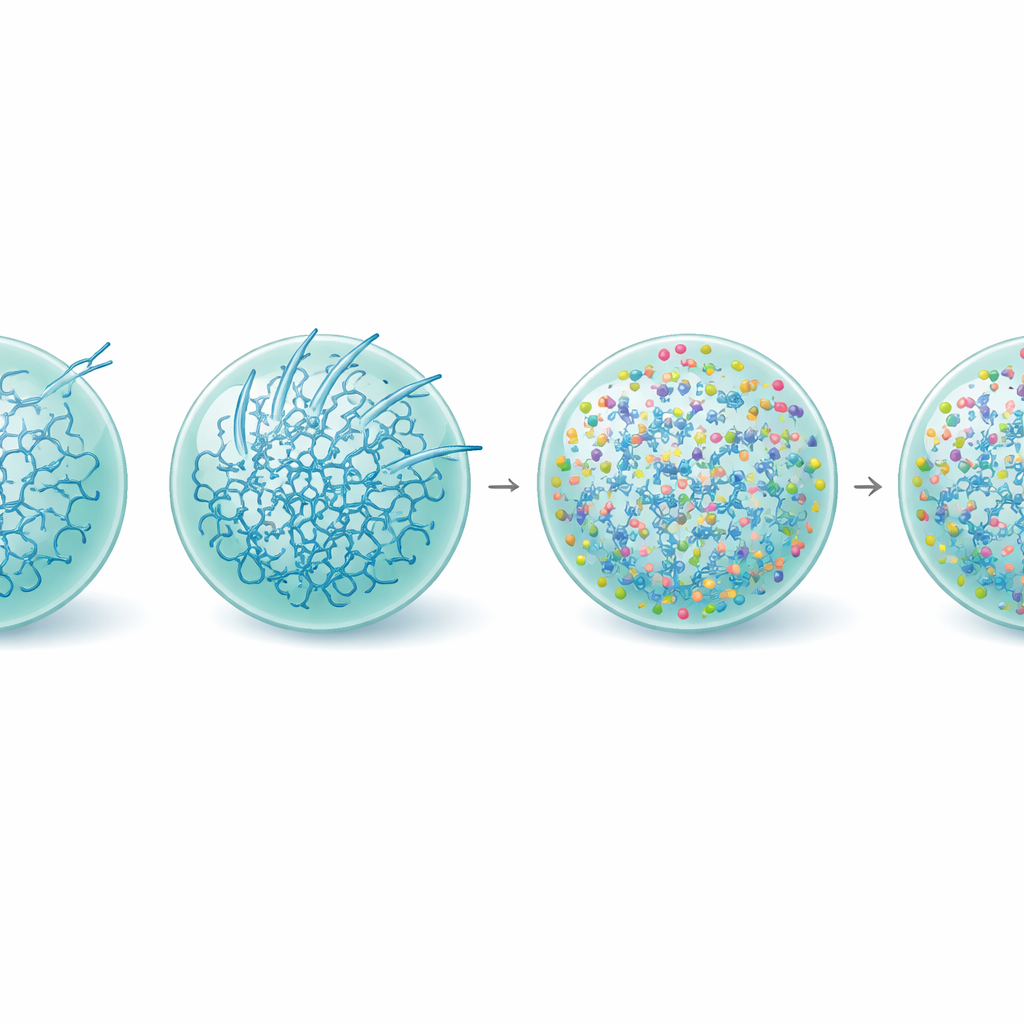
液滴の硬化を抑え、機能を守る
さらに掘り下げると、チームはL-アルギニンがTau液滴の内部にどのように作用するかを調べました。タンパク質構造の測定では、L-アルギニン存在下では、古くなった液滴においてもアミロイドに関連する剛直なβ豊富な形をとるTau分子の割合が減少していることが示されました。動画ベースのナノレオロジー—濃縮体内部の微小ビーズの動きを追跡する手法—は、L-アルギニンがTau液滴を実際にはより粘弾性にすることを明らかにしました。つまり、内部ネットワークがより強く相互連結する一方で流体状の性質を保ちます。この強化は系を準安定で機能的な状態に保ち、特に液滴表面での線維形成に対するエネルギー障壁を高めるようです。これと一致して、L-アルギニン処理された濃縮体は、処理していない液滴が不活性化した時点でも均一にチューブリンを集め続け、微小管成長を支えました。
今後の治療法にとっての意味
この研究は、タンパク質の液滴形成を駆動する力と有害な線維形成を駆動する力は関連しているが、切り離し可能であることを示しています。L-アルギニンのような代謝物で濃縮体内部の化学環境を調整することで、有益な液状状態を保持しつつ、病態に結びつくアミロイド線維への移行を遅らせたり防いだりすることが可能です。本研究はin vitroで特別に設計されたTau系を用いていますが、一つの原理的証明を提供します:濃縮体の安定性を選択的に強化する小分子は、将来的に生体分子濃縮体の通常の組織化機能を阻害することなく、細胞を有毒なタンパク質凝集の徐々の蓄積から守る手助けをする可能性があります。
引用: Mahendran, T.S., Singh, A., Srinivasan, S. et al. Decoupling phase separation and fibrillization preserves activity of biomolecular condensates. Nat Commun 17, 2841 (2026). https://doi.org/10.1038/s41467-026-69244-z
キーワード: Tauタンパク質, 生体分子濃縮体, アミロイド線維, L-アルギニン, 神経変性