Clear Sky Science · ja
スクレロスチン欠損はマウスの白色脂肪を褐色化刺激に敏感にしてビージングを誘導する
脂肪を温めれば病気を冷ます理由
私たちは骨と体脂肪を別々の世界と考えがちだ:ひとつは体の構造を支え、もうひとつはエネルギーを貯蔵する。このマウス研究は、骨と脂肪が常に化学的に対話しており、骨細胞がつくるタンパク質が「白色」脂肪をただのカロリー貯蔵庫にしておくか、より活動的でカロリーを燃やす「ベージュ」脂肪に変えるかを左右しうることを明らかにしている。この隠れた対話を理解することで、肥満、糖尿病、骨減少を同時に扱う新しい手法が開ける可能性がある。
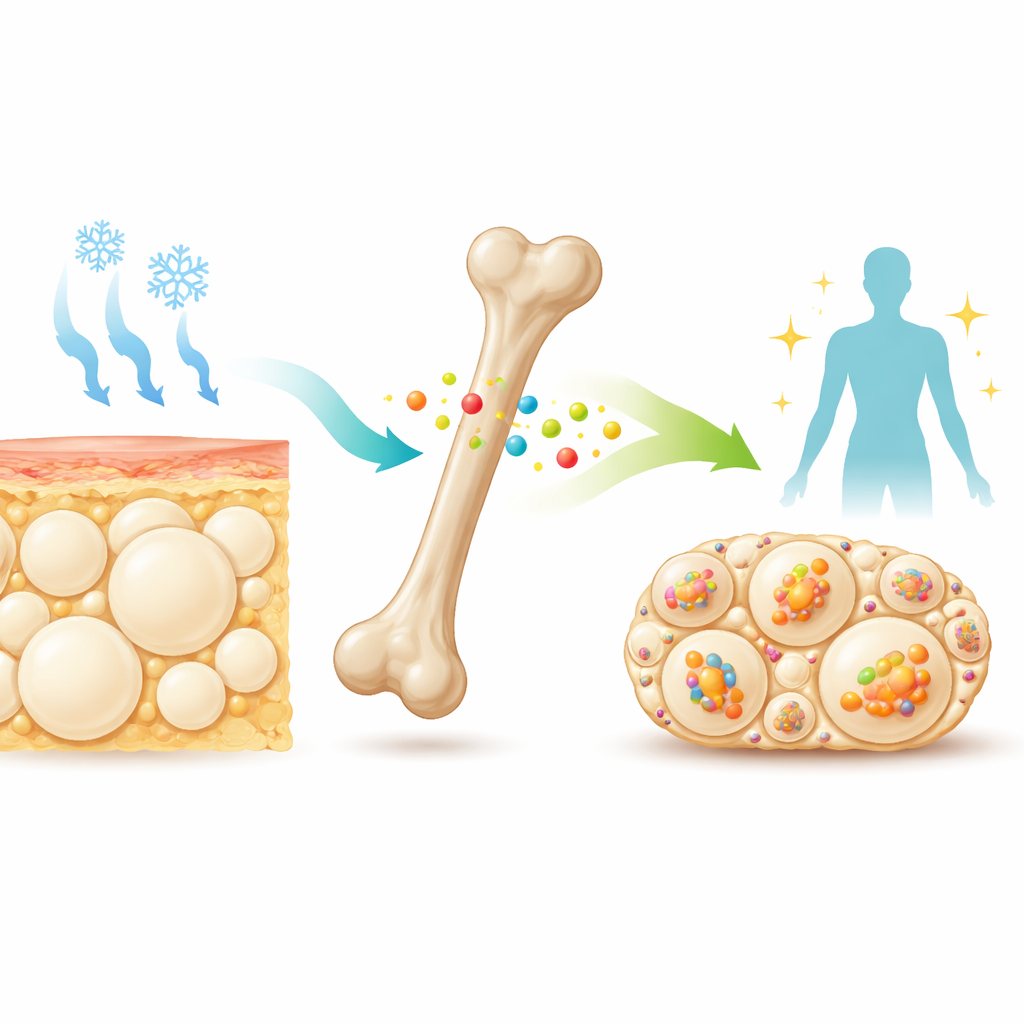
骨からの静かな伝達因子
骨の深部では、特殊な細胞がスクレロスチンという小さなタンパク質を血流へ放出している。臨床では骨折リスクのある患者で骨を強くするためにスクレロスチンを標的にする薬が用いられている。以前の研究は、スクレロスチンを欠くマウスが骨が非常に丈夫なだけでなく、よりやせ形でインスリン感受性が高いことを示していた。これらのマウスの皮下脂肪、特に股の周り(鼠径部白色脂肪)には、多数のコンパートメントを持ち「ベージュ」脂肪に似た小型の脂肪細胞が含まれ、燃料を燃やして熱を作る能力がある。これらの手がかりから研究者たちは、冷感や神経信号を模倣する薬剤にさらされたときに白色脂肪をベージュへ変える能力に対し、スクレロスチンが通常ブレーキとして働いているかを問い始めた。
冷刺激、骨の信号、そして脂肪の点火
研究チームは、正常マウスとスクレロスチン遺伝子欠損マウス(Sost-/-)に対し、特定の脂肪細胞受容体(β3アドレナリン受容体)を活性化する薬剤あるいは軽度の寒冷を与えた。正常な動物では、これらの熱産生刺激が骨におけるスクレロスチン産生を増加させ、血中濃度を上げた。この上昇は海綿骨の減少と関連したが、皮下脂肪への変化は控えめだった。対照的に、スクレロスチン欠損マウスははるかに強い反応を示した:その鼠径部脂肪はより多くのグルコースを取り込み、より多くの脂肪酸を放出し、細胞サイズが縮小し、ミトコンドリアで満たされたベージュ様の細胞で充満した。主要な熱産生遺伝子はこれらのマウスでより強くオンになり、とくに皮下脂肪で顕著だった一方で、古典的な褐色脂肪は大きくは変わらなかった。
共有のスイッチで脂肪燃焼を微調整する
スクレロスチンがどのようにこの制御を行うかを理解するため、研究者たちはスクレロスチンが骨で通常抑制するWntシグナル経路に関与するタンパク質、β-カテニンに着目した。出生後に脂肪でβ-カテニンを活性化すると白色細胞はベージュ様の状態へ向かい、β3アドレナリン信号への応答が高まったが、この効果は体が余分な熱を必要としない暖かい等温環境(サーモニュートラル)に飼育すると消失した。逆に、スクレロスチン欠損マウスの脂肪細胞でβ-カテニンを特異的に欠失させるとベージュ脂肪が消え、より大きな白色脂肪細胞が回復し、インスリンや脂肪酸の改善も逆転した。これらの実験は、スクレロスチンが低いときに脂肪細胞内のβ-カテニンが白色脂肪を熱産生刺激により敏感にする重要な内部のレバーになることを示唆している。
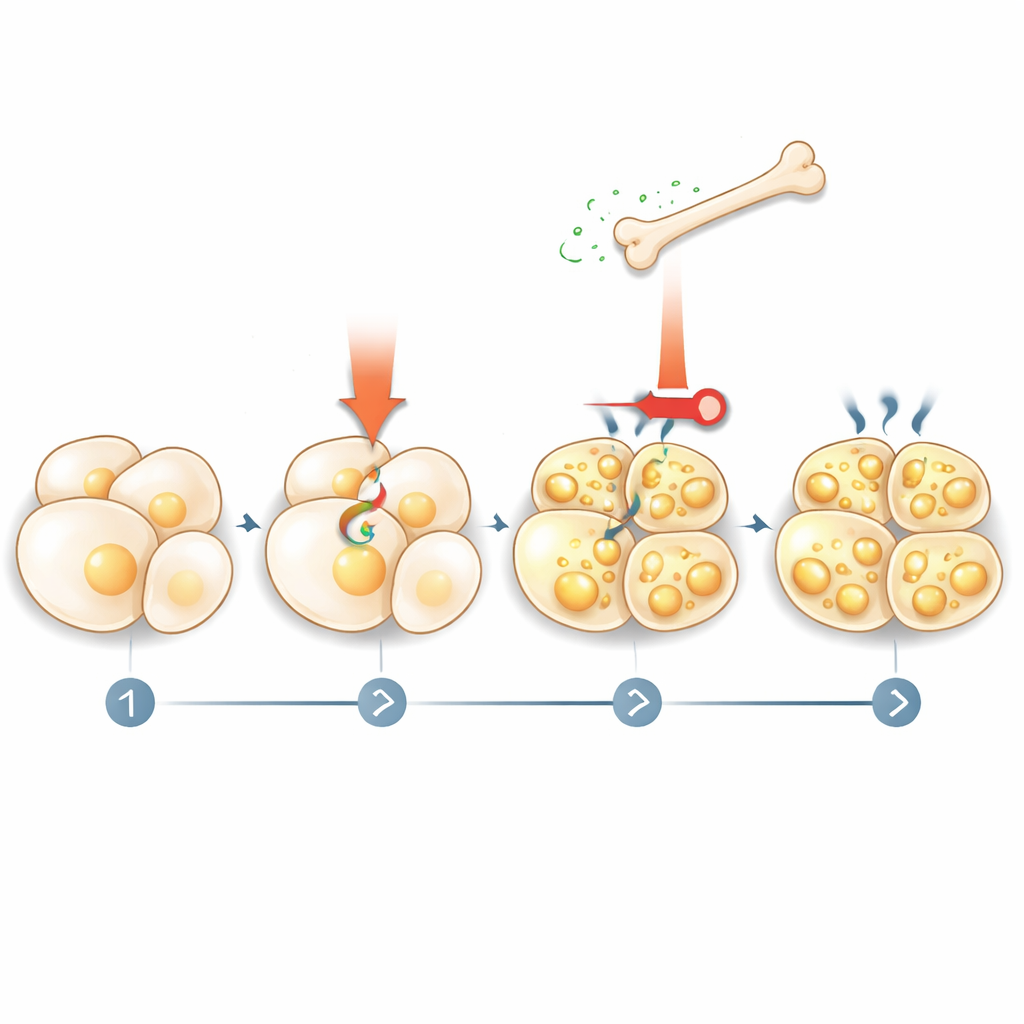
脂肪が骨に応答する仕組み
話は骨が脂肪に命令するだけでは終わらなかった。チームは、熱産生刺激が脂肪分解(リポリシス)を活性化し、脂肪酸を血中に放出することを見出した。これらの脂肪酸は核内受容体PPARγを介して骨細胞に作用し、スクレロスチン産生を増強する。研究者らが脂肪細胞でのリポリシスを阻害するか骨細胞からPPARγを除去すると、寒冷模倣薬はもはやスクレロスチンレベルを上げられなかった。これはフィードバックループを明らかにする:熱産生信号が脂肪に燃料を放出させ、その燃料が骨にスクレロスチンを分泌させ、スクレロスチンがさらに脂肪の活性化とベージングを抑えるという循環である。
代謝健康のために骨と脂肪の薬を組み合わせる
最後に、研究者たちはこのループを断ち切ることが病態類似の状況で役立つかどうかを試した。高脂肪食で肥満になったマウスに、膀胱障害で既に用いられるβ3アドレナリン薬ミラベグロンの低用量、スクレロスチンを中和する抗体(ロモソズマブ、骨粗鬆症に承認)あるいはその両方を投与した。どちらか一方の薬剤だけでは効果は控えめだったが、併用すると主要な脂肪貯留部位の脂肪量が減少し、より小さく活動的な細胞へのシフトが起き、インスリン、トリグリセリド、コレステロールが低下し、骨の強度は保たれた。体が熱をあまり必要としない温かい飼育環境では、スクレロスチン欠損による代謝上の利点はほとんど消失し、この経路が熱産生シグナルが存在するときに最も重要であることを強調した。
将来の治療への意義
平たく言えば、本研究は骨が単なる受動的な足場ではなく、脂肪細胞がどれだけエネルギーを燃やすかを能動的に調整する器官であることを示している。スクレロスチンは熱産生活動を抑えるボリュームノブのように働き、燃料消費を抑制している。そのノブを遺伝や薬で下げると、体が寒さや特定の薬で刺激されるときに特定の白色脂肪貯蔵が熱を産生するモードに切り替わりやすくなる。マウスでは同じ介入が骨を強くし代謝健康を改善するため、慎重に設計された骨・脂肪両方を標的とする治療の組合せは、いずれ肥満、糖尿病、骨粗鬆症を個別にではなく同時に治療する助けになるかもしれない。
引用: Choquette, G.M., Kim, S.P., Wilkinson, K.J. et al. Sclerostin deficiency sensitizes white adipocytes to thermogenic signals that induce beiging in mice. Nat Commun 17, 2394 (2026). https://doi.org/10.1038/s41467-026-69227-0
キーワード: スクレロスチン, ベージュ脂肪, 骨と脂肪のクロストーク, 熱産生, 代謝疾患