Clear Sky Science · ja
セプチンに結合するPIPKIγアイソフォームによる局所的なPI(4,5)P2合成が細胞質分裂中の中央紡錘体複合体のミッドボディ結合を制御する
細胞が二つに分かれる最終段階
細胞質分裂――一つの細胞が二つに分かれる最後の締め付け――は当然のことのように見えますが、これがうまくいかないとがんや他の疾患の一因になります。本研究は、生まれたばかりの二つの細胞をつなぐ狭い橋(インタセルラーブリッジ)で現場監督のように働き、分裂がきれいに完了するようにする分子の一群の仕組みを明らかにします。
娘細胞間の最後の橋
細胞が遺伝情報を複製し染色体を分離した後、物理的に分かれる必要があります。タンパク質フィラメントからなる収縮リングが細胞の中央を締め付け、溝状の切開溝(クリービッジファロー)を作ります。この溝が内側に引き込まれると、二つの娘細胞は細いインタセルラーブリッジでつながれ、その中に密なコアであるミッドボディが残ります。ミッドボディは束状の微小管、足場タンパク質、シグナル脂質からなる小さく複雑な構造で、係留機能と制御センターの両方を果たし、分裂の最後の段階と最終切断を調整します。 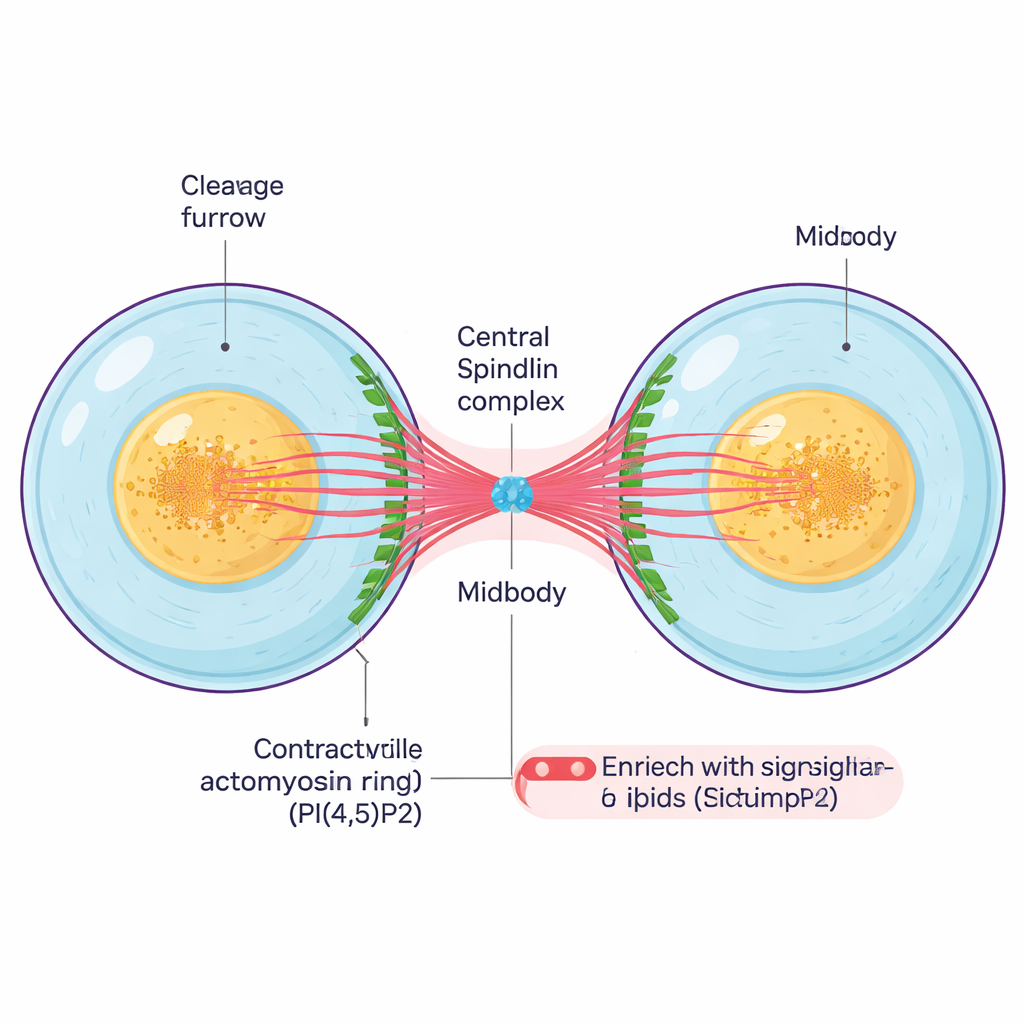
正しい場所に存在しなければならない脂質シグナル
この過程の重要な担い手のひとつが、細胞膜中のシグナル脂質であるPI(4,5)P2です。この脂質は収縮リングを構築・収縮させる多くのタンパク質を固定し、橋の安定化を助けます。問題は、PI(4,5)P2が膜内を拡散しうるにもかかわらず、細胞がどのようにしてその発現の場所とタイミングを制御しているかでした。著者らはPI(4,5)P2を合成するタイプI PIPキナーゼに注目し、特に複数の微妙に異なるスプライス体をもつPIPKIγという遺伝子に着目しました。ヒト細胞で各キナーゼを選択的に減少させ、高度な顕微鏡観察で効果を調べたところ、PIPKIγは細胞質分裂の後期、橋とミッドボディが形成されるときに特別な役割を果たしていることがわかりました。これは細胞表面全体のPI(4,5)P2量を大きく変えないにもかかわらずです。
セプチン足場が特殊な酵素を呼び寄せる
研究チームは、PIPKIγの二つのスプライスバリアント、i3とi5が、セプチンと呼ばれる構造タンパク質によって適切な場所に運ばれる精密な道具のように働くことを発見しました。セプチンはフィラメントやリングを形成して橋の形を整え、他の構成要素を組織します。生化学的なプルダウンと細胞イメージングにより、PIPKIγ-i3とPIPKIγ-i5はセプチン複合体に物理的に結合してセプチンフィラメントに装飾する一方で、他のPIPKIγ変異体はそうではないことが示されました。これらのスプライス挿入部の特定の二つのアミノ酸を変異させると、酵素はセプチンに結合できなくなりました。分裂中の細胞では、正常なPIPKIγ-i3/i5は拡散した膜パターンから切開溝に集中し、その後セプチンや別の足場タンパク質であるアニリンと同期してインタセルラーブリッジとミッドボディを輪郭づけます。i3とi5の変異体だけを除去すると、アニリンとセプチンが橋に沿ってミッドボディから散らばり、多くの細胞が細胞質分裂に失敗して多核化しました。
局所的な脂質産生が分裂装置を固定する
これらの効果が局所的なPI(4,5)P2産生に依存するかどうかを検証するために、著者らはミッドボディ周辺のPI(4,5)P2を測定し、この脂質を付加または除去する酵素を操作しました。PIPKIγ-i3/i5を枯渇させるとミッドボディでのPI(4,5)P2が減少し、PI(4,5)P2分解酵素を阻害すると逆の効果が生じました。重要なのは、正常でセプチン結合能と触媒活性を持つPIPKIγスプライス体を回復させると橋でのアニリンとセプチンの適切なクラスタリングが回復したのに対し、キナーゼ活性欠損型やセプチン結合能欠損型の変異体では回復しなかったことです。ライブイメージングと、試料を物理的に膨らませて微細構造を明らかにするエクスパンション顕微鏡法を用いて示されたのは、PIPKIγ-i3/i5がないとセプチンがもはや橋の微小管上に移動せず、橋が短く束化が弱くなり、中央紡錘体複合体(centralspindlin)と呼ばれる重要な複合体がミッドボディに強固に結合し続けられないということでした。 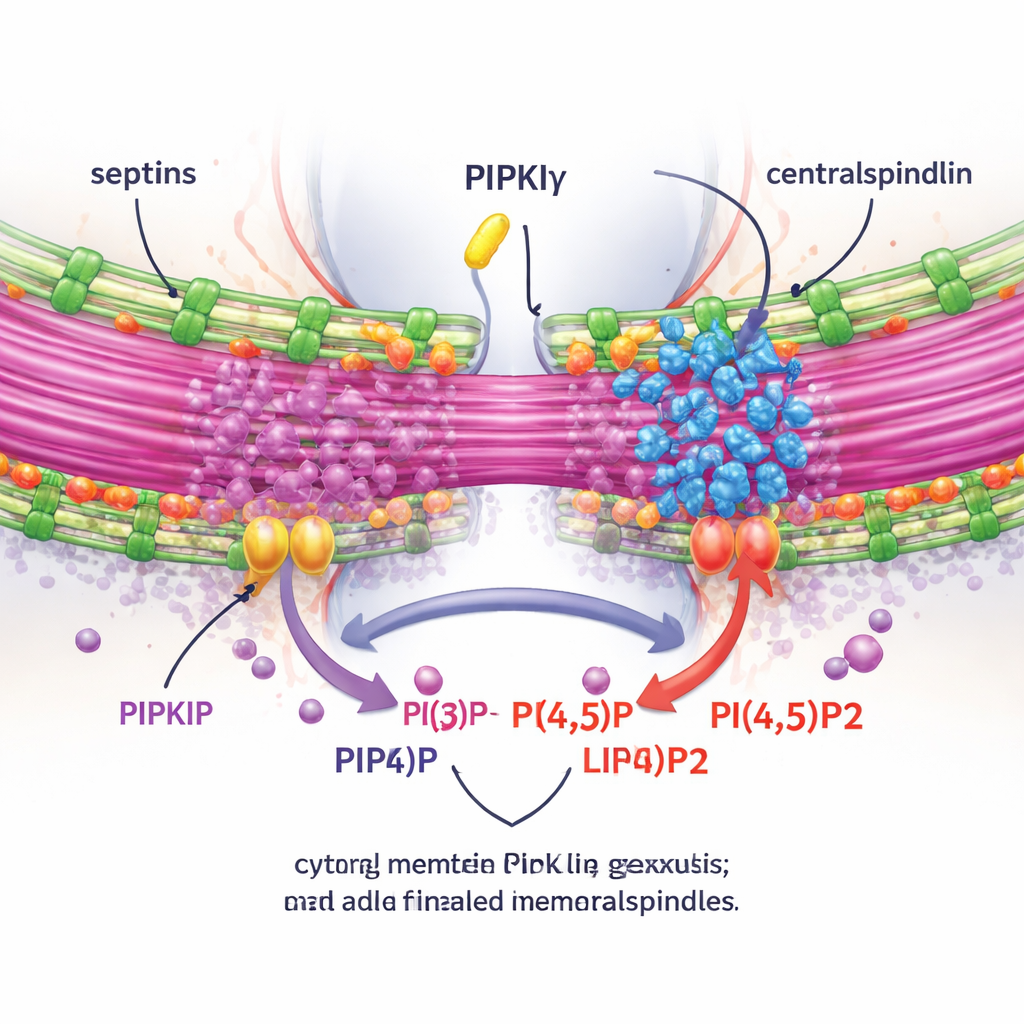
きれいな切断のためのチェックポイントを構築する
中央紡錘体はミッドボディの微小管を周囲の膜に結びつけ、細胞形状を制御する小さな分子スイッチを調節します。本研究は、中央紡錘体がセプチンとPIPKIγの両方と結合しており、どちらか一方を失うとミッドボディでの存在が同様に弱まることを示しています。著者らは、セプチンがPIPKIγ-i3/i5を浸入した溝(ingressed furrow)に呼び寄せ、そこでこれらの酵素が濃縮されたPI(4,5)P2のパッチを作るというモデルを提案します。この局所的な脂質プールは、結果としてアニリン、中央紡錘体、セプチンをミッドボディ近傍で安定化させ、橋の微小管の束化と安定化を促進し、インタセルラーブリッジが最終的な離断(アブスィジョン)まで成熟するのを可能にします。このシステムが乱れるとPI(4,5)P2が誤った場所に現れ、足場タンパク質が拡散し、微小管の束化が不十分になり、しばしば細胞質分裂が失敗します。
基礎細胞生物学を超えて重要な理由
特定のPIPKIγスプライスバリアントとセプチンが協調してミッドボディで局所的な脂質シグナルを生み出す仕組みを特定することで、本研究は非常に移動性の高いシグナル分子に空間的精密さをどのように与えるかを説明します。その精密さは細胞分裂を安全に完了させるために不可欠であり、染色体の誤分配や異常な細胞数を防ぎ、腫瘍の発生を抑えるのに寄与します。同じミッドボディ構造は分裂後の細胞運命や増殖にも影響を与えるため、それらの組み立て機構を理解することは、これらのナノスケールな足場の誤りががんにどう寄与するか、あるいは幹細胞を操作する方法を探る新たな道を開きます。
引用: Russo, G., Hümpfer, N., Jaensch, N. et al. Local PI(4,5)P2 synthesis by septin-associated PIPKIγ isoforms controls centralspindlin association with the midbody during cytokinesis. Nat Commun 17, 1482 (2026). https://doi.org/10.1038/s41467-026-69224-3
キーワード: 細胞分裂, 細胞質分裂, シグナル脂質, セプチン, がん生物学