Clear Sky Science · ja
水素原子移動を介した動的エピマー化によるアルキンの光触媒立体選択的編集で平面分子を3次元分子へ変換
平面的な分子を3次元へ変える意義
多くの現代医薬品は、合成が容易な平坦でシート状の分子断片に由来しますが、生体内で必ずしも理想的に振る舞うとは限りません。創薬の現場では、コンパクトな三次元骨格を持つ化合物の方がしばしば優れた性質を示すことが分かってきました:生体標的により密に適合したり、体内での挙動が変わったり、副作用が軽減される場合もあります。本稿は、単純で平面的な分子の“ワイヤー”を一段で複雑な3次元ケージへとひねる、新しい光駆動の手法を紹介します。これにより次世代医薬品や機能性材料の探索が迅速化される可能性があります。
直線から小さなケージへ
架橋環と呼ばれるケージ様構造を構築する従来法は、いったん比較的平坦な環系を作り、それを続く段階でつなぎ合わせるという、いわば回り道を取ることが多いです。その二段階戦略は有効ですが時間がかかり、到達可能な形状の幅も限られます。著者らは代わりに非常に単純な一次元の出発物質、すなわち直鎖アルキン(C≡C三重結合)とアルデヒド(小さなC–O単位)から直接、一本の操作でコンパクトな3次元骨格へ跳躍することを目指しました。通常の迂回を避けることで、創薬で価値ある新たな“化学空間”を開くことが狙いです。
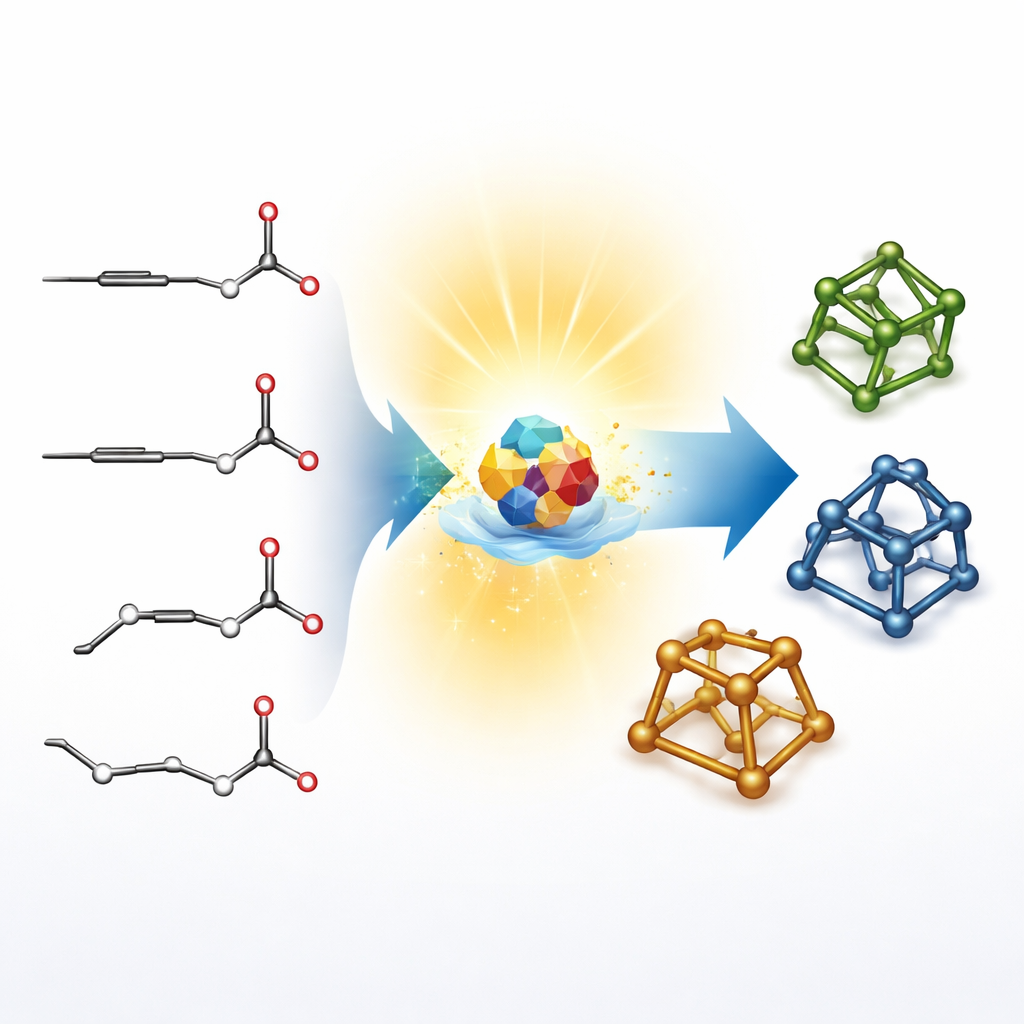
光に重労働をさせる
研究チームはデカタンスタットと呼ばれるポリオキソメタレートに基づく光感受性触媒を利用します。バイオレット光下でこの触媒はアルデヒドから水素原子を引き抜き、一時的に高活性なフラグメントを生成します。そのフラグメントがアルキンに付加し、折り返して五員環を形成します。この最初の環形成自体は、鍵となる炭素原子で多様な3次元配列の混合物を生じさせます。賢い仕掛けは同じ光駆動系がその場で何度も水素を引き抜き戻すことでこれらの配列を入れ替え、より安定な形へ混合物を寄せていける点にあります。
自己修正する3次元編集
発見の核心は動的キネティック分解として知られる内蔵の自己修正機能です。初期の環状中間体は空間配座がわずかに異なる二つの近縁の3次元形態として存在します。光活性化された水素のシャトルによりこれらは素早く相互変換し、別の塩基を助けとする閉環反応は最終的なケージ形成において一方のみを有利にします。その結果、優先される中間体が連続的に一つの明確な二環性生成物へと取り込まれ、劣勢な形は常にそのパートナーへ変換されます。可逆的な形の切り替えと選択的な捕捉の相互作用により、第一段階がかなり非選択的でも複数箇所の立体配向を高い精度で制御した生成物が得られます。
多様で有用な3次元骨格の構築
著者らは、この光駆動アプローチが幅広い出発物質で機能し、化学者が取り扱いたいさまざまな置換基でケージを飾ることができることを示しています。生成される骨格は、医薬化学で重宝される二つの族、bicyclo[2.2.1]heptanoneとbicyclo[3.2.1]octanoneに属し、天然物、触媒、材料にも見られる重要なビルディングブロックです。さらに、研究チームはこれらの3次元ケージを、発光材料の重要中間体や既知の脳受容体阻害剤の剛直化バージョンなど、より複雑な化合物へ変換できることを実証しました。ある例では、薬の柔軟な環を新たに作った3次元ケージに置き換えることで、生物学的な活性がわずかに改善しました。
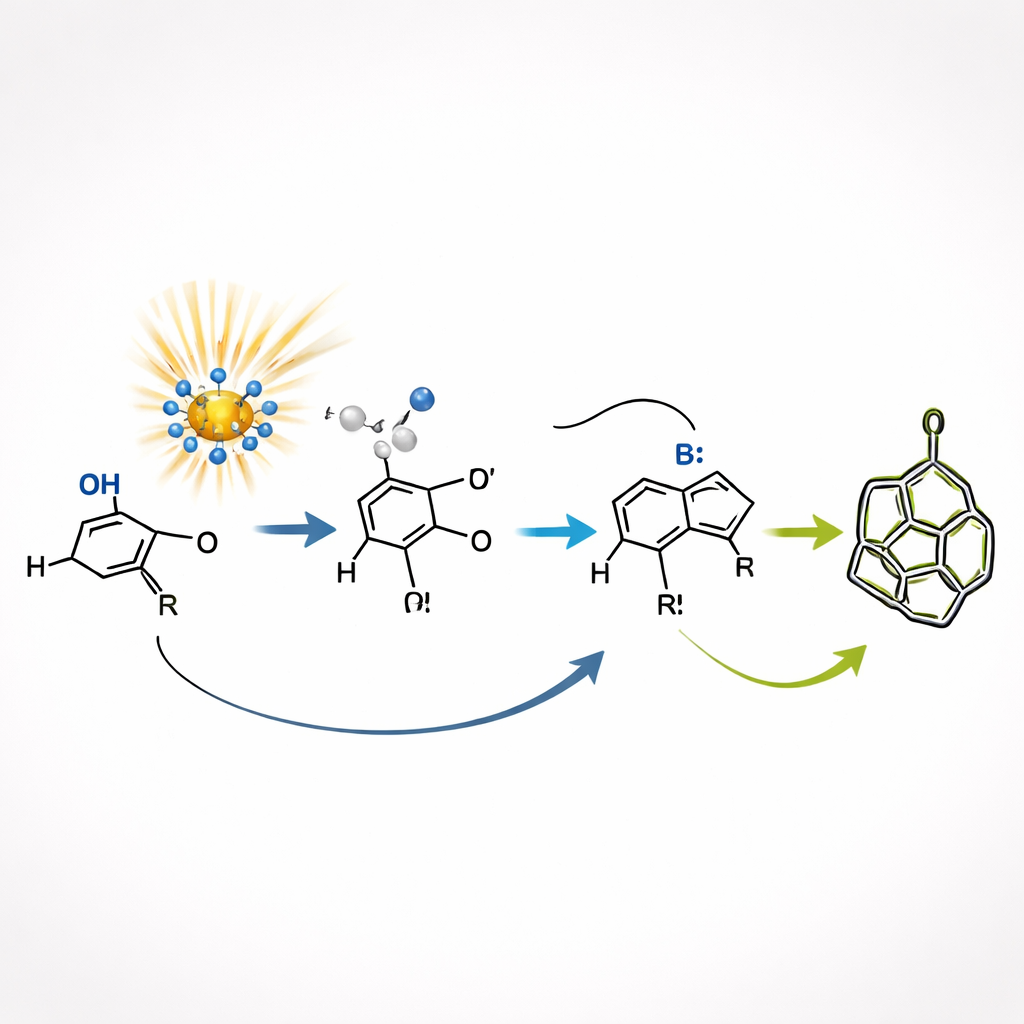
豊かな分子形状への近道
日常的な言い方をすれば、本研究は単純な直線状の分子“スティック”を光と賢い触媒を用いて一度の操作で精密な3次元“彫刻”へ折り畳む方法を示しています。このプロセスは骨格の構築と原子の空間配置の微調整という二つの仕事を同時に行い、しかも穏やかな条件で進行します。アルキンは一般的で安価な原料であるため、この戦略は安価な原料を複雑で薬剤様の骨格へ変換する汎用的な近道になり得ます。化学者が三次元分子の領域をさらに開拓する中で、本手法のようなツールは、設計によってよりよく機能する医薬品や材料の創製に重要な役割を果たす可能性があります。
引用: Gu, Z., Zeng, T., Yuan, Z. et al. Photocatalytic Stereoselective Editing of Alkynes to 3D Molecules via Hydrogen Atom Transfer-Mediated Dynamic Epimerization. Nat Commun 17, 2518 (2026). https://doi.org/10.1038/s41467-026-69219-0
キーワード: 光触媒, 水素原子移動, 3次元分子骨格, 動的キネティック分解, 医薬化学