Clear Sky Science · ja
パントRAF阻害薬エクサラフェニブはBRAFクラスII/IIIのNSCLCを標的とし、ARAF–KSR1による耐性と併用戦略を解明する
なぜこの研究が肺がん患者にとって重要か
多くの人が、特定の遺伝的変化に狙いを定める標的治療薬について聞いたことがあるでしょう。しかし、特にBRAFという遺伝子に比較的まれな変異を持つ腫瘍を抱える多くの肺がん患者にとって、現行の標的薬は十分に効果を発揮しません。本研究は、新たな実験薬エクサラフェニブを紹介し、より広範なBRAF駆動腫瘍を標的にする設計と、がん細胞がそれを回避しようとする仕組みを示すことで、腫瘍をより長く抑え込む可能性のある併用治療を明らかにします。
見落とされがちな多数派の変異
研究者らはまず基本的な問いを立てました:進行がん、特に非小細胞肺がん(NSCLC)において、BRAFの異なる変異はどれほど一般的か。16万人を超える大規模なリキッドバイオプシーのデータベースを用いて、血流中を循環する腫瘍DNA断片を解析したところ、肺がんでは患者のおよそ4〜5%にBRAF変異が見つかり、世界的には多数の患者に相当することが分かりました。重要なのは、これらの肺腫瘍の約3分の2が、現在承認されているBRAF薬では効果的に標的にできないいわゆるクラスIIおよびクラスIIIのBRAF変異を有していた点です。特にクラスIIを持つ患者は、より一般的なクラスI変異を持つ患者に比べて生存期間が短い傾向があり、これはクラスI患者は確立された標的治療を受けられる一方で、クラスII/III患者は主に標準化学療法や免疫療法を受けることが多いためと考えられます。
経路全体を標的とする次世代薬
BRAFは細胞表面から核へ成長シグナルを伝えるタンパク質の中継(MAPK経路)の一部です。既存の多くのBRAF薬は一つの変異型のみを遮断するよう設計されており、場合によっては正常細胞の関連タンパク質を逆に刺激してしまうこともあります。エクサラフェニブは異なるアプローチで作られており、単独あるいは二量体として働く複数のRAFファミリー(ARAF、BRAF、CRAF)を遮断する“パントRAF”阻害薬として設計され、他の多くの細胞酵素はできるだけ温存するように作られています。数百種類のヒトキナーゼに対する生化学的試験では、エクサラフェニブは三つのRAFタンパク質を強力に阻害しながらオフトarget(非特異的)作用は少なく、既存のパントRAF化合物より安全性プロファイルが良好である可能性を示唆しました。
治療困難な腫瘍モデルでの強力な効果
研究チームは、さまざまなBRAFおよびRAS変異を持つ細胞株やマウスモデル、患者由来腫瘍を用いてエクサラフェニブを評価しました。細胞培養では、エクサラフェニブは古典的なBRAF V600E変異細胞のみならず、クラスIIおよびクラスIII変異を持つ細胞や、現行の有効な標的薬が乏しい多くのRAS変異細胞において増殖を抑え、MAPKシグナルを遮断しました。これらの変化を持つ肺腫瘍を移植したマウスでは、エクサラフェニブは用量依存的に腫瘍を縮小または成長抑制し、薬物濃度、経路抑制、腫瘍反応の間に明確な関連が認められました。進行したBRAF変異肺がんの2例の早期臨床データ(まれなBRAF融合を持つ患者とクラスII点変異を持つ患者)は部分奏効と有意な症状改善を示し、前臨床データの臨床的関連性を支持しました。
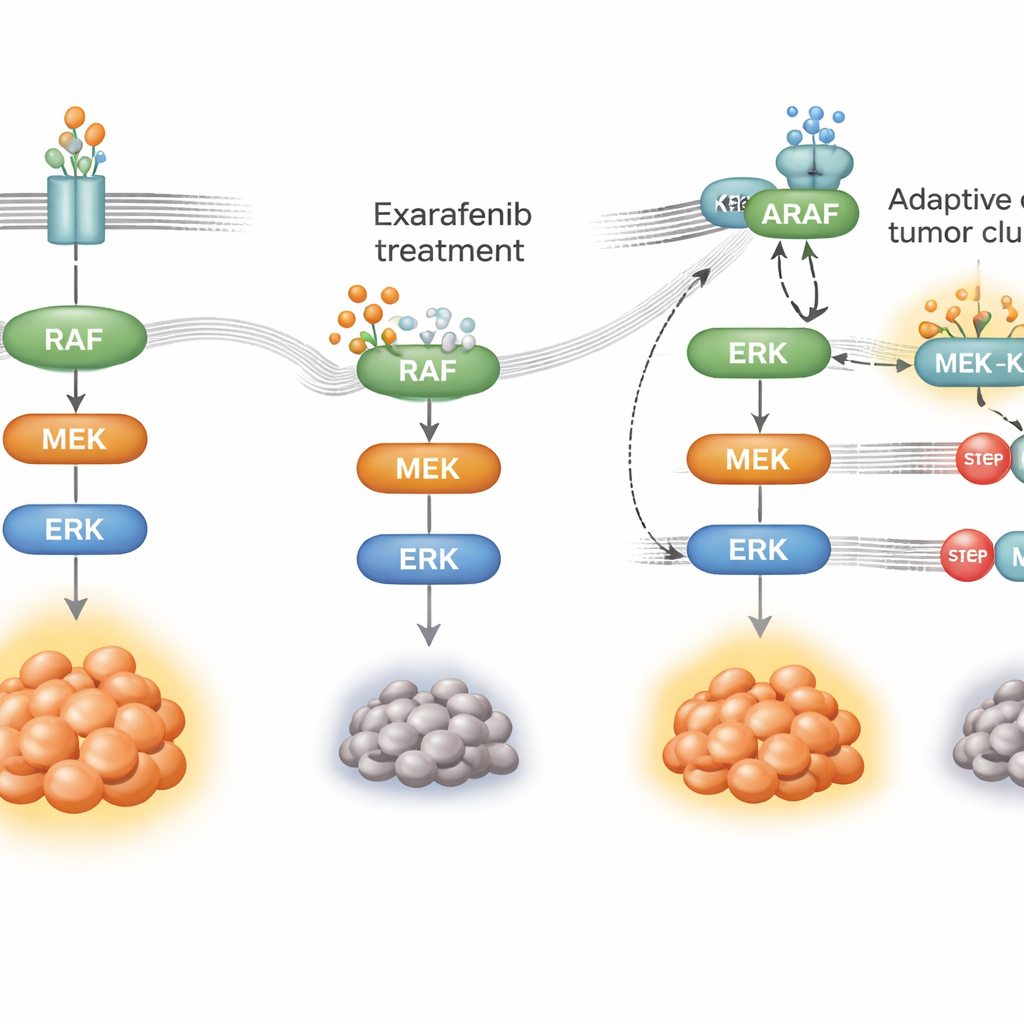
がんがどのように薬を回避するか
どの標的治療も永遠に効くわけではなく、がん細胞は適応します。腫瘍がエクサラフェニブに耐性を示す仕組みを探るため、研究者らは数か月にわたりBRAF変異肺がん細胞を薬にさらし、耐性集団が出現するまで選択しました。これらの細胞は同じ増殖経路に依存しているものの、その利用法を再配線していました。変異BRAFへの依存を減らし、上流のスイッチであるRAS活性を高め、別のファミリーメンバーであるARAFと足場タンパク質KSR1の利用を増やしていました。薬剤圧下ではARAFとKSR1が緊密な複合体を形成し、エクサラフェニブが結合している間もMAPK中継を維持していました。研究者がARAFやKSR1を選択的にサイレンシングしたり、RAS活性を低下させると、耐性細胞は再びエクサラフェニブに感受性を取り戻し、生存シグナルは崩壊しました。
耐性に先手を打つ併用戦略
この機序図を基に、研究チームは元の経路と回避経路の双方で共有される分岐点を遮断できるパートナー薬を探しました。エクサラフェニブと、MAPK中継の下流にある重要な段階であるMEKまたはERKを阻害する薬剤を組み合わせると、多くの細胞・マウスモデルで強い相乗効果が得られ、もともと感受性の低い腫瘍や獲得耐性を示す腫瘍も含めて有効でした。これらの併用は経路をより長く抑え、細胞死をより多く誘導し、動物ではしばしばエクサラフェニブ単剤の高用量と同等かそれ以上の効果を示し、明らかな追加毒性は観察されませんでした。RASを直接標的とする薬剤も、RASが明確に耐性を駆動しているモデルでエクサラフェニブの効果を高め、臨床的に有望な別の戦術を示唆しました。
患者にとっての意義
クラスIIまたはクラスIIIのBRAF変異、あるいは複雑なBRAF融合やRAS共変異を持つNSCLC患者には、現時点で承認された標的治療がなく、転帰はより一般的な変化を持つ患者に比べて遅れをとっています。本研究は、エクサラフェニブがRAF駆動のシグナル伝達を広く遮断することでそのギャップを埋める可能性があるという強力な科学的根拠を提示します。また、腫瘍がARAF–KSR1のバイパス経路を介して適応する方法を説明し、RAFとMEK阻害剤を組み合わせる、あるいはRAS阻害剤を加えることで経路を多層的に遮断すれば、より深く持続的な腫瘍制御が得られる可能性を示しています。これらの知見は、これまで十分に治療されてこなかった大きな肺がん患者群に合わせた併用標的治療を臨床で検討する道筋を描いています。
引用: Manabe, T., Bergo, H.C., Li, Q. et al. Pan-RAF inhibitor exarafenib targets BRAF class II/III NSCLC and reveals ARAF-KSR1 resistance and combination strategies. Nat Commun 17, 2484 (2026). https://doi.org/10.1038/s41467-026-69216-3
キーワード: BRAF変異肺がん, パントRAF阻害薬, MAPKシグナル伝達, 薬剤耐性, 標的治療の併用