Clear Sky Science · ja
14-3-3ζはFOXO3aのDNA結合ドメインと相互作用し、二重モチーフのテザリングで競合的にDNAを解離させる
がん細胞が自らの自滅スイッチをどう遮断するか
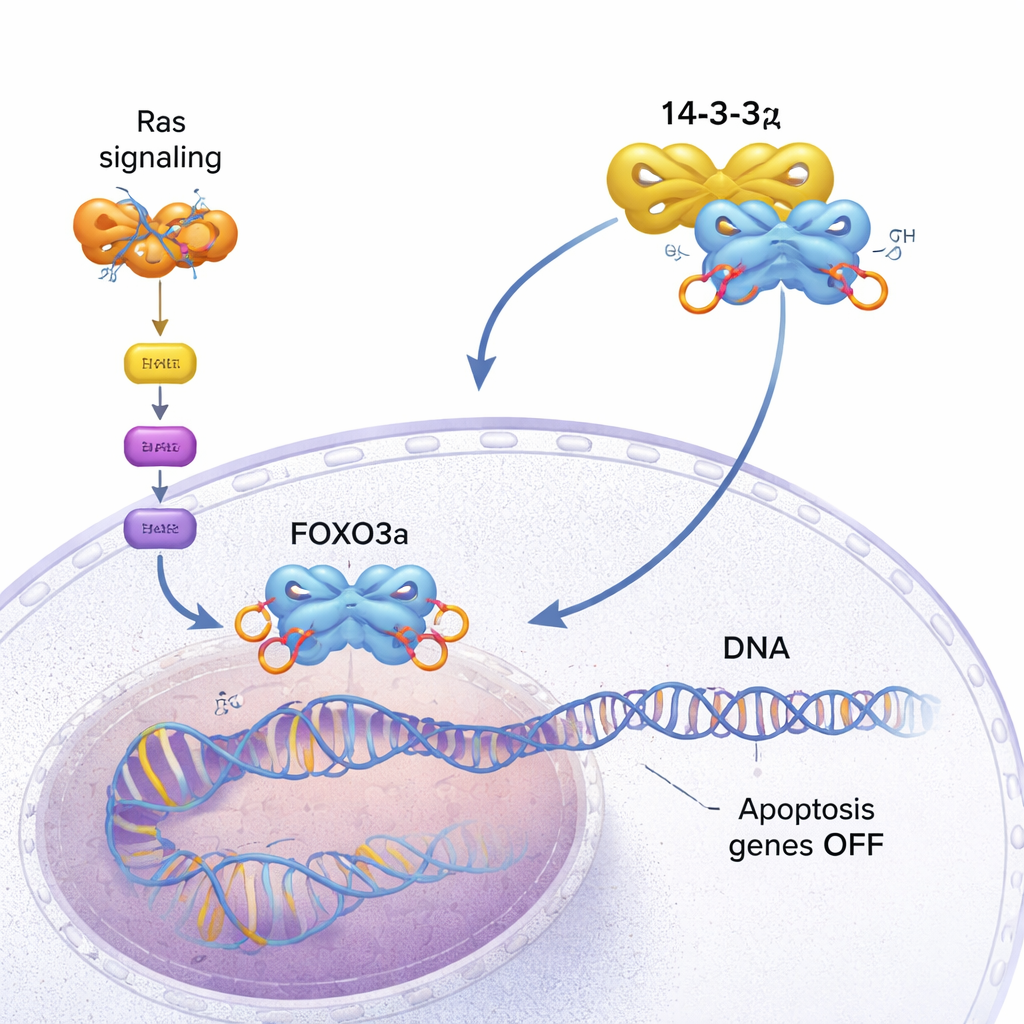
私たちの細胞には、あまりに損傷したり危険になったりしたときに自ら死を誘導する組み込みのフェイルセーフ機構があります。そのひとつを制御するのがFOXO3aというタンパク質で、異常な細胞に自殺を促す遺伝子をオンにします。しかし多くのがんはFOXO3aを沈黙させ、増殖を続ける方法を見つけ出します。本研究は、別のタンパク質である14-3-3ζがどのようにしてFOXO3aをDNAから引き離し、この自滅スイッチを無効化するのかを分子レベルで掘り下げています。
がんに抵抗する番人タンパク質
FOXO3aは細胞の安全検査官のように働きます。特定のDNA配列に結合して、異常が起きたときに増殖を抑えたりプログラムされた細胞死(アポトーシス)を誘導したりする遺伝子を活性化します。健康な細胞ではこれが腫瘍の形成を防ぎます。しかし多くのがんでは、変異したRasタンパク質による増殖促進経路が恒常的にオンになりがちです。この経路はAKTというキナーゼを活性化し、AKTはFOXO3aの複数の部位にリン酸基を付加します。そのリン酸化部位が14-3-3ζという二量体の“アダプター”タンパク質のドッキング場所を作ります。14-3-3ζがFOXO3aにとりつくと、細胞の内部ブレーキが効かなくなり始めます。
単純な結合強度では説明できない理由
関連するタンパク質FOXO4を用いた以前の研究では、14-3-3がFOXO因子をDNAから引き離すのは単により強く結合するからだと示唆されていました。しかしFOXO3aはその天然のDNA標的を、旧来のモデルが想定したより強く好むことが分かっています。本研究では、DNA結合ドメインと二つの重要なリン酸化部位を含むFOXO3aのバージョンを作製し、このタンパク質がDNAまたは14-3-3ζにどれだけ強く結合するかを測定しました。結合強度の差は控えめで、14-3-3ζはDNAより約2倍程度強いパートナーに過ぎませんでした。それでも、クロマトグラフィーで分子の移動を追跡する混合実験では、14-3-3ζがほぼ完全にFOXO3aからDNAを解放でき、期待よりも約100倍も競合的に有利であるかのように振る舞いました。この不一致は、追加のメカニズムが働いていることを示唆しました。
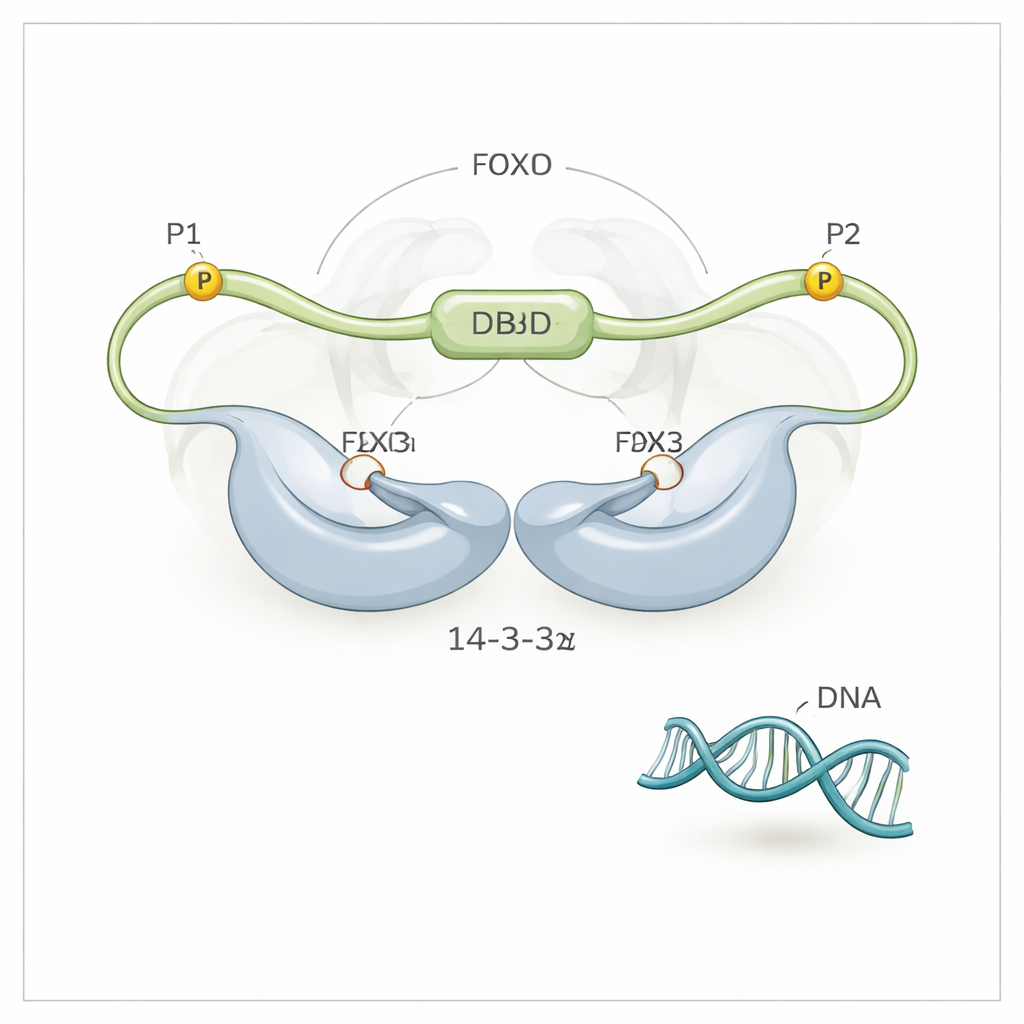
DNAを締め出す三点グリップ
高分解能のNMR分光法を用いて、研究チームは14-3-3ζがFOXO3aの二つのリン酸化モチーフ(P1とP2)を掴む以上のことをしていると発見しました。14-3-3ζはFOXO3aのDNA結合ドメイン(DBD)自体—通常DNAに密着する表面—とも直接的に、ただし弱めに接触しているのです。14-3-3ζは二つの溝を持つ対称的な二量体を形成します。各溝がFOXO3aの一つのリン酸化モチーフを挟み込み、FOXO3aを二点で14-3-3ζにテザー(係留)します。これらのうちP2は配列上でDBDに非常に近いため、この“二重モチーフ・テザリング”は14-3-3ζをDBDのすぐそばに保持し、DBDがDNAではなく14-3-3ζの表面にぶつかって結合する確率を大幅に高めます。研究者たちはDBDが14-3-3ζ二量体の両側を行き来し、時間の大部分をDNAから遮蔽された状態で過ごしていることさえ観察できました。
どのリン酸化タグが重要か
二つのリン酸化部位の役割を明らかにするため、研究チームは一度に一つだけがリン酸化可能なFOXO3a変異体を作製しました。DBD近傍のP2のみが活性化されている場合、14-3-3ζはDNAを部分的に押しのけることはできても完全には解離させられませんでした。より遠位にあるP1のみが活性化されている場合、14-3-3ζはFOXO3aに結合できてもそのDNA保持力にはほとんど影響を与えませんでした。DNAの完全な解放には両方の部位が協調して働くことが必要でした:P1は14-3-3ζの高親和性な初期ドッキング点を提供し、P2は二量体をDBDに十分近づけて、その局所濃度を事実上非常に高くします。この多段階のテザリングは、控えめな結合の好みを強力なDNA追い出し能へと増幅します。
分子間の綱引きから新たな薬物アイデアへ
非専門家向けの要点は、がん細胞が単なる結合強度の差だけでなく巧妙な分子ジオメトリを利用して主要な腫瘍抑制タンパク質を沈黙させている、ということです。14-3-3ζはFOXO3aの二つの小さなドッキングタグを錨点として使い、次にFOXO3aコア領域のDNAを掴む面を覆い隠すように手を伸ばし、細胞死遺伝子をオンにするのを阻みます。同じFOXOおよび14-3-3ファミリーは多くの組織で広く使われているため、この二重テザリング戦略は他のがんでも一般的である可能性が高いです。リン酸依存のアンカーのいずれか、あるいはFOXO3aのDNA結合面との弱い接触を破壊することで、腫瘍細胞における自己破壊プログラムの活性化を回復させることができるかもしれず、抗がん薬設計に有望な新たな角度を提供します。
引用: Enomoto, S., Kuwayama, T., Nakatsuka, S. et al. 14-3-3ζ interacts with DNA-binding domain of FOXO3a and competitively dissociates DNA by dual-motif tethering. Nat Commun 17, 1503 (2026). https://doi.org/10.1038/s41467-026-69203-8
キーワード: FOXO3a, 14-3-3タンパク質, アポトーシス, Ras–AKTシグナル伝達, がん治療薬