Clear Sky Science · ja
P450-レドックスパートナー最適化とDoxAの構造解析によるドキソルビシン生合成の代謝工学
がん薬の由来が重要な理由
ドキソルビシンは白血病から乳がんまで幅広いがん治療に用いられる現代化学療法の主力薬の一つです。それでも何十年もの使用にもかかわらず、この薬の製造法は意外に迂回的です。工業的には通常、関連化合物から合成され、元の微生物に最終工程を任せることは少ないのです。本研究は、生産菌が最後の化学工程をうまく完了できない理由を明らかにし、その内部機構を再設計することで完全なドキソルビシンの産生を大幅に増加させられることを示し、より信頼性が高く潜在的に低コストな供給への道を開きます。
土壌細菌から命を救う医薬へ
ドキソルビシンはアントラサイクリン類に属し、土壌細菌の属であるStreptomycesが作る天然分子群です。これらの化合物は、塩基対の間に滑り込む堅く平らな炭素骨格と、DNAの溝に収まる糖部分を共に持ちます。これらが合わさって細胞のDNAを扱う機構を妨げ、最終的に細胞死を誘導します ― 急速に増殖するがん細胞に対して有用です。代表的な生産菌であるStreptomyces peucetiusは、主に前駆体薬のダウノルビシンを作り、わずか一つの酸素を持つ置換差しかないより有効なドキソルビシンはわずかな量しか生産しません。その小さな構造変化が活性を劇的に向上させますが、微生物にとって効率的に達成するのは驚くほど難しいことがわかりました。
細胞内部の“配線”を見つける
薬骨格の最後の三段階の酸化を担う重要な酵素はDoxAと呼ばれ、シトクロムP450ファミリーに属します。小さな化学工場のように、DoxAは酸素を活性化し薬分子に新たな酸素原子を導入するために安定した電子の流れを必要とします。細菌内では、これらの電子はレドックスパートナーとして知られる補助タンパク質の中継を通じて供給されます。S. peucetiusのゲノムにはいくつかの候補が含まれており、どれがDoxAと実際に組むかは不明でした。正常株、ダウノルビシンが豊富な変異株、ドキソルビシンが豊富な変異株の遺伝子発現と代謝を比較することで、研究者らは一つのフェレドキシン(Fdx4)と一つのフェレドキシン還元酵素(FdR3)を自然なパートナーとして特定しました。試験管内反応でこの三者を再現すると、DoxAはまさにこの特定の電子伝達系に接続されたときに最も良く働くことが確かめられ、機器に合った電源アダプターを選ぶような関係であることが示されました。
酵素自身が引き起こす停滞を解消する
正しい“配線”があっても、DoxAはダウノルビシンをドキソルビシンに変換する最終段階で停滞しがちです。以前の研究は、生成物自身が酵素を詰まらせる可能性を示唆していました。研究チームは隣接する遺伝子で機能が不明だったdnrVに注目しました。生化学的試験により、DnrVタンパク質はドキソルビシンを含むさまざまなアントラサイクリン分子を化学変化させることなく強く結合することが示されました。DoxA反応にDnrVを加えると化学反応の流れが大幅に改善し、前駆体から最終薬までの完全な変換が可能になり、破壊的な副反応を回避できました。実務的には、DnrVは内部のスポンジのように働き、新たに作られたドキソルビシンを吸い取り、酵素の詰まりや生産細胞内のDNA損傷を防ぎます。
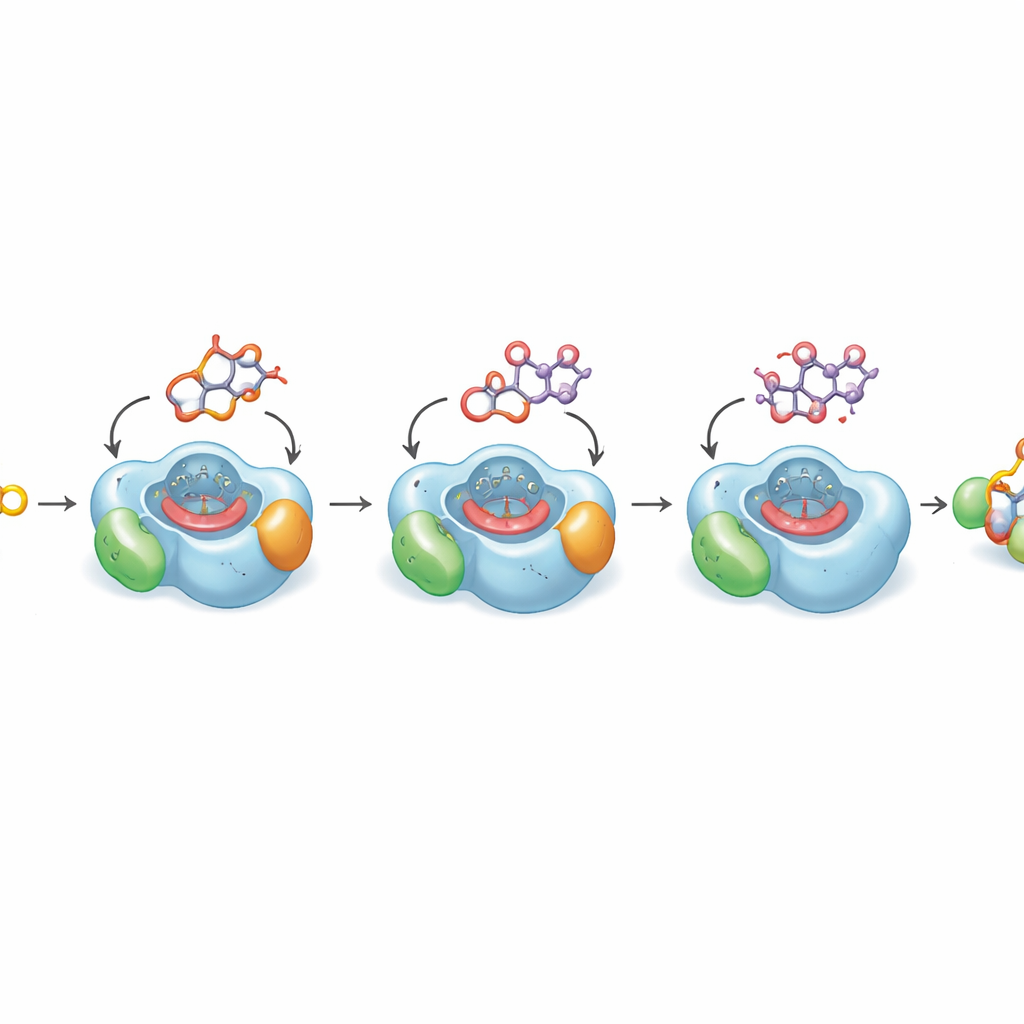
なぜ最後の段階がこれほど遅いのかを可視化する
重要な最後の酸化が本質的に遅い理由を理解するために、著者らはDoxAに結合した三つの連続する中間体の高解像度結晶構造を解きました。これらの構造は、平らな薬コアと付随する糖が酵素のヘム群の上にある狭いポケットにどのように収まるかを明らかにします。ヘムは酸化を行う反応性の金属中心です。初期段階では、修飾されるべき炭素原子はヘムに近く、反応に理想的な位置にあります。しかし最終基質であるダウノルビシンでは、水酸化されるべき分子部分がヘムから離れて小さな油性キャビティに向かって曲がっており、量子計算はその配向がエネルギー的に有利であることを示します。マイクロ秒スケールのコンピュータシミュレーションは、その分子が最後の酸素導入に有効な姿勢を取るのは稀であることを確認しました。この構造的な偏りがドキソルビシンへの変換が本来効率的でない理由を説明します。
より良いドキソルビシン生産株の構築
こうした知見を手に、研究者らはランダム変異に頼るのではなく理論的に菌株を再設計しました。生産を安定させるためのDNA修復遺伝子を導入し、ついでdoxA、最適なレドックスパートナーであるfdx4とfdr3、および有用な結合タンパク質dnrVのコピーを適切に選んだプロモーターの下で導入して量のバランスを取れるようにしました。培養条件も微調整し、毒性のある粘着性中間体を吸着する特殊樹脂を用いました。実験室フラスコおよび20リットルバイオリアクターで、最良の改変株は1リットル当たり336ミリグラムのドキソルビシンを生産し、ドキソルビシン対ダウノルビシンの比率は81:19でした ― 出発株に比べて約180%の増加で、はるかに純度の高い生成物混合物です。
将来のがん薬供給にとっての意義
電気的な補助システムと主要酵素の3次元構造の両方を解剖することで、本研究は医療的に重要な微生物が最も価値あるアントラサイクリンの生産でなぜ力を発揮できていないかを説明します。DoxAを自然なレドックスパートナーと組ませ、薬を結合する補助タンパク質を追加し、遺伝子発現のバランスを取り直すことで、消極的な生産株を強力なものに変えられました。さらなる酵素改良で最後の化学段階をさらに加速できる可能性はありますが、この研究は既に完全に生物学的なドキソルビシン製造を工業現実に一歩近づけています。患者や医療制度にとって、こうした進展は主力の化学療法薬へのより安全で拡張可能、かつ費用対効果の高いアクセスにつながる可能性があります。
引用: Koroleva, A., Artukka, E., Yamada, K. et al. Metabolic engineering of doxorubicin biosynthesis through P450-redox partner optimization and structural analysis of DoxA. Nat Commun 17, 2358 (2026). https://doi.org/10.1038/s41467-026-69194-6
キーワード: ドキソルビシン生産, アントラサイクリン生合成, 酵素工学, 微生物による医薬品製造, シトクロムP450