Clear Sky Science · ja
ヘム・ペルオキシダーゼ触媒中間体で延長した鉄-酸素結合をフェリック・オキシル励起状態で説明できるか?
酵素における鉄と酸素の結合が重要な理由
細胞内では、酵素と呼ばれる特別なタンパク質が酸素を利用して強力な化学反応を安全に進めます。その中でもヘム・ペルオキシダーゼは、中心にある鉄–酸素ペアを使って過酸化水素という反応性で潜在的に有害な分子を分解します。何十年も、科学者たちはこの鉄–酸素結合の正確な性質について議論してきました:それはしっかりした二重結合に近いのか、それとも緩い単結合に近いのか――そしてそれが酵素の働きに何を意味するのか?本研究はウルトラファストX線法と高度な計算を用いてこの謎に取り組み、その答えが鉄–酸素ユニット自身のきわめて短命な励起状態にあることを明らかにします。
酵素の動きをリアルタイムで追う
研究者たちは細菌由来の染料脱色性ペルオキシダーゼに着目しました。このヘム酵素は通常、Compound I と Compound II と呼ばれる二つの重要な高エネルギー形を循環します。これらの形はいずれも酸素に結合した鉄原子を特徴とし、酵素が過酸化水素を処理し他の分子を酸化する際の中心です。類似酵素に対する以前の実験では不可解に長い鉄–酸素結合長が報告され、一部の研究者はそれをX線による変化か、プロトン付加による性質の変化の証拠と解釈しました。そうしたアーティファクトを避けるため、チームはX線自由電子レーザーでの時間分解連続フェムト秒結晶構造解析を用い、室温で数千の微小タンパク結晶からの回折とX線発光信号を数十フェムト秒という損傷が起きる前の時間スケールで捉えました。
結晶内で化学が展開する様子を観察する
実験では、わずかに改変した酵素のマイクロ結晶を移動するテープ上で過酸化水素と直接混合し、遅延時間を0.5秒から数十分まで変えてプローブしました。初期の時間点ではCompound Iの形成が有利で、後の時間点ではCompound IIが優勢になります。構造データは、両中間体において鉄原子がヘムポケット内の単一の酸素原子の隣に位置し、タンパク質の保護ループ領域がこの強力な酸化中心を覆うように移動していることを示しました。重要なのは、精密な測定で鉄–酸素結合長が全ての時間点で約1.83オングストロームのままであり、古典的なフェリル(Fe(IV)=O)の二重結合としては長めで単結合に近い一方、X線発光および光吸収のスペクトル指紋はCompound IおよびIIに一致する高い酸化状態を明確に示していた点です。
単純な説明を排除する
実験は超短パルスと室温条件で行われたため、結合長の歪みを説明する通常の原因――X線誘起還元や低温による人工的効果――は大きく排除できます。チームはまた、鉄に結合した酸素がプロトン化されて二重結合が水酸化物様の単結合になった可能性も検討しました。しかし、類似ヘム中心の既知の酸解離特性や以前の化学的研究は、この種の酵素でそのようなプロトン化が起きる可能性に強く反論します。分光データはさらに、過酸化水素との反応後も鉄が期待どおり高い酸化状態かつ低スピン状態にとどまっていることを示し、予想外に長い結合が単純な化学形の変化ではなく微妙な電子効果に起因すると考える証拠を補強しました。
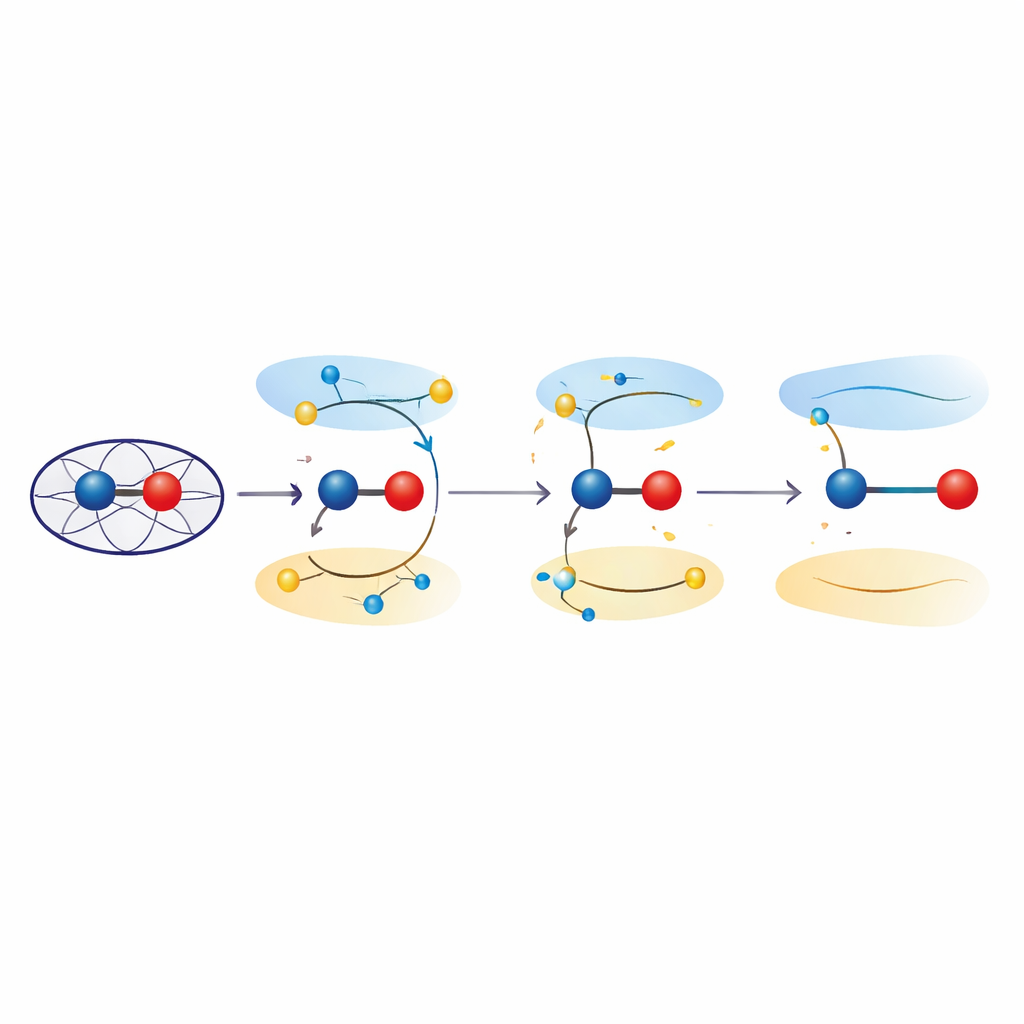
結合を伸ばす励起状態
これらの効果を調べるため、研究者たちは単純化モデルとタンパク質環境全体の両方で量子力学的計算を行いました。時間依存密度汎関数理論と量子力学/分子力学併用法を用い、鉄–酸素ユニット内で結合性軌道から反結合性軌道へ電子を励起すると好まれる結合長がどう変わるかを検討しました。これらの励起状態は基底のフェリル状態に対してエネルギー的に近く、いずれも鉄–酸素距離を1.8–1.9オングストロームの範囲に一貫して伸ばし、結晶学的観測と一致しました。電子分布の解析は、これらの状態では鉄–酸素対がもはや純粋なFe(IV)=Oの二重結合の振る舞いをせず、むしろフェリック–オキシルferric–oxyl的性格を帯び、酸素中心ラジカルに近いFe(III)に類似した性質を示すことを明らかにしました。実験構造の量子精密化は、こうした励起状態の記述が従来の基底状態モデルと同等以上にデータに適合することを確認しました。
酵素の力を理解するうえでの意味
簡潔に言えば、本研究はヘム・ペルオキシダーゼで観察された長い鉄–酸素結合が損傷、還元、隠れたプロトンを想定する必要はなく、フェリルユニットが短時間に低位置の励起状態へアクセスすることで自然に生じ得ることを示唆します。非専門家向けに言えば、多くの酸素活性化酵素の「仕事をする部分」は、従来考えられていたよりも動的で電子的に柔軟であり、電子の配置のわずかな変化が結合強度と反応性を変え、全体の化学種を変えずに作用する可能性があるということです。これらの励起状態を認識することは、強力な生体酸化剤の構造データ解釈を変え、人工触媒の設計においてこの微妙な電子バランスを模倣または意図的に調整する道を開くかもしれません。
引用: Williams, L.J., Kamps, J.J., Brânzanic, A.M.V. et al. Can ferric-oxyl excited states explain elongated iron-oxygen bonds in heme peroxidase catalytic intermediates?. Nat Commun 17, 2324 (2026). https://doi.org/10.1038/s41467-026-69192-8
キーワード: ヘム・ペルオキシダーゼ, フェリル中間体, 鉄-酸素結合, 励起電子状態, X線自由電子レーザー