Clear Sky Science · ja
効力選択的Nav1.7阻害剤により明らかになったヒトNav1.7不活性化の低電位依存性の分子決定要因
痛み信号の音量を下げる
なぜ軽い接触で激しい痛みを感じる人がいる一方で、ほとんど痛みを感じない人もいるのでしょうか。大きな理由の一つは、神経細胞にある電気信号を制御する小さなタンパク質の通路にあります。本研究は、Nav1.7と呼ばれるそのような通路の微妙な構造的特徴が痛みの引き金に特に重要である理由と、天然化合物ウバリグラノールDがそれを選択的に遮断する仕組みを明らかにします。この成果は、心臓の機能を鈍らせたり中枢を混濁させたりせずに、過活動の痛み神経だけを静める鎮痛剤設計の新たな戦略を示唆します。 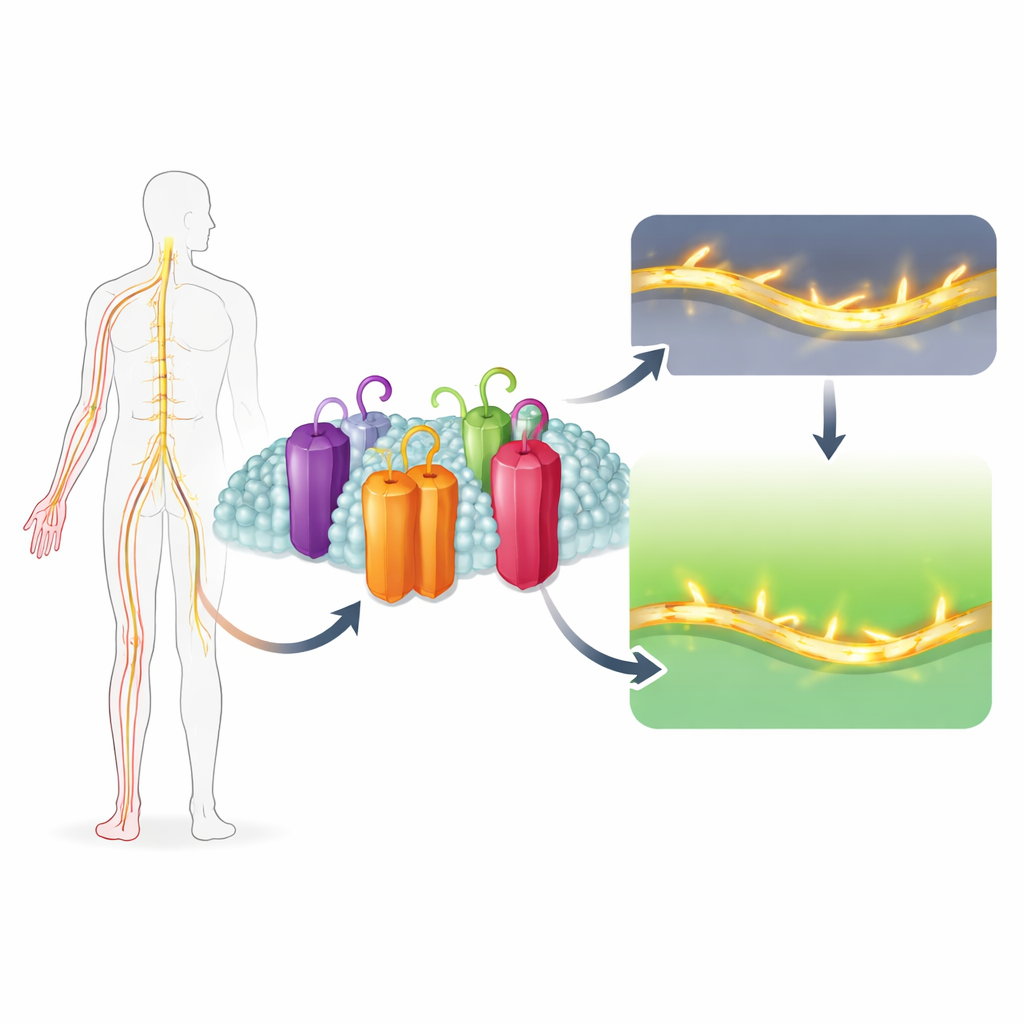
痛みに特化した番人
神経はナトリウムチャネルという微小な孔を使って電気インパルスを発生させます。これらの孔は一時的に開いて正に帯電したナトリウムイオンを細胞内に流入させます。ヒトには主に9種類のナトリウムチャネルがあり、それぞれ脳、筋肉、心臓、痛み感受性神経など異なる組織に適合しています。Nav1.7は末梢の痛覚線維に豊富に存在するバリアントです。特徴的なのは、他のチャネルよりも低い電位でオン・オフできる点で、微小な電位変化にも応答できるため、弱い痛みのシグナルを強力に増幅します。遺伝学的研究は、Nav1.7が過活動だと重度の遺伝性疼痛症候群を引き起こし、逆に完全に機能しないと痛みをまったく感じなくなることを示しています。
痛み選択的ブロッカーの発見
薬剤開発者は長くNav1.7を慢性痛治療の標的にしようとしてきましたが、Nav1.7は心拍や脳機能に必須の他のナトリウムチャネルに似ているため困難が伴います。ほとんどの候補薬は多くのチャネル型に結合し、副作用を引き起こしたり臨床試験で失敗したりします。研究者らは膜電位の変化を検出する細胞ベースのアッセイで1,500以上の天然化合物をスクリーニングし、ウバリア・グランディフローラという植物由来の分子群を同定、うちウバリグラノールD(UGD)に注目しました。UGDは複数のチャネル型でナトリウム電流を抑えましたが、Nav1.7をほぼ完全に沈黙させる一方で、他のナトリウムチャネルは高用量でも半分程度しか抑えませんでした。これは選択性がより強い結合から来るのではなく、結合後の効果(効力)がはるかに大きいことを意味します。 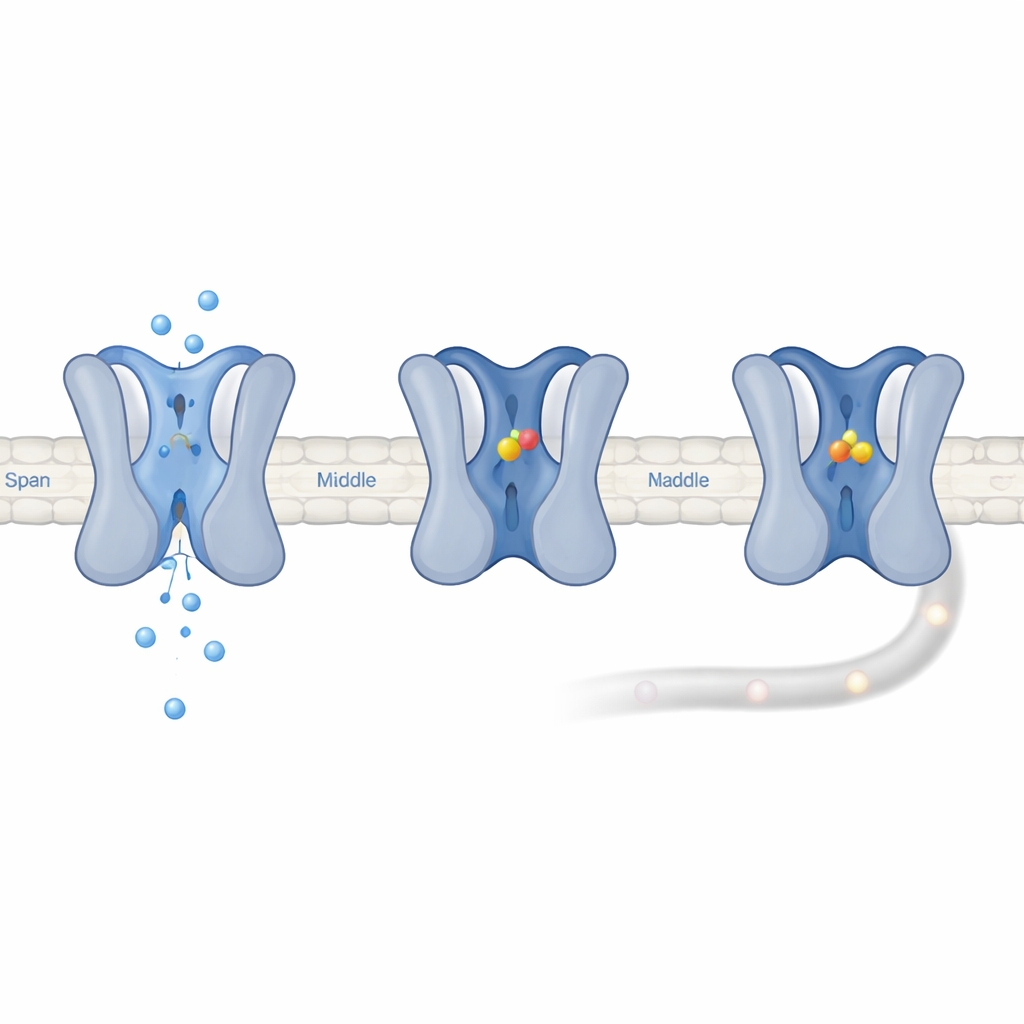
Nav1.7を特別にする原子サイズのわずかな違い
なぜUGDがNav1.7に非常に効果的なのかを解明するため、研究チームはNav1.7と密接に関連する脳チャネルNav1.2の間で領域を入れ替えたキメラチャネルを作製しました。これにより、ドメインIIIのS5とS6という構造区間の間、穴の外側付近にある小さな領域がUGDの完全な遮断力を決める鍵であることが特定されました。アミノ酸配列の比較では、ヒトの他のナトリウムチャネルがその位置により大きなメチオニンを持つのに対し、Nav1.7だけが1398位にスレオニンを持つことが分かりました。研究者らがNav1.7のスレオニンをメチオニンに置き換えるとUGDはもはやチャネルを完全には閉鎖できず、逆にNav1.2でメチオニンをスレオニンに変えるとそのチャネルはNav1.7のように振る舞いました。この単一の置換はチャネルの電位に対するオン・オフのタイミングも変え、スレオニンを持つとチャネルはより負の電位で速やかに開閉(不活性化)し、痛み神経の通常の静止電位付近でも非休止状態にある傾向を強めます。
チャネルを休止しにくい状態にロックする
電気生理記録は、UGDが閉じた状態や短時間開いた状態のNav1.7に付着するわけではないことを示しました。むしろUGDは、孔が閉じ回復に数百ミリ秒以上かかる長時間持続する「遅い不活性化」状態に入ったチャネルを好みます。UGD存在下では、チャネルがこの状態から脱するまでの時間が約10倍長くなり、UGDがこの状態を安定化させることを意味します。計算機シミュレーションは、UGDがドメインIIIのループとドメインIVのヘリックスが会合する箇所にできるポケットに収まり、5つのアミノ酸と重要な接触を作ることを示唆しました。これらの残基のいずれかを変異させるとUGDの効果が弱まり、ポケットの重要性が裏付けられました。Nav1.7のスレオニンが多い構造はより低い電位で不活性化状態へ移行しやすくするため、より多くのチャネルがUGDが好んで結合する状態にあり、結合親和性は似ていても機能的にNav1.7が他よりずっと強く抑制される理由が説明されます。
イオン孔から痛みの緩和へ
最終的に重要なのは、これらの分子イベントが実際の細胞にどのように影響するかです。ラットの後根神経節(dorsal root ganglion)由来の痛み感受性ニューロンでは、UGDは活動電位(痛み情報を運ぶ急速な電圧スパイク)の発生回数を大幅に減らし、低マイクロモル〜サブマイクロモル濃度で最終的に完全に停止させました。対照的に、主に異なるナトリウムチャネル(Nav1.5)を用い、やや低い静止電位で休止するヒト心筋様細胞は約60倍感受性が低かったです。これは、UGDのような「効力選択的」阻害剤が、Nav1.7が不活性化して薬剤好ましい状態にある頻度の違いゆえに、心臓など他の興奮性組織よりも痛み経路をはるかに強く抑えることができることを示唆します。
将来の疼痛治療への示唆
本研究は、1つのスレオニンという小さな構造的差異がNav1.7の低電位挙動と「しきい値電流」(痛みニューロンが発火するかどうかを決める微小信号)を生み出す基盤であることを明らかにしました。不活性化型のチャネルに結合してそれを安定化することで、UGDはその組み込みの傾向を利用し、他のナトリウムチャネルよりNav1.7をはるかに強く抑えます。一般向けの要点としては、著者らが体内の痛みの番人に対する正確な弱点を特定し、心臓や脳のチャネルを大きく乱すことなくそこを押さえる方法を示したということです。この知見は、単にNav1.7への結合親和性を追うのではなく、電位挙動とチャネル状態を標的にして過活動の痛み神経を静める新たな鎮痛剤設計への道を開きます。
引用: Zhao, F., Xi, C., Li, J. et al. Molecular determinant of low-voltage dependence of human Nav1.7 inactivation revealed by efficacy-based Nav1.7 selective inhibitor. Nat Commun 17, 2559 (2026). https://doi.org/10.1038/s41467-026-69184-8
キーワード: Nav1.7 ナトリウムチャネル, 慢性痛, ウバリグラノールD, 状態依存性阻害, 電位依存性ナトリウムチャネル