Clear Sky Science · ja
ビブリオ・コレラエのNADH-キノンオキシドレダクターゼにおける酸化還元駆動型Na+ポンピング機構は動的な構造変化に依存する
コレラの発電所が薬物標的になった理由
コレラを引き起こす細菌、ビブリオ・コレラエは、細胞膜に埋め込まれた小さな分子発電所を稼働させることで生き残り増殖する。本研究は、その主要なエンジンのひとつである酵素Na⁺-NQRが、ナトリウムイオンを細胞外へ汲み出す作業を行う際にどのように形を変えるかを、前例のない詳細で明らかにした。この分子機械を理解することは、生命がどのように栄養を利用可能なエネルギーに変換するかという基礎的な好奇心を満たすだけでなく、有害な細菌をヒト細胞に影響を与えずに停止させる新しい抗生物質設計の方向性を示す。
細菌のナトリウム駆動エンジン
多くの海洋性および病原性細菌は、呼吸鎖の最初の段階としてNa⁺-NQRに依存している。Na⁺-NQRは内膜に位置し、NADHという燃料分子から電子を受け取り、色のついた“補助”分子(補因子)を介して膜に埋め込まれた別の小分子キノンへと電子を渡す。電子が流れるエネルギーを利用して、酵素は細胞内から外へナトリウムイオン(Na⁺)を押し出し、ナトリウム勾配を形成する。この勾配は帯電したバッテリーのようなもので、細菌の鞭毛モーターの駆動、ATP(細胞のエネルギー通貨)の合成、栄養素の取り込みや薬物排出に使われる。Na⁺-NQRは細菌にのみ存在し、我々のミトコンドリアにある関連酵素とは大きく異なるため、高選択性の抗生物質の有望な標的となる。
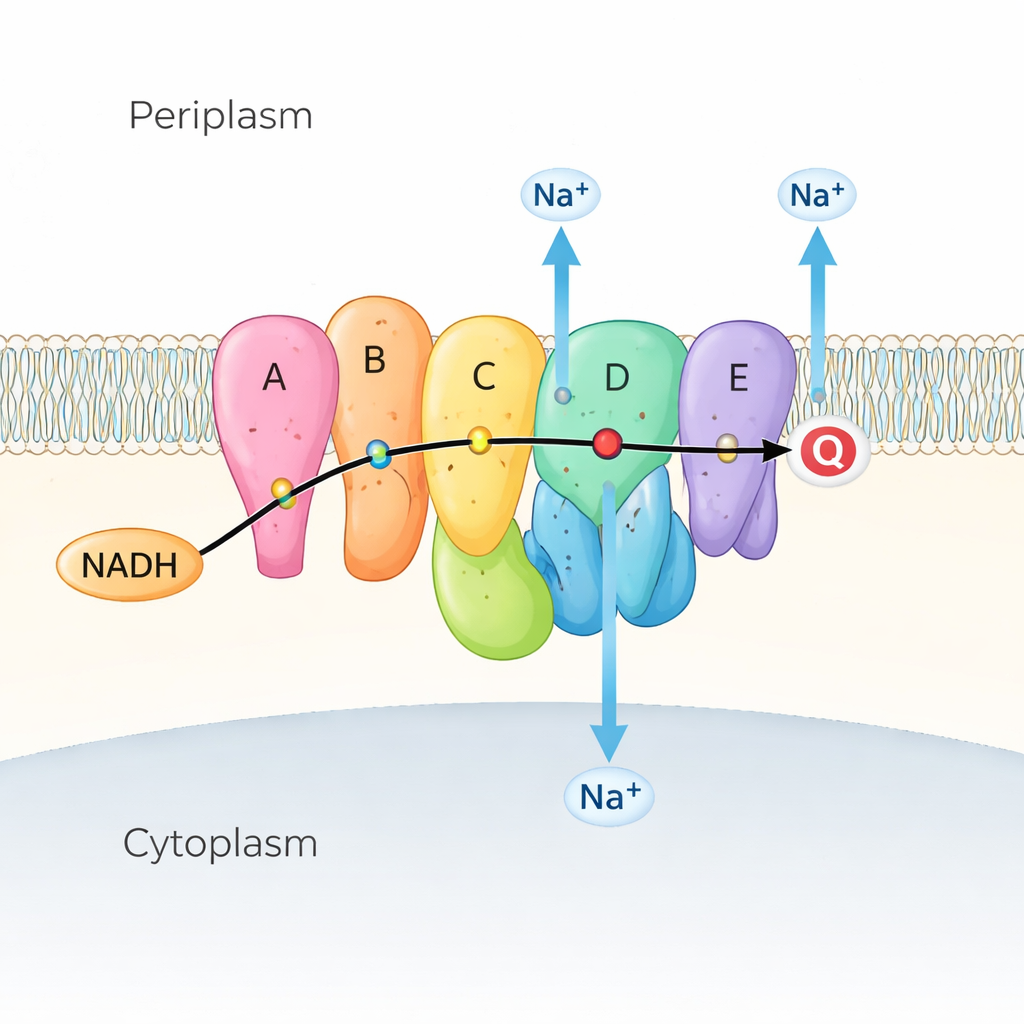
機械の動きを観る
これまでのX線やクライオ電子顕微鏡の断片的な断面像は、Na⁺-NQRのサブユニットや補因子の配置を示してきたが、一方で重要な電子の飛び移りが効率的に起こるには距離が離れすぎており、タンパク質が形を変える必要があるという謎も残していた。著者らはこれに対処するため、わずかに異なる多数の条件下でNa⁺-NQRを捕捉した。特定の補因子を除く変異体、反応を特定段階で止める薬剤、ナトリウムの有無の溶液などを用いた。高解像度のクライオEMと高度な画像解析により、同一酵素の複数のコンフォメーションを分離・再構築でき、静的なスナップショットをその作動サイクルの映画に変えた。
可動する腕とシャトルするクランプ
重要な発見の一つは、二つの電子担持補因子を持つ可撓性の細胞質サブユニットNqrFに関するものだ。研究チームはその“フェレドキシン様”ドメインが「上」「中」「下」の三つの位置を取ることを特定した。稀であるが決定的な「下」状態では、この小さなドメインがNqrDとNqrEという二つの膜サブユニットによって形成されたポケットに振り子のように入り込み、その鉄硫黄クラスターを電子を渡せるほど近づける。同時に、ペリプラズム側(外側)のサブユニットNqrCは可動式のクランプのように振る舞う。あるコンフォメーション(「安定」)ではNqrCは別の膜サブユニットNqrBに寄り添い、最終的なキノン受容体へ電子を渡す位置にある。別の(「移動」)コンフォメーションではNqrCはNqrD/Eへ移動し、フラビン補因子を彼らの鉄硫黄中心から電子を受け取れる近さにする。これらの動きは、NqrFとNqrCが大きな補因子間のギャップを橋渡しする動的な運び手として機能することを示す。
形の変化がナトリウムを汲み上げる仕組み
ナトリウムポンプの核心は、中心に束を作る膜貫通ヘリックスを持つ対のNqrDおよびNqrEサブユニットにある。構造解析と原子レベルの分子動力学シミュレーションの両方を用いて、著者らはNqrD/Eの鉄硫黄クラスターが還元(電子を受け取る)されると、細胞質側からNa⁺イオンと数個の水分子を引き寄せる負に帯電した部位が生じ、一時的な結合ポケットを形成することを示した。このポケットの上下に位置する疎水性アミノ酸は内側ゲートと外側ゲートのように振る舞い、イオンへのアクセスを制御する。NqrD/Eが「内向き開放」から「外向き開放」へ形を変えると、Na⁺はペリプラズム側へ移動し、鉄硫黄クラスターが再酸化される過程で最終的に放出される。シミュレーションではNa⁺が部分的に水和された状態を保つが、連続した水路が形成されることはなく、酵素が不要なプロトン漏洩に対してしっかりと密閉されていることを示唆している。
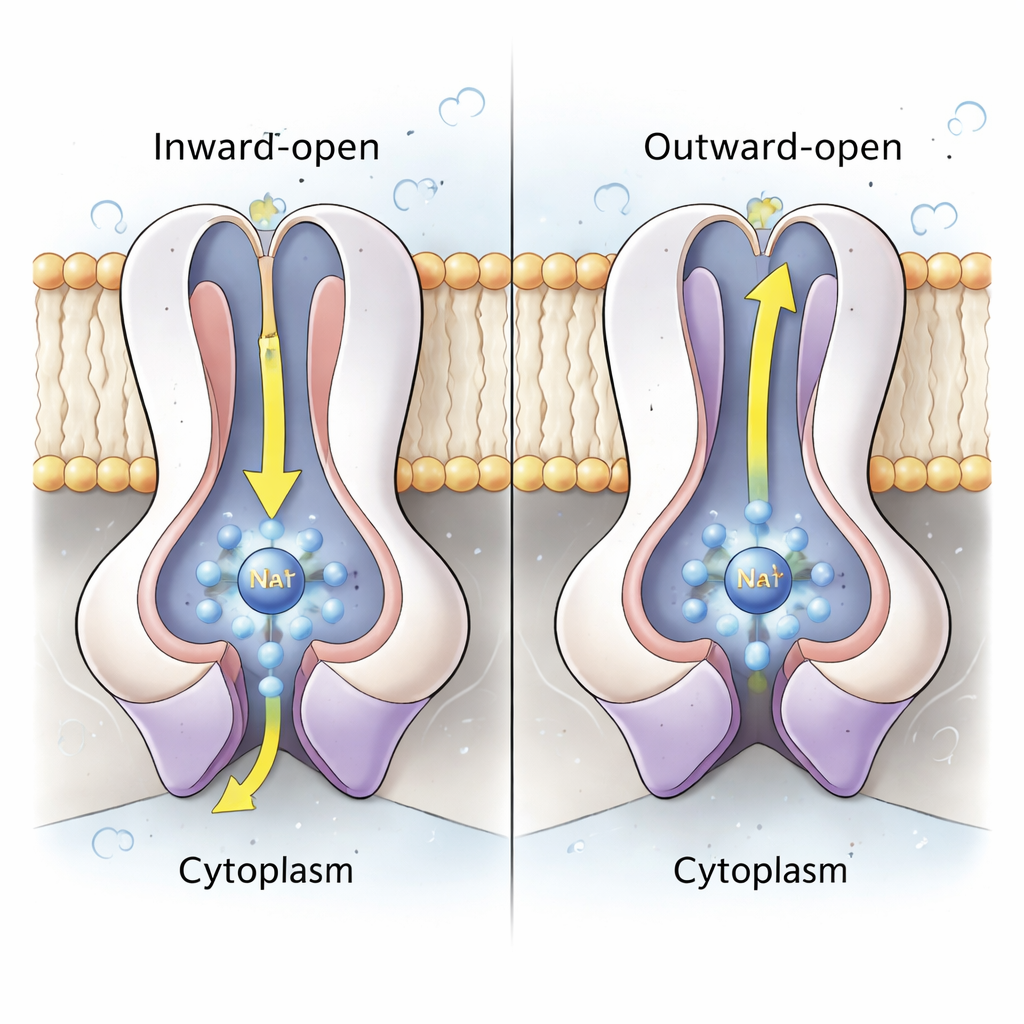
方向性を固定する協調的サイクル
すべての構造状態とシミュレーションを組み合わせて、研究者たちは6段階のサイクルを提案する。まずNADHが結合してNqrFに電子を供与し、NqrFは続いてNqrD/Eへ電子を一つ渡す。この事象が細胞質からのNa⁺取り込みを引き起こし中心ポケットにイオンを装填する。NqrD/Eのコンフォメーション変化が外向き開放形へと進むと、Na⁺はペリプラズムへ放出されると同時にNqrCが電子を受け取る位置へ移動することが促される。その後の段階で電子は最終的なフラビンおよびリボフラビン補因子へと渡り、最終的にキノンへと届く。キノンは還元されてキノールになるために二つの電子を受け取る必要がある。重要なのは、Na⁺を移動させる同じ形の変化がNqrFとNqrCの緩みと強化を交互に引き起こし、Na⁺が外向きにポンピングされる場合にのみ電子の順方向の流れが起こりやすく、逆流を抑えるという点である。この結合が酵素が既存の勾配に逆らってNa⁺を汲み上げ、細菌の「バッテリー」を充電し続けるのに寄与する。
医学と生物学にとっての意義
非専門家から見れば、本研究はタンパク質で精巧に振付けられた機械がどのように構築されるかを示しており、電荷の微小な変化が大きく有用な運動を引き起こすことを示している。感染症研究の観点では、Na⁺-NQRにおけるNa⁺の移動は従来疑われていたNqrBではなく主にNqrD/Eコアを通ることを明確にした。この知見は、ビブリオ・コレラエや他の病原体の動力源を最も効果的に破壊するために将来どこに薬が結合すべきかを絞り込む。より広くは、この研究は酸化還元反応がどのようにイオンポンピングに結び付けられるかの構造的設計図を提供しており、自然が多様な生体エネルギー装置で再利用する設計原理を示している。
引用: Ishikawa-Fukuda, M., Seki, T., Kishikawa, Ji. et al. The redox driven Na+-pumping mechanism in Vibrio cholerae NADH-quinone oxidoreductase relies on dynamic conformational changes. Nat Commun 17, 1394 (2026). https://doi.org/10.1038/s41467-026-69182-w
キーワード: ナトリウムポンプ, 細菌の呼吸, Na+-NQR, クライオ電子顕微鏡, 抗生物質標的