Clear Sky Science · ja
タイプIII‑E CRISPR 核酸分解酵素‑プロテアーゼに基づくRNA応答性ピロトーシスの合成システム
致命的な細胞爆裂を標的ツールに変える
体は時に、感染したり損傷を受けた細胞を炎症性の自己破壊(いわば爆発)によって排除して防御します。この爆発は危険な細胞を取り除くだけでなく、免疫系を呼び寄せます。本研究はDAMAGEと呼ばれる合成遺伝子回路を紹介し、細胞内のRNAメッセージを読み取りその細胞を破壊すべきかどうかを決定できます。微生物の防御機構を我々の細胞死機構につなぐことで、研究者らはウイルス感染細胞、がん細胞、あるいは老化細胞を選択的に消去しつつ健康な隣接細胞を残す方法を示しました。 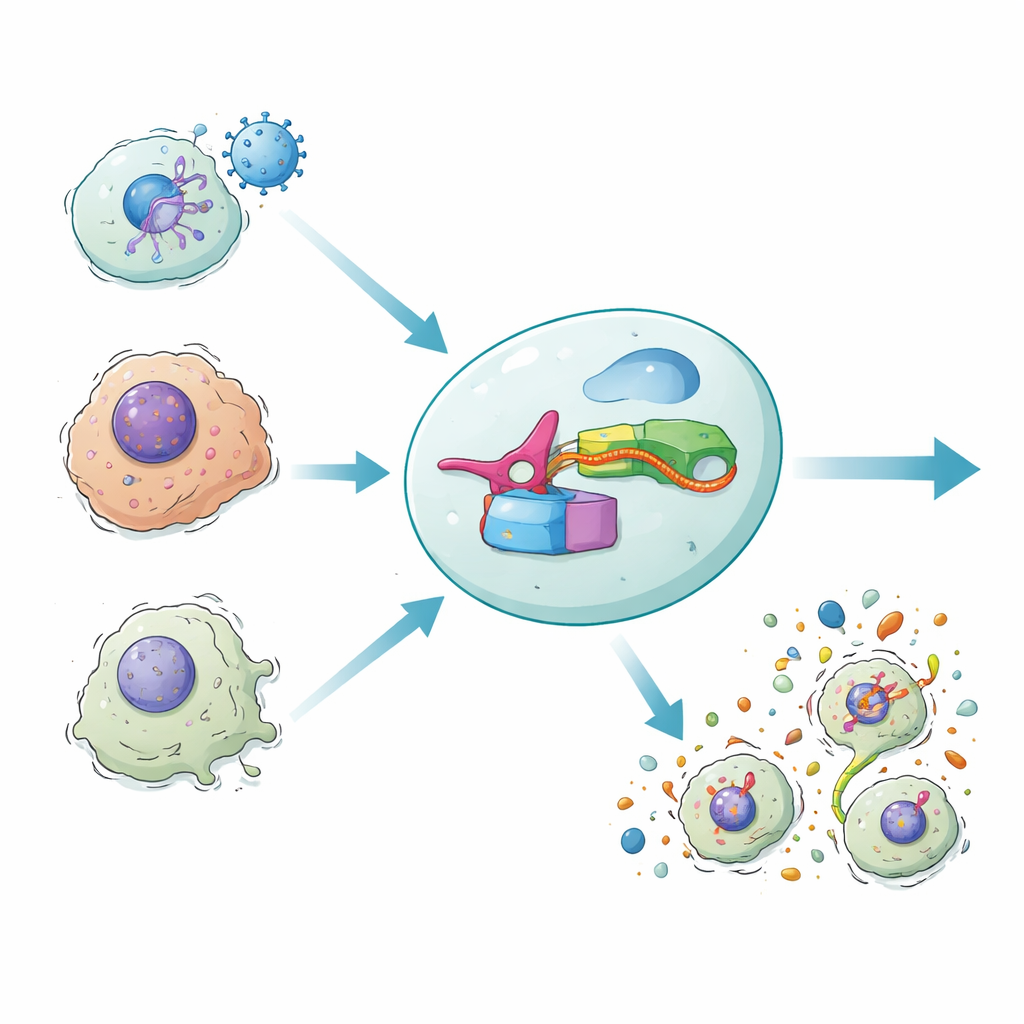
細胞が通常どのように自壊するか
炎症性細胞死では、ガスデルミンと呼ばれるタンパク質群が細胞内に装填された爆薬のように存在します。各ガスデルミンは膜に穴を開ける「キラー」側の前半と、そのキラーを抑える「安全キャップ」側の後半を持ちます。免疫のセンサーが危険を検知すると、酵素がガスデルミンを二つに切断し、前半が膜に孔を組み立てられるようになります。細胞は膨張して破裂し、免疫細胞を呼び寄せる警報シグナルを放出します。この強力な応答は感染や腫瘍と戦うのに有効ですが、その自然の制御ネットワークは絡み合っており治療へ書き換えるのは困難です。
バクテリアの防御を借りてRNAを読む
バクテリアはCRISPR技術で知られるコンパクトな防御モジュールを進化させてきました。その一つ、タイプIII‑EシステムはCas7‑11と呼ばれるタンパク質を用い、短いガイドRNAの助けで特定のRNA配列に結合します。Cas7‑11が標的RNAを見つけると、伴走する酵素Csx29が活性化されてパートナーのCsx30を切断します。著者らはCsx30が任意の二つのタンパク質部位の間にカスタマイズ可能な「蝶番」として働けることに気づきました。彼らはこの蝶番をヒトのガスデルミンのキラー側と安全キャップ側の間に組み込み、CRISPR様センサーが細胞内の選択したRNAを検出したときにのみ分断される人工の実行体を作りました。
病的細胞のためのプログラム可能な死のスイッチ
この設計はDAMAGE(Death Manipulation Gene)と名付けられ、五つの要素で構成されています:Cas7‑11センサー、Csx29切断酵素、ガスデルミン–Csx30融合、ガイドRNA、そして細胞内の標的RNA。適切なRNAメッセージが現れるとCas7‑11がそれに結合してCsx29を活性化し、Csx29が融合タンパク質中のCsx30蝶番を切断します。するとガスデルミンのキラー側が解放されて膜に孔を開け、細胞は炎症性の爆発で死にます。ガイドRNAを変えるだけで研究チームはDAMAGEを別の細胞ターゲットへ向け直しました。呼吸器合胞体ウイルス由来RNA、子宮頸がん細胞中の高リスクヒトパピローマウイルスRNA、さらには通常のRNAと一塩基だけ異なる幾つかのがん駆動KRAS変異RNAを認識することを示しました。いずれの場合も、疑わしいRNAを持つ細胞は選択的に除去され、近傍の対照細胞は無事でした。 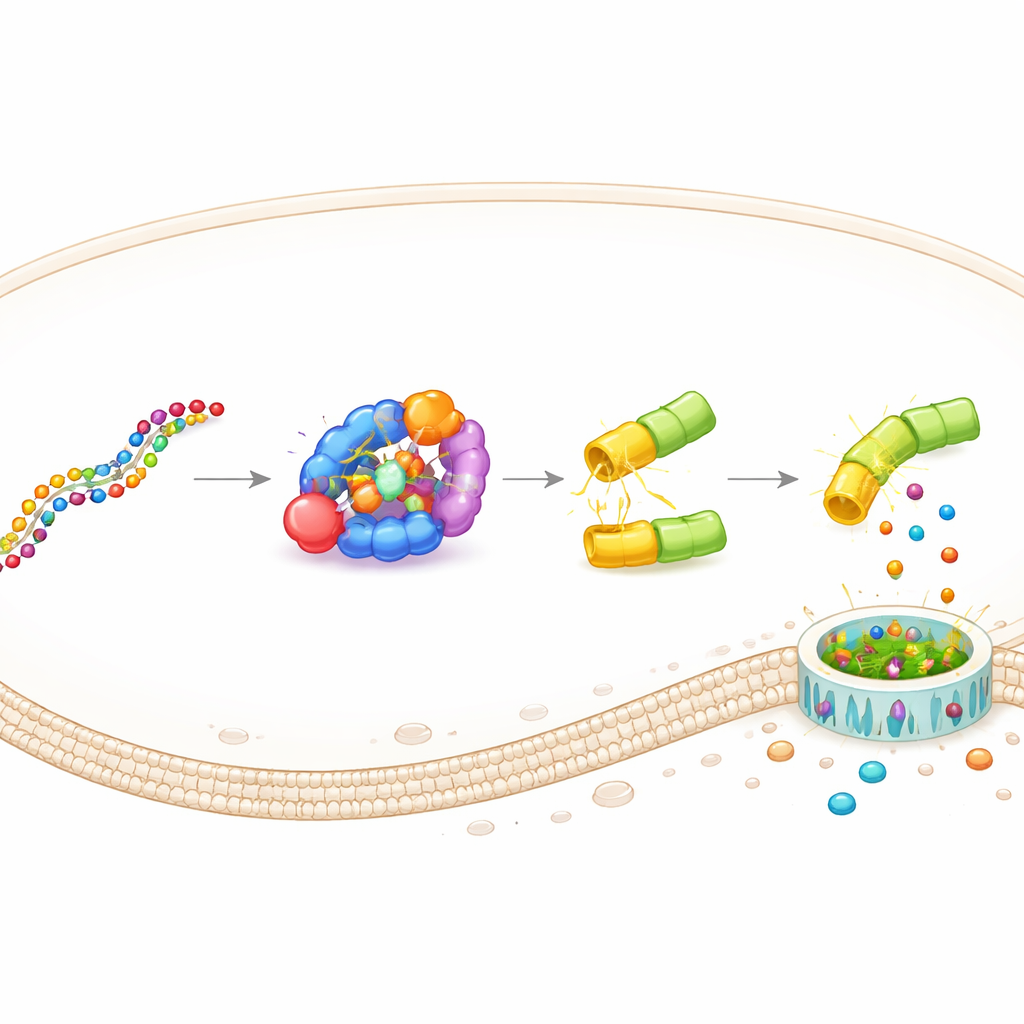
老化細胞に狙いを定める
研究者らはDAMAGEが老化細胞—分裂を止め組織に蓄積して虚弱や慢性疾患に寄与する老化・ストレス細胞—を探索できるかも検討しました。こうした細胞は一般にゲートキーパータンパク質のp16とp21の産生を増やします。p16およびp21のRNAを標的とするガイドを組み込んだバージョン、DAMAGE‑Agingを作成したところ、これらのメッセージが高レベルの細胞を殺し、p16が遺伝的に除去された細胞は生存しており、システムが固定されたDNA変化ではなくリアルタイムのRNA量を読み取っていることを確認しました。p16やp21のレベルを上げる薬剤処理により、細胞はこの標的化された自己破壊に対してより感受性を示しました。
将来の治療のためのパッケージ化
実用化に近づけるため、著者らはDAMAGEの多数のDNAパーツを圧縮して簡略化した構成体DAMAGE‑Plusを作り、これが依然として確実に機能することを示しました。次にこの構成体を合成mRNAへ転写し、COVID‑19ワクチンで用いられるものに似た脂質ナノ粒子に梱包して細胞培養へと導入しました。mRNA版は回路を組み立て標的化された炎症性細胞死をウイルスやがん関連RNAを持つ細胞に誘導することに成功しました。全体としてシステムはまだ大きく細胞株でしか検証されていませんが、プログラム可能なRNA誘導性の細胞殺傷が将来的に注射可能なmRNA製剤で展開され得ることを示唆しています。
細胞内メッセージを読み取り反応する新しい方法
平たく言えば、DAMAGEは分子バウンサーのように各細胞の内部RNA「ID」をチェックし、ウイルス感染、変異保有、あるいは老化といった危険に見えるもののみを爆発的な自己破壊に追い込み排除します。この研究は、細菌由来のRNAセンサーをヒトの細胞死機構に高精度で結び付け、遺伝子メッセージの一塩基差さえ識別できることを実証しました。動物や人に安全に用いるにはまだ多くの工学的課題が残りますが、細胞内の生きたRNAのやり取りを読み取り直接的に生死の決断へ翻訳する強力な新戦略を提示しています。
引用: He, M., Wang, W., Zhou, H. et al. A synthetic system for RNA-responsive pyroptosis based on type III-E CRISPR nuclease-protease. Nat Commun 17, 2565 (2026). https://doi.org/10.1038/s41467-026-69179-5
キーワード: ピロトーシス, CRISPR, RNA標的治療, がん免疫療法, 細胞老化