Clear Sky Science · ja
AlphaFoldによる本質的に無秩序なタンパク質の原子解像度アンサンブル
形を変えるタンパク質が重要な理由
細胞内には単一の剛直な形に落ち着かないタンパク質が数多く存在します。これらの「本質的に無秩序な」タンパク質は、きっちり折りたたまれた機械というよりも柔らかいヌードルのように振る舞いますが、細胞シグナル伝達から神経変性疾患に至るまで多くの過程で中心的役割を担います。常に動き回り柔軟に変形するため、その全ての形を原子レベルでとらえることは極めて難しく、通常は長年の実験と大規模な計算を要します。本稿では、人工知能と物理法則を組み合わせることで、こうした落ち着きのない分子をはるかに効率的に写し取る新しい方法を紹介します。
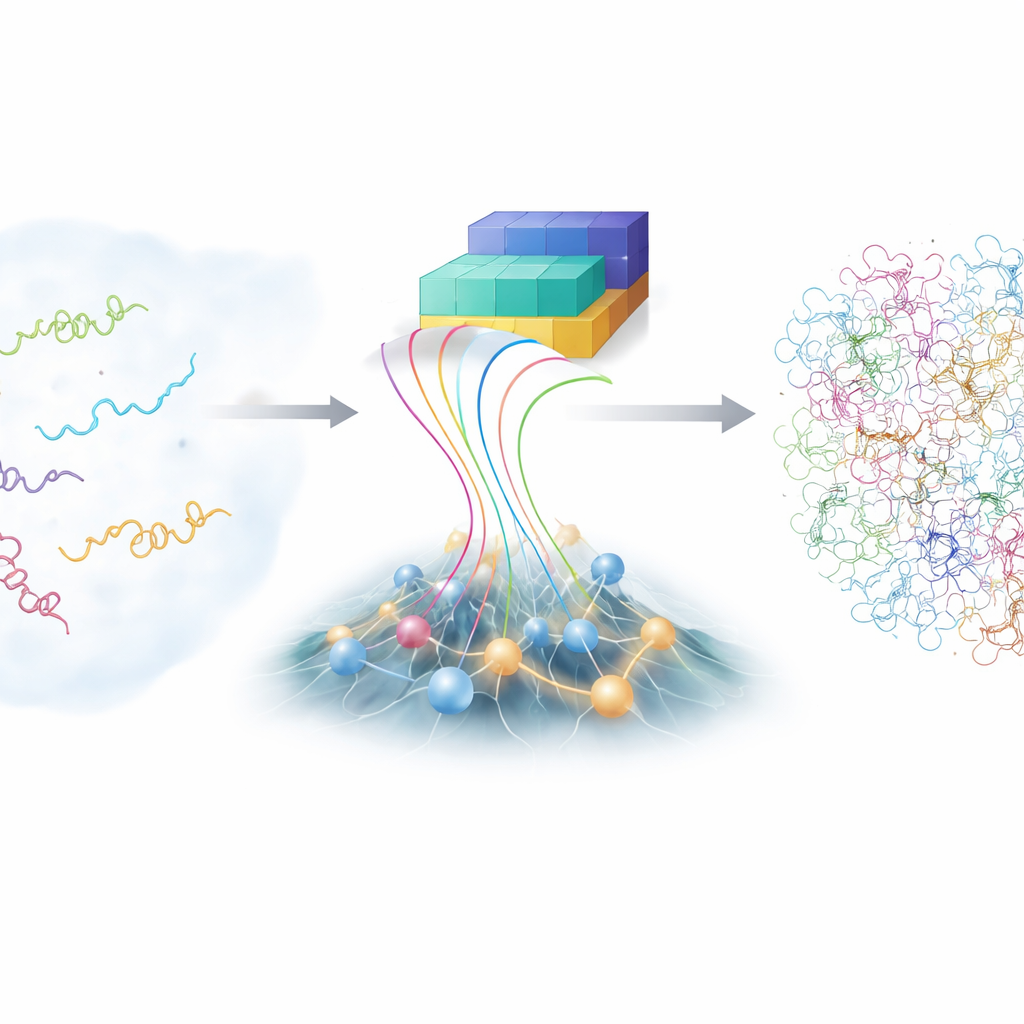
落ち着きのない分子たちの課題
教科書的なタンパク質モデルが示すひとつの整った構造とは異なり、本質的に無秩序なタンパク質(IDP)は膨大な形のランドスケープをさまよいます。その柔軟性は多様な相手を認識するのに役立ちますが、同時に研究を極めて難しくします。高度な核磁気共鳴(NMR)やX線散乱のような従来の実験手法は、多くの形の平均を報告することはできますが、個々の形を特定することはできません。原子レベルのコンピュータシミュレーションなら理論上はIDPのあらゆる原子の挙動を追えるものの、計算コストが非常に高く、精巧に調整された物理モデルに依存します。その結果、正確で詳細なIDPアンサンブルは科学界において限られた蓄積しかありません。
賢い推測と物理法則の融合
近年、AlphaFoldファミリーの深層学習ツールは、アミノ酸配列からタンパク質構造を予測して生物学界を驚かせました。しかし、無秩序タンパク質にとっては、AlphaFoldの強みである「ひとつの最適形を推定する」ことはあまり役に立ちません。IDPには単一の形がないからです。とはいえ、AlphaFoldが提供するのは、鎖の異なる部分が近づくか離れるかの確からしさに関する豊富な情報です。著者らはこのAI由来の情報を柔らかいガイダンスとして扱い、ランダムコイルの視点から出発する高速な物理モデルと組み合わせる新しい枠組みbAIesを構築しました。ランダムコイルでは鎖が特定の構造を好まずあらゆる曲がりやねじれを探索します。
ランダムなもつれから現実的なアンサンブルへ
まず研究者らは、既知の多数のタンパク質構造から抽出した統計に基づき、完全に非構造化されたタンパク質鎖の挙動を再現する効率的な物理モデルを構築しました。このモデルは「事前分布(prior)」として機能し、他に情報がなければIDPがどう動くかの基準を与えます。次にbAIesは、どの残基対が近づきやすいかについてのAlphaFoldの予測を読み取ります。タンパク質を単一のパターンに無理に押し込めるのではなく、これらのヒントを不確かさを組み込んだ穏やかな距離拘束に変換し、鎖がAIの示唆をより広い物理的な状況と矛盾しないときにのみ満たせるようにします。
実験との照合
このアプローチが有効かを確かめるため、チームはほぼ完全なランダムコイルから一時的なヘリックスや複数のドメインをもつより複雑な系まで含む21種類のタンパク質にbAIesを適用しました。それぞれについて、生成されたコンピュータアンサンブルを局所的な詳細と全体の大きさや形状の両方を探る多様な実験測定と比較しました。アルツハイマー関連ペプチドAβ40のように非常に柔らかいタンパク質では、単純なランダムコイルモデルですでに現実に近く、bAIesはこの良好な一致を保持しました。部分的に構造を持つタンパク質では、bAIesは短いヘリカル領域やコンパクトなパッチが現れたり消えたりする位置を正しく捉えて実験との一致を改善しました。重要なのは、AlphaFoldが自信過剰になって溶液実験が示す無秩序の箇所を誤って安定した折りたたみとして予測した場合でも、bAIesがAI入力の誤りを明示的に許容するため堅牢性を保てた点です。
既存手法との比較
著者らは次に、専用のスーパーコンピュータで実行される全原子シミュレーション、タンパク質をビーズに簡略化する粗視化モデル、そしてシミュレーションデータで訓練された新しい深層学習生成器とbAIesを比較しました。複数の試験にわたり、bAIesは実験データの再現において一貫してこれらの手法に匹敵するか上回り、フルスケールのシミュレーションよりもはるかに計算コストが低いことが示されました。また、単純なIDPを超えて、柔軟な連結部でつながれた複数の剛直なドメインをもつタンパク質の扱いや溶液中での全体形状の回復も可能でした。研究者らがさらにbAIesアンサンブルを実験データで微調整すると、一致はさらに向上し、この方法が統合的モデリングの強力な出発点となり得ることが示されました。
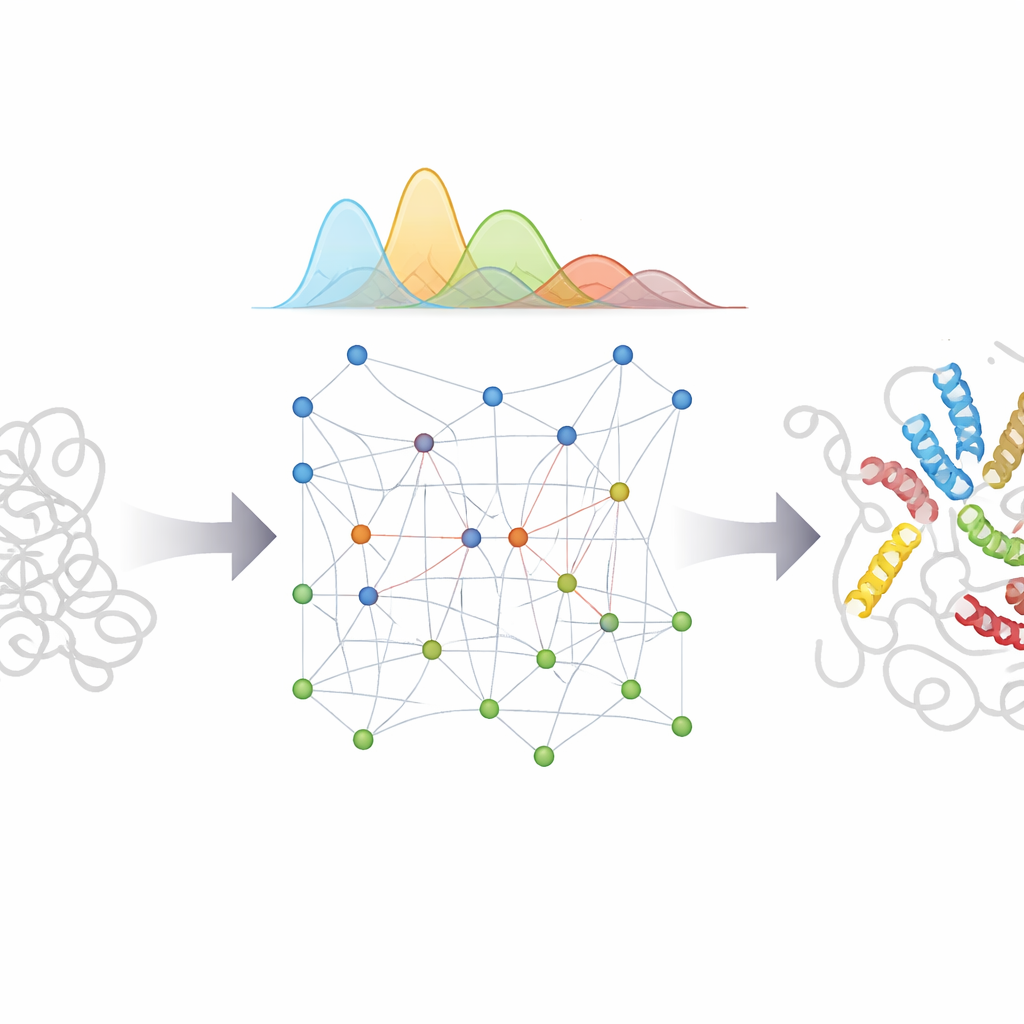
生物学と医学への意義
AlphaFoldのパターン認識力を慎重に設計された物理モデルと不確実性のベイズ的扱いと結びつけることで、bAIesは単一のスナップショットではなく無秩序タンパク質の詳細な「ムービー」を得る実用的な手段を提供します。これらの原子レベルのアンサンブルは、柔軟な領域がどのように相手を認識するか、パーキンソン病やアルツハイマー病などの疾患で誤った折りたたみや凝集がどのように始まるか、そして小分子が捉えどころのない揺らぐ標的にどのように結合するかを理解する助けになります。方法が効率的でオープンソースのソフトウェアとして実装されているため、多くの無秩序タンパク質について現実的なアンサンブルを作成するために広く採用され、実験を導き、単に一つの構造ではなく生命の最も柔軟な分子が取りうる形の全域を予測しようとする将来のAIシステムを支援するでしょう。
引用: Schnapka, V., Morozova, T.I., Sen, S. et al. Atomic resolution ensembles of intrinsically disordered proteins with Alphafold. Nat Commun 17, 2399 (2026). https://doi.org/10.1038/s41467-026-69172-y
キーワード: 本質的に無秩序なタンパク質, AlphaFold, ベイズモデリング, タンパク質アンサンブル, 構造生物学