Clear Sky Science · ja
統合的構造生物学的アプローチが明らかにするR2SP四次シャペロン複合体の動的な構成
細胞はどのようにして複雑な分子機械を組み立てるか
細胞内では多くのタンパク質が単独で働くわけではなく、機能を発揮するために複雑な機械構造に組み合わさる必要があります。この組み立て過程を正しく進めることは、正常な呼吸や運動、さらには生殖にも不可欠です。本論文はそのような組み立ての補助因子の一つ、R2SPと呼ばれる分子の「建設チーム」を取り上げ、その構造と機能を明らかにしています。R2SPを理解することは重要です。なぜなら、その構成要素が障害されると、細胞表面の毛のような繊毛が適切に動かず、慢性的な呼吸器障害などの疾患につながるからです。
細胞の建設チーム:R2TP と R2SP
細胞は、シャペロン複合体と呼ばれる補助タンパク質群に依存して、他のタンパク質が正しい多成分構造に組み合わさるのを導きます。長年研究されてきたチームの一つであるR2TPは多くの組織に存在し、RNA合成装置やDNA損傷センサーといった大型機械の組み立てを助けます。R2SPはR2TPの近縁体で、どちらも二つのパートナータンパク質であるRUVBL1とRUVBL2からなるリング状のモーターを中心に構成され、ATPというエネルギー分子を消費します。相違点はクライアントをモーターに取り込むためのアダプターにあり、R2TPはRPAP3とPIH1D1を使うのに対し、R2SPはSPAG1とPIH1D2を用います。これら部品の小さな違いが、それぞれの複合体のクライアント選択を決め、特にR2SPが粘液や液体を組織表面で掃く運動性繊毛の構築に関与する理由を説明します。
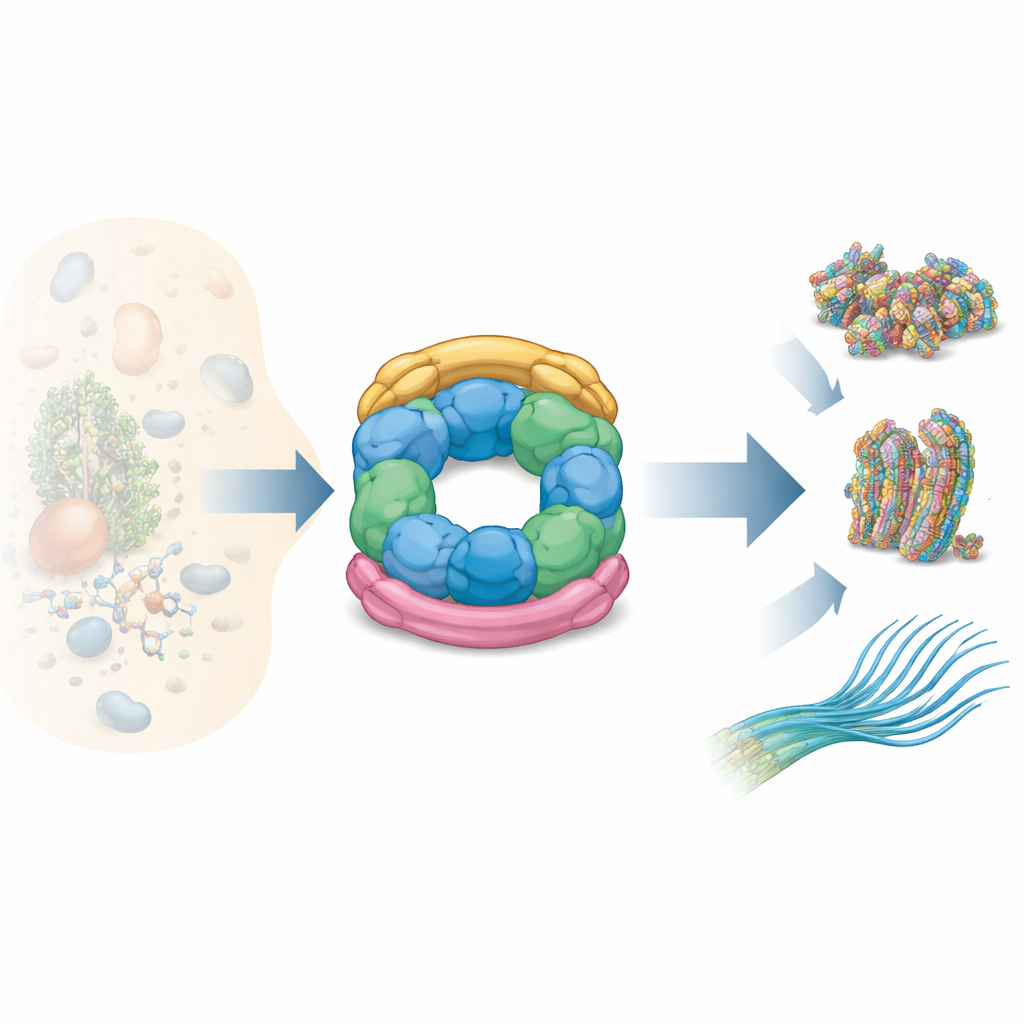
R2SPの部品はどのように組み合わさるか
著者らは核磁気共鳴(NMR)、クライオ電子顕微鏡(cryo‑EM)、架橋質量分析(cross‑linking MS)といった複数の構造手法を、生化学的試験と組み合わせてR2SPの構築様式をマッピングしました。彼らはSPAG1の末端領域がRUVBL1/RUVBL2リングを、R2TPにおけるRPAP3の結合様式に似た形で把持することを示しましたが、形状や接触点に重要な違いがありました。第二のアダプターであるPIH1D2はリングの下に入り込みつつ、モーターの柔軟な側方ドメインにも届きます。これらの側方ドメインはヒンジのように働き、ATPを消費する中心部の動きを結合したクライアントへ伝達する役割を果たします。データはSPAG1とPIH1D2が独立して付着するのではなく協力して動き、上方と下方からリングを挟み込む結合ユニットを形成して、独特の三次元構造を安定化していることを明らかにしました。
ギアを切り替える動的なリング
静止画像にとどまらず、研究チームはR2SPの挙動にも着目しました。相互作用の測定により、RUVBL1/RUVBL2モーターは単一リングまたは積層した二重リングとして存在し得ることがわかりました。SPAG1とPIH1D2が結合すると、この平衡は強く単一リング側へ傾き、最大で三組のアダプターユニットを飾ることができます。同時に、アダプターはモーターのATP加水分解活性を著しく高め、ATPに類似した分子が活性部位に結合・解離する速度も変化させます。R2TPと比較すると、SPAG1とPIH1D2はヌクレオチド放出の過程の異なる段階を有利にし、R2SPが中核モーターのエネルギーサイクルを特有の方法で調整していることを示唆します。この精密に制御されたエネルギー利用が、運動性繊毛に必要なクライアント複合体の段階的な組み立てを駆動していると考えられます。
繊毛構成要素を組み立てるための柔軟なプラットフォーム
すべての構造的制約を単一モデルに統合することで、著者らはR2SPが柔軟で多腕のプラットフォームのように機能すると提案します。SPAG1の尾部はリングの上部にしっかりとアンカーされ、一方でその他の領域やPIH1D2の二つのドメインはモーターのより開いた腕状の側方へ伸びます。この側方はクライアントタンパク質やHSP70、HSP90といったヘルパーシャペロンが結合する最もあり得る場所です。ひとつのリングに最大三つのSPAG1–PIH1D2ユニットが付着し得て、柔軟な腕が絶えず動くため、全体としては触手で複数のクライアント部品を同時につかみ、調整し、より大きな繊毛構造へと渡していくタコのような複合体に似ています。
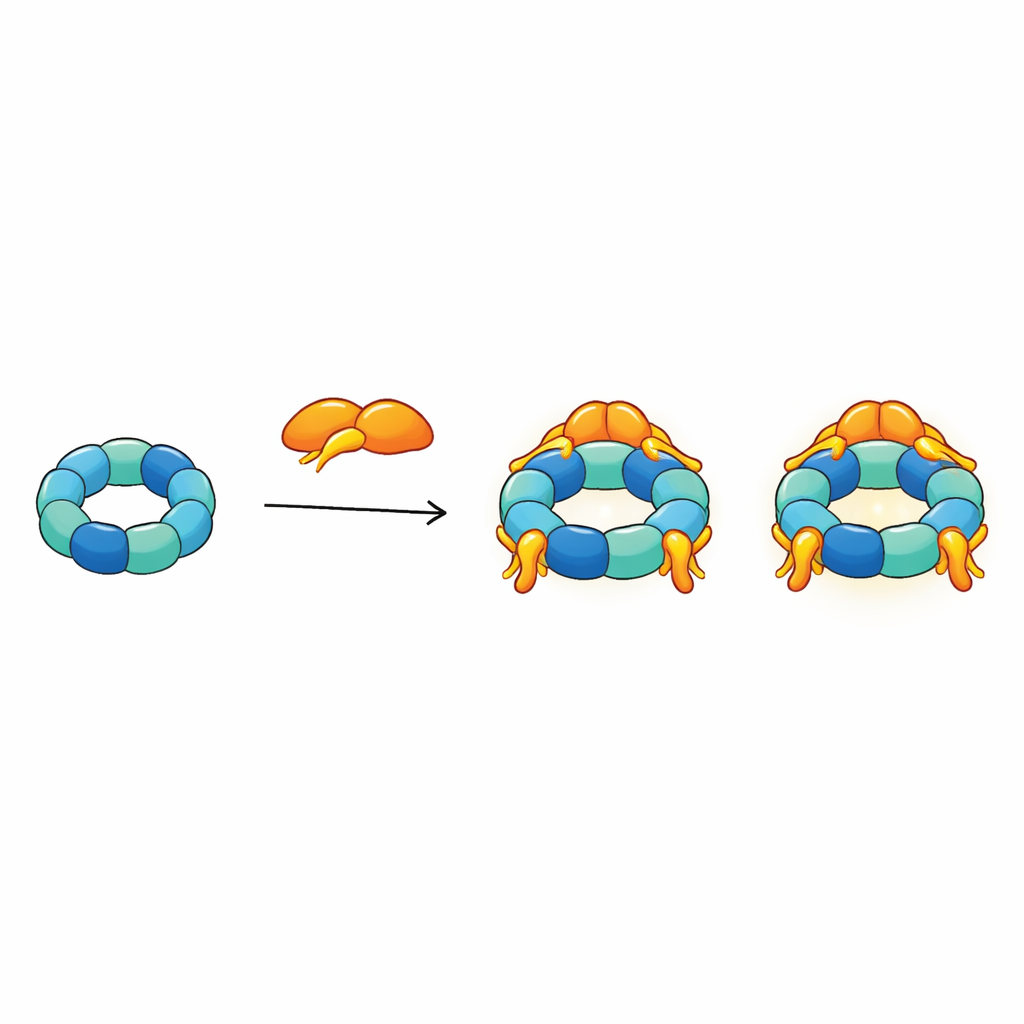
健康と疾患にとっての意義
一般向けの主なメッセージは、R2SPは細胞の一般的な建設機械の専門化バージョンであり、わずか二つのアダプタータンパク質を入れ替えることで再配線されているということです。この入れ替えは中核モーターの制御方法とクライアントの配列を変え、なぜR2SPが運動性繊毛の部品構築に特化し、R2TPが他の細胞工場に機能するのかを説明します。SPAG1の欠陥はすでに原発性繊毛運動不全(原発性線毛運動障害)を引き起こし、慢性の感染症や生殖障害を特徴とすることが知られています。本研究がR2SPの詳細な配置と作動原理を明らかにしたことで、特定の変異がどのように繊毛の組み立てを乱すかを理解する基盤が築かれ、最終的にはこの重要な分子建設チームを回復・調節するための標的化治療の道を開く可能性があります。
引用: Santo, P.E., Chagot, ME., Gizardin-Fredon, H. et al. An integrative structural biology approach reveals the dynamic organization of the R2SP quaternary chaperone complex. Nat Commun 17, 2605 (2026). https://doi.org/10.1038/s41467-026-69157-x
キーワード: 分子シャペロン, タンパク質複合体の組み立て, 運動性繊毛, 構造生物学, RUVBL1 RUVBL2