Clear Sky Science · ja
バクテリオファージT4のポータル–ネック組立中間体のクライオEM構造が明らかにしたウイルスのゲノム保持機構
ウイルスはどのように高圧のDNAを閉じ込めるか
バクテリオファージT4は大腸菌に感染するウイルスで、頭部にDNAを非常に高密度に詰めるため、内部の圧力はシャンパン瓶の中よりも5〜7倍高くなることがあります。それでもウイルスが残りの構造を組み立てる間、DNAは漏れ出しません。本研究は、T4が遺伝物質のためのエアロックのように働く小さな二重ゲートを用いてこの問題をどのように解決しているかを分子レベルで明らかにします。
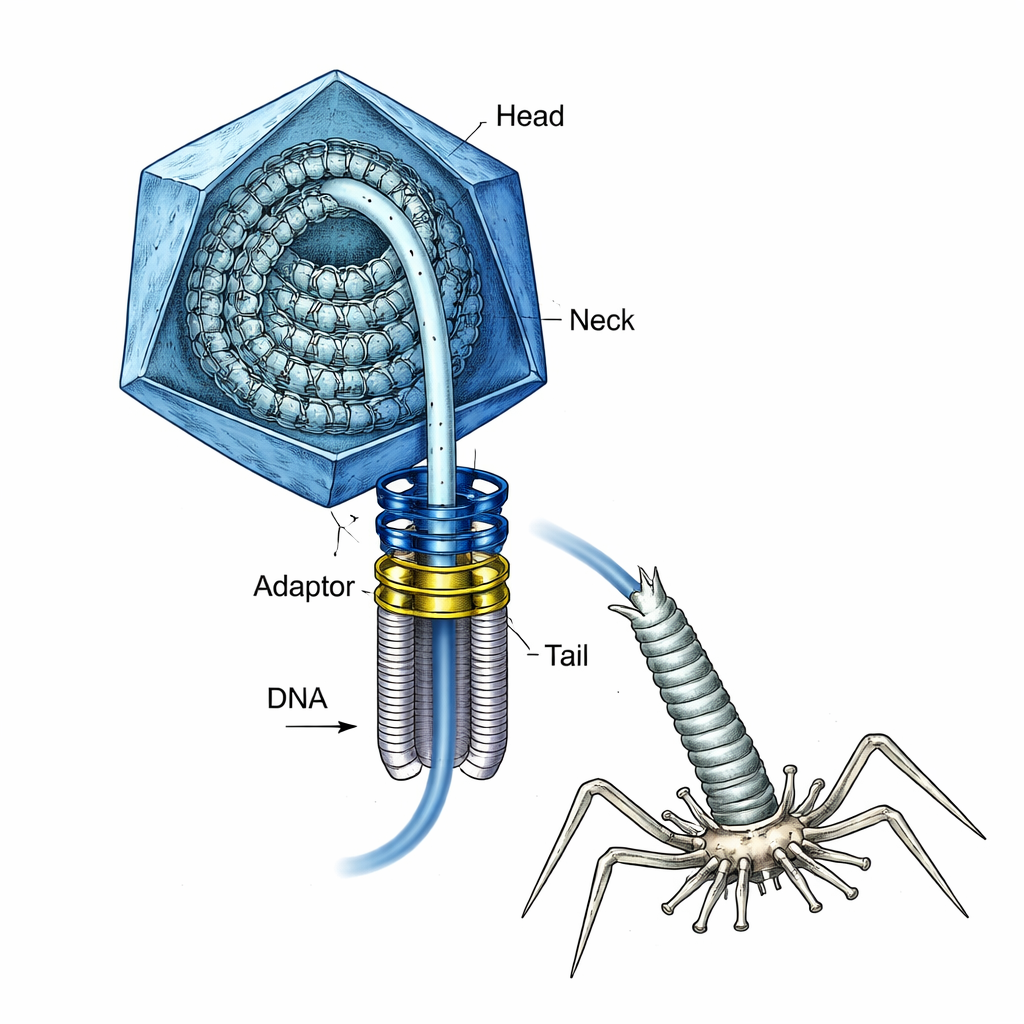
内側に巻かれたバネを持つウイルス
T4は長年分子生物学の実験系として広く使われてきました。また将来のワクチンや遺伝子送達ツール構築のモデルでもあります。組み立ての過程で、ウイルスはまず空のタンパク質殻(頭部)と頂点の一つに環状の「ポータル」を作ります。強力な分子モーターがこのポータルを通してDNAを頭部内に巻き取り、頭部が「満杯」になるまで詰め込みます。その時点でモーターは外れ、ネックと尾部が取り付けられ、後にDNAは細菌に注入されます——いずれの場合も加圧されたDNAが早まって飛び出さないようにしなければなりません。これほどの応力がかかったDNAをこれらの過程の間安全に保持する仕組みは、これまで十分に理解されていませんでした。
試験管内でネックを再構築する
研究者たちはT4の主要な構成要素を大腸菌内で再現し、それらを制御された条件で混ぜ合わせてネック(頭部と尾部をつなぐ連結部)がどのように組み立てられるかを観察しました。gp13とgp14と呼ばれる二つのウイルスタンパク質が別々に産生されました。それぞれ単独では単量体として存在しましたが、共存させると積み重なった環を形成し、DNA通路の中央トンネルを作りました。研究者を驚かせたのは、これらの調製物に第三のタンパク質が繰り返し現れたことです。それは通常大腸菌でRNAや遺伝子活性の制御を助けるよく知られた細菌性タンパク質Hfqでした。質量分析はHfqがgp14に特異的に結合していることを確認し、ウイルスがネックの一部として宿主タンパク質を借用していることを示唆しました。
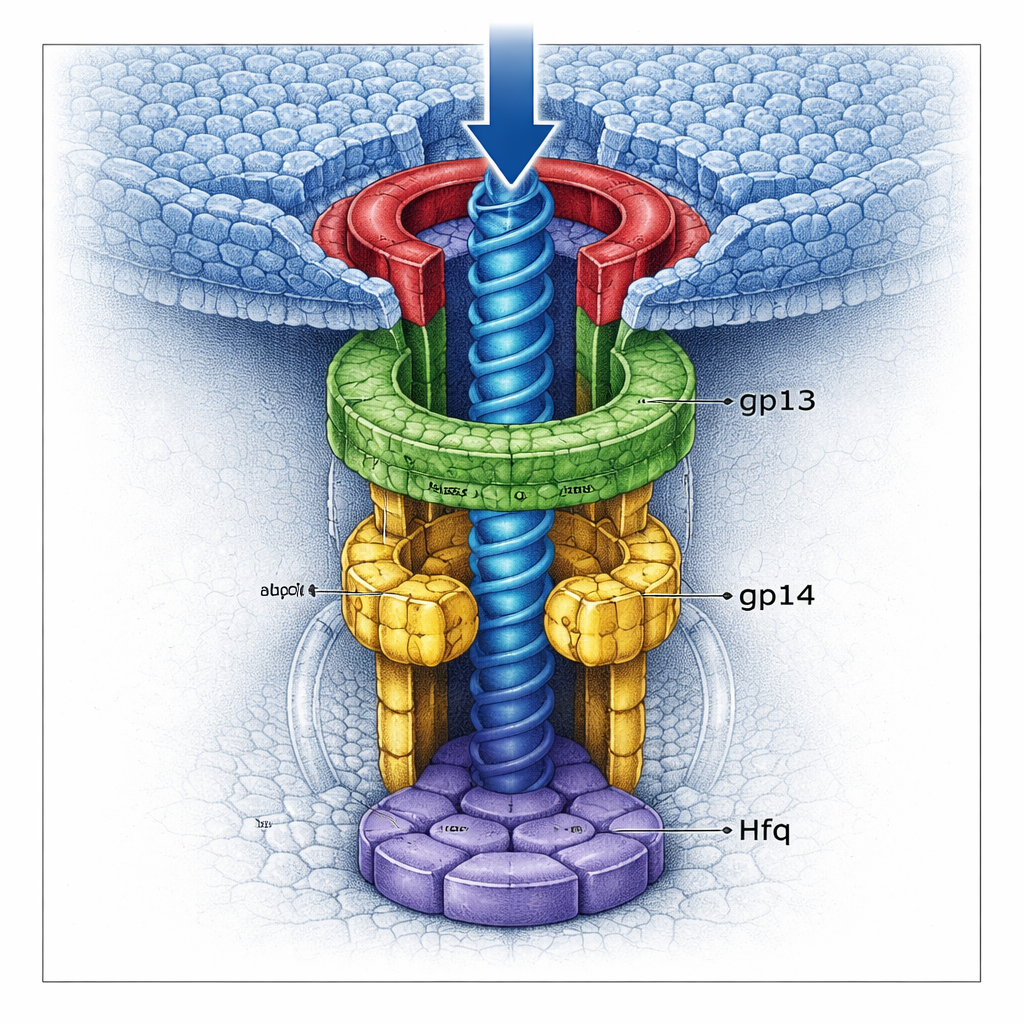
ゲノムをロックする二重のゲート
高分解能のクライオ電子顕微鏡を用いて、チームはネック複合体のいくつかの形態をほぼ原子レベルで可視化しました。gp13はポータルに適応する幅広の環を形成し、gp14はその下に六量体として座り、より狭いチャネルを作っていることが分かりました。重要なのは、各gp14サブユニットが長いループを持ち、それがトンネルの中央に回り込むことです。6つのそのような「ストッパーループ」が集まって、頭部から出ようとする最後のDNA断片を捕えるきついゲートを形成します。gp14の下では、乗っ取られたHfqタンパク質が自身の六量体を組み立て、下側のチャネルを第二の扉のように塞ぎます。Hfqが存在するとgp13–gp14構造はより完全で剛直になり、二つのゲートがトンネルをさらに狭めるため、DNAの漏出ははるかに起こりにくくなります。
タイミング、誤組立防止、そして借用された助っ人
この研究は、このシステムが単なる静的な塞ぎではなく、入念に調整された形状変化の連続であることも示しています。頭部が満杯になると内部圧力がポータルを新しい立体構造へ押し込み、gp13の結合部位を露出させます。あらかじめ組み立てられたgp13–gp14–Hfqネックがポータルにドッキングします。gp13はたわみ、上方に振れ、ポータルと外殻の両方に固定してネックを頭部にしっかりと織り込みます。この段階を通じて、gp14のストッパーループとHfqのプラグがDNAを所定の位置に保持します。Hfqは品質管理因子としての第二の役割も果たします:gp14上の重要な表面を占有することで、gp14が誤った位置でポータルに結合してネックを誤組立てするのを防ぎます。事前に組み立てられた尾部が到着したときにのみ、尾端タンパク質gp15がgp14とさらに強い結合を形成してHfqを押しのけ、尾部への制御されたDNA放出の道を開きます。
一つのウイルスを超えて重要な意味を持つ理由
平たく言えば、T4は二重扉の安全ロックを使って強力なDNAの「バネ」を抑えつつウイルスの残り部分を組み立てます。第一の扉は自身のネックタンパク質gp14で作られ、第二の扉は宿主のHfqタンパク質から一時的に借用され、ウイルスはそれを使った後に捨てます。この二重ゲートによりほとんどDNAが失われず、最終的なウイルスが完全に感染性を持つことが保証されます。多くの大型ウイルスが類似の極端な圧力下でゲノムを詰め、関連する構造を共有していることから、同様のゲーティング機構や宿主タンパク質の一時的な乗っ取りが広く見られる可能性が示唆されます。これらのメカニズムを理解することは、医療向けのより安全なウイルスベクターの設計に役立ち、有害なウイルスのゲノム「ロック」を標的にして阻害する新たな方法を示す可能性があります。
引用: Han, L., Mao, Q., Zhu, J. et al. Cryo-EM structures of bacteriophage T4 portal-neck assembly intermediates reveal a viral genome retention mechanism. Nat Commun 17, 1964 (2026). https://doi.org/10.1038/s41467-026-69107-7
キーワード: バクテリオファージT4, ウイルスの組み立て, クライオ電子顕微鏡, ゲノム包装, 宿主–ウイルス相互作用