Clear Sky Science · ja
マウス網膜を標的とするゲノム編集タンパク質送達剤の開発のための組合せ的合成戦略
遺伝性失明治療への新たな希望
多くの遺伝性失明は、眼の奥の光受容細胞にある単一の欠陥遺伝子から始まります。CRISPRのような現代の遺伝子編集ツールは原理的にはこれらの誤りを修正できますが、編集機構を適切な細胞に安全に届けることが大きな障壁となってきました。本研究では、特別に設計した脂質様粒子を用いて強力な遺伝子編集酵素をマウス網膜に直接運ぶ新しい方法を示しており、遺伝性眼疾患の患者に対する一度の治療で視力を回復する可能性を開きます。
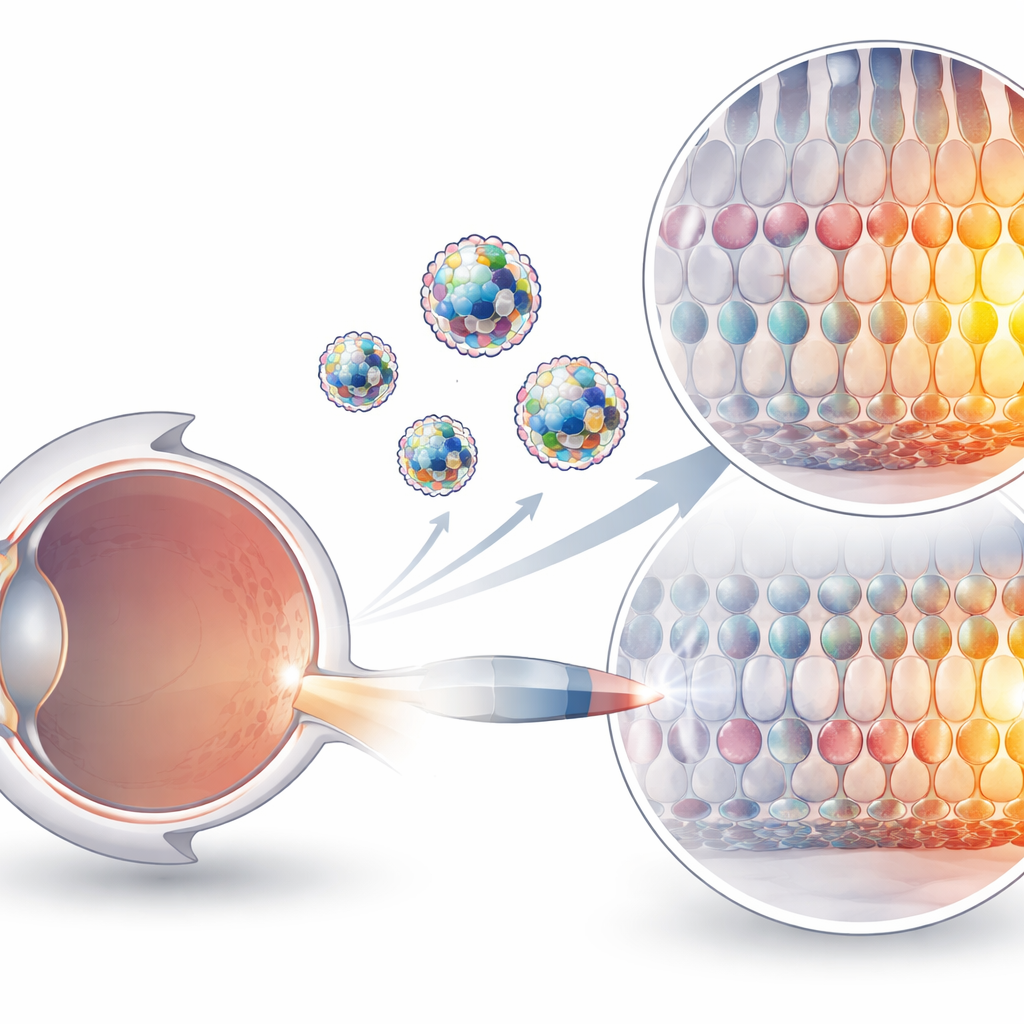
遺伝子編集酵素の送達が難しい理由
CRISPRベースのツールは、二本鎖を切断することなくDNAの個々の塩基を変換できるようになり、遺伝性疾患の治療に魅力的です。しかし、これらは大きく、タンパク質–RNAからなる機械であり、体内では電荷を持ち脆弱です。現在の送達法は主に改変ウイルスや、編集酵素そのものではなく編集酵素の設計図である遺伝情報を運ぶ粒子に依存しています。ウイルスは免疫反応を引き起こす可能性があり容量制限がありますし、メッセンジャーRNA送達は肝臓では非常に効果的ですが、眼を含む多くの他の組織では非効率のままです。事前に組み立てられたタンパク質–RNA複合体を直接注入することは概念的によりクリーンで安全ですが、細胞膜を越えて標的に到達させるための適切な輸送体が欠けていました。
染料に着想を得たタンパク質シャトル
研究者らは予想外の出発点に目を向けました:クマシー・ブリリアント・ブルー(Coomassie Brilliant Blue)、生物学の実験室でよく使われ、一部の眼科手術でも既に承認されている濃青色の染料です。この染料は多くのタンパク質に強く結合します。チームはクマシーの「頭部」と脂質様の「尾部」を化学的に結合させ、リピドイドと呼ばれる新しい分子群を作りました。水中では、これらのリピドイドは油性部分を内側に、クマシー基を外側にしてクラスタを形成し、外側のクマシーがタンパク質を掴むことができます。尾部の長さ、分岐、電荷を変えることで、研究者たちは一方で遺伝子編集タンパク質に結合し、他方で細胞膜と相互作用する候補化合物を数十種類作り上げました。
眼細胞へのタンパク質送達の評価
どの設計が実際に機能するかを確認するため、グループはまずCreリコンビナーゼという単純なテスト用タンパク質を用いました。これは組換え細胞やマウス内で遺伝子スイッチを緑から赤、あるいは赤から緑へと反転させるものです。いくつかのクマシー・リピドイドは培養細胞へCreを効率的に運び、大部分の細胞を緑から赤へと変えました。報告マウスの網膜下に注入すると、選択した化合物は視機能を支える色素上皮層と光を感知する視細胞の両方で顕著な色変化を引き起こし、タンパク質が失明を引き起こす多くの疾患に最も影響する細胞に到達したことを示しました。これらの初期実験はまた、リピドイド構造の微妙な変化が標的となる細胞種を変えることがあり、将来のバージョンで特定の網膜層に合わせて調整できる可能性を示唆しました。
遺伝子編集の強化と視力の回復
次にチームは系にアデニンベースエディター(ABE)を搭載しました。これは、重度の小児性失明モデルであるrd12マウスにおける視力喪失の原因となる特定の一塩基変異を修正できる改良型CRISPRです。編集酵素のタンパク質–RNA複合体単体では細胞内浸透が不十分でした。あるリピドイド、CBB11と名付けられたものは送達を改善しましたが、溶液中で凝集しがちでした。これを安定化させるために、研究者らはCBB11を小さく均一なリポソームに組み込みました—これらはいくつかの脂質成分からなる中空の球で、mRNAワクチンに使われている臨床成分も含まれます。この製剤では、リポソーム表面のCBB11が編集酵素のタンパク質部分を掴み、他の脂質がRNAガイドの結合を助け、複合体全体を粒子外側に保持する協奏的な殻を作り出しました。
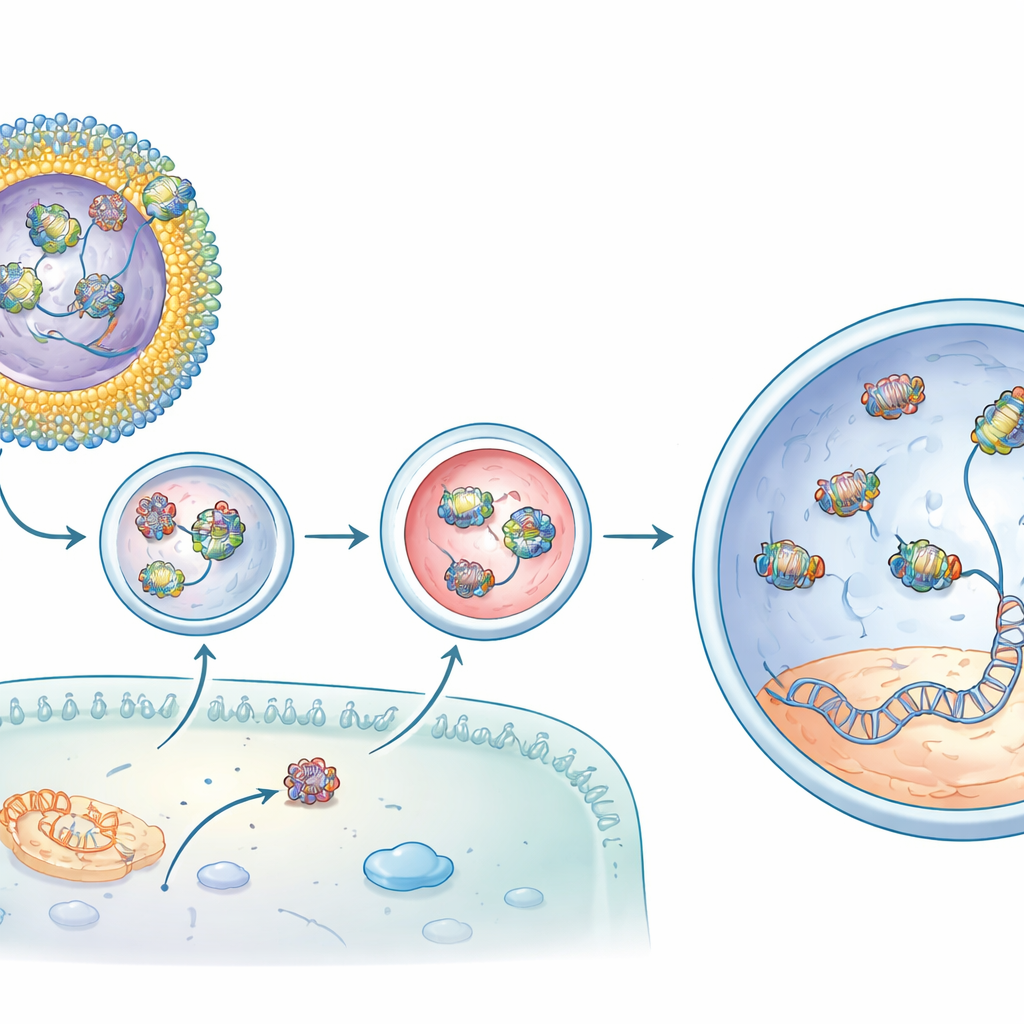
分子修復から回復した光応答へ
CBB11含有リポソームに搭載されたベースエディターをrd12マウスの網膜下に注入すると、結果は劇的でした。エディター単独の注入と比較して、最適化された製剤は標的遺伝子における望ましいDNA修正を一桁以上増加させ、修正されたメッセンジャーRNAの量はさらに高くなりました。化学分析は、疾患で欠損していた光感受性網膜色素の回復を示しました。最も説得力のある所見は、動物の眼からの電気記録で、杆体(ロッド)細胞が薄暗い光に反応する能力をかなり回復し、良好な例では正常なマウスの約3/4に達したことです。ゲノムの他の部位でのオフターゲット変化は背景レベルにとどまり、編集が高効率かつ高精度で行われたことを示唆しました。
将来の眼科治療に示す意味
非専門家にとっての要点は、著者らが生体内の眼で直接機能する再利用可能な「シャトルバス」を構築したことです。ワクチン様の安全な脂質粒子をタンパク質を掴む染料で飾ることで、さまざまな編集酵素を表面で捕捉し、それらを網膜細胞に送達し、病的な変異を修正し、単回投与でマウスの視力を回復させるシステムを作り出しました。安全性の十分な評価、標的化の改善、およびヒトへの適用のための適応など、さらに多くの作業が必要ですが、このプラットフォームは、遺伝性網膜疾患や局所的なDNA修復によって盲目と視力の違いが生じる可能性のある他の遺伝性疾患に対する将来の一回限りの精密医療に向けた道筋を示しています。
引用: Zhang, J., Hołubowicz, R., Smidak, R. et al. A combinatorial synthetic strategy for developing genome-editing protein-delivery agents targeting mouse retina. Nat Commun 17, 2479 (2026). https://doi.org/10.1038/s41467-026-69077-w
キーワード: 網膜遺伝子治療, CRISPRベース編集, リポソーム, タンパク質送達, 遺伝性失明