Clear Sky Science · ja
結腸の空間単一細胞プロテオミクスとマウスモデルがクローン病における二量体IgA分泌形質細胞欠損をミトコンドリア機能不全に結びつける
なぜ腸の抗体がクローン病で重要なのか
クローン病は腸の炎症の激しい増悪で知られますが、症状が顕在化するずっと前から腸を守る免疫系に微妙な変化が生じることがあります。本研究は単純だが重要な問いを投げかけます:寛解期のクローン病患者は、腸内微生物を穏やかに抑えるのに適した種類の抗体を依然として作れているか?患者試料、高解像度の組織プロファイリング、代謝解析、マウスモデルを組み合わせることで、著者らは細胞のエネルギー生産に結びつく、腸の抗体バリアの隠れた脆弱性を明らかにしました。
保護的コーティングが不足している
腸は粘膜に分泌される分泌型IgAと呼ばれる特殊な抗体に依存しています。特に二量体IgAは細菌などの微生物をコーティングして、それらが組織内部に入り込むのではなく表面に留まるように助けます。本研究では、寛解期のクローン病患者と炎症のない対照者から採取した結腸生検、血液、および糞便を調べました。結腸組織内では、クローン病患者はB細胞や抗体産生細胞が増え、IgA関連の遺伝子やタンパク質の発現も高かった。しかし糞便中のIgAを測定すると予想に反して、腸腔内の分泌型IgAは有意に減少していました。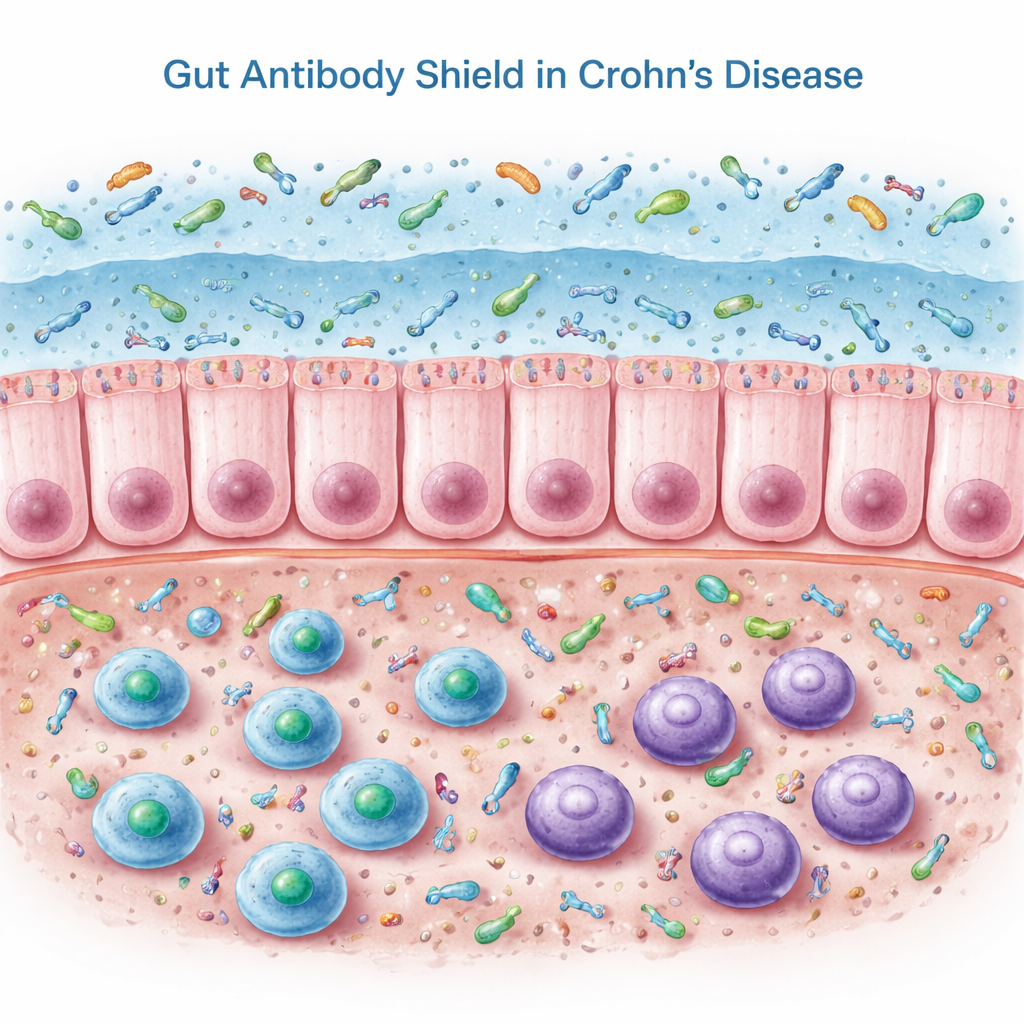
途中で止まる:完全に成熟しない抗体産生細胞
IgAを分泌する細胞である形質細胞は通常、活性化された短命の前駆細胞から、二量体IgAを大量に分泌する長寿で高産出の専門家へと段階的に成熟します。組織を保ったまま個々の細胞上の多数のタンパク質をマッピングする空間単一細胞プロテオミクスを用いて、著者らは結腸内の未熟な形質細胞サブセットと完全に成熟した形質細胞サブセットを区別できました。クローン病患者では初期の形質芽球や未熟な形質細胞が増加し、最も成熟した形質細胞は減少していました。生化学的解析は、結腸における二量体対単量体IgA比が低く、各抗体産生細胞が平均して分泌する二量体IgA量が少ないことを裏付けました。結腸から切り替え記憶B細胞を分離して培養で形質細胞へ誘導すると、クローン病由来の細胞は重要な成熟マーカーを上げられず、総IgAおよび二量体IgAの産生が少なかった(IgG産生は概ね正常のままだった)ことから、IgAを分泌する形質細胞の成熟プログラムに特異的な内在性のブロックがあることが示唆されます。
圧迫されるエネルギー生産工場
このブロックの原因を探るため、研究者らは細胞代謝に注目しました。クローン病組織の形質細胞は細胞表面の酵素でNAD+を消費するCD38の発現が高く、NAD+はミトコンドリアのエネルギー生産に中心的な燃料です。ミトコンドリアの酸化的リン酸化—栄養からATPを生み出す主要経路—に関与する遺伝子群はクローン病の結腸組織で広く下方制御されており、血漿代謝物のパターンも効率的なミトコンドリア呼吸からの移行と一致していました。ex vivo実験では、クローン病由来の形質細胞はグルコース消費が少なく、乳酸の放出も少なく、ミトコンドリアエネルギー遺伝子の発現が低下しており、代謝的に「休止」あるいは弱った状態を示しました。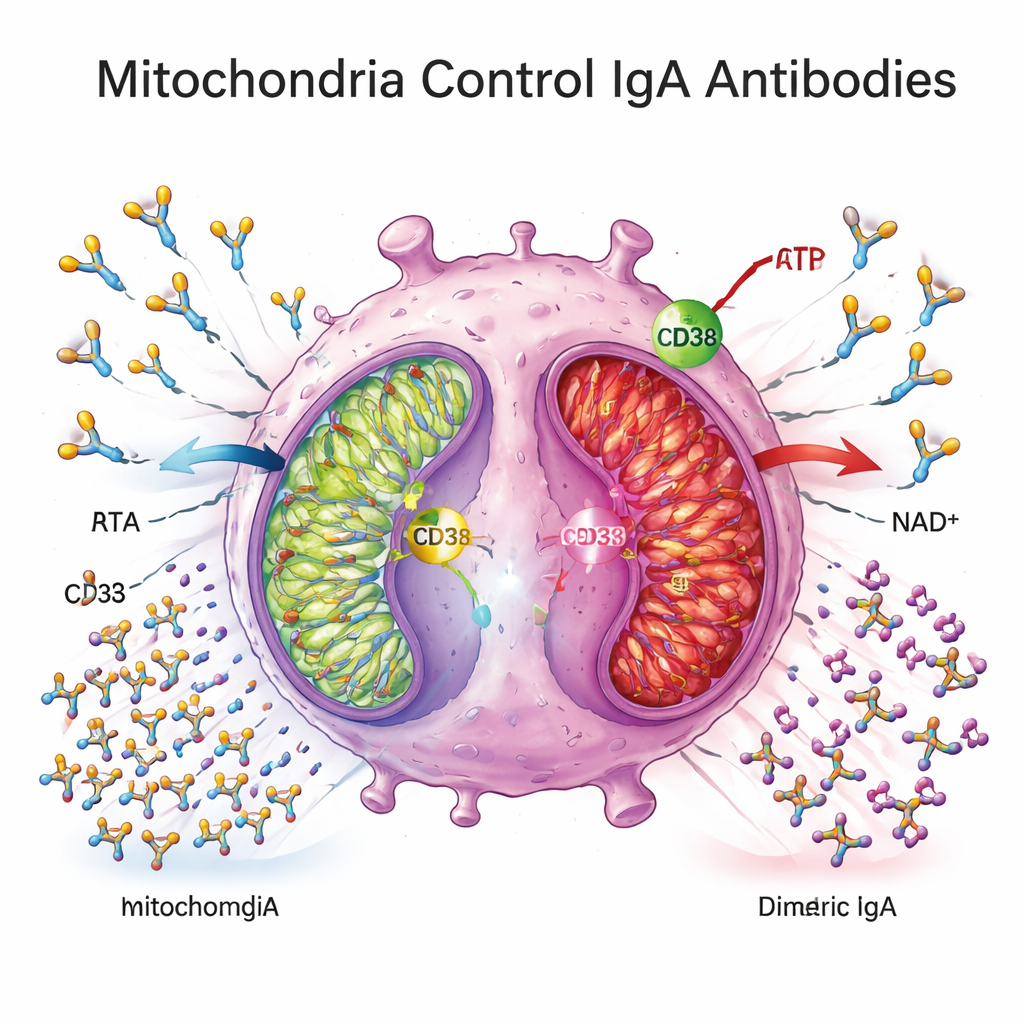
マウスモデルと食餌からの手がかり
マウスモデルもさらなる支持を与えました。ATPを産生する複合体Vを障害する特定のミトコンドリア変異を持つマウスは、腸関連リンパ組織で成熟形質細胞が減少し、結腸での形質細胞マーカー発現が低下し、結腸組織中の単量体および二量体IgAのレベルが低下しました。逆に、結腸でミトコンドリア活性を高めるグルコースフリーの高タンパク食を与えた健康なマウスは、IgA産生細胞が増え、糞便中のIgAが上昇しました。これらの相補的な実験は、ミトコンドリアの性能が形質細胞の成熟と腸内での強固なIgAバリア維持能力に直接結びつくことを示しています。
クローン病患者にとっての意義
総じて、本研究は臨床的寛解期であってもクローン病が結腸における未熟なB系列細胞の過剰と、粘膜中に二量体IgAを分泌する成熟度の高いエネルギー要求の多い形質細胞の不足を伴う像を描きます。腸は外見上は落ち着いて見えるかもしれませんが、その抗体バリアは薄く、効果が低下しています。この欠陥をミトコンドリア機能不全、部分的には高まったCD38活性が駆動している可能性に結びつけることで、細胞のエネルギー代謝を回復させるかCD38シグナルを微調整することを目的とした治療が粘膜のIgAバリアを再構築する助けになるかもしれないことを示唆します。患者にとっては、将来の治療が炎症を抑えるだけでなく、発作を未然に防ぐために腸の第一線抗体防御を強化する可能性を秘めているという展望が開けます。
引用: Raschdorf, A., de Almeida, L.N., Solbach, P. et al. Colonic spatial single-cell proteomics and murine models link mitochondrial dysfunction to dimeric IgA-secreting plasma cell deficiency in Crohn’s disease. Nat Commun 17, 1590 (2026). https://doi.org/10.1038/s41467-026-69069-w
キーワード: クローン病, 腸の抗体, IgA, ミトコンドリア, 腸管免疫