Clear Sky Science · ja
細胞内で抗体インタラクトームを確実に再利用する
抗体を細胞内の小さな道具に変える
抗体は血流中でウイルスやその他の脅威を特異的に狙うことで知られています。しかしアルツハイマー病、パーキンソン病、一部のがんを含む多くの疾患では、主要な病態は細胞の内部で進行し、通常の抗体はそこに到達できないか、うまく働きません。本研究は、既存の抗体を系統的に小型の「イントラボディ」に組み替え、生きたヒト細胞内で安定して機能するようにする方法を示しています。これにより、細胞内部で直接働く新しい診断法、研究ツール、将来的には治療法への道が開かれます。
なぜ通常の抗体は細胞内で苦戦するのか
通常サイズの抗体は、細胞外で働くように進化した大きなY字型タンパク質です。分泌経路で組み立て・化学修飾されたのち血流へ放出されます。細胞内に取り込まれても、通常は細胞質の流動的な内部ではなく分解コンパートメントへ送られます。研究者は抗体を認識領域だけに切り詰めた単鎖可変フラグメント(scFv)として細胞内に発現させ、イントラボディとして用いることができますが、これらはしばしば凝集して不溶化し、標的結合能を失います。これまで、従来の抗体を確実に動作するイントラボディに変える一般的で信頼できるレシピは存在しませんでした。
可溶性イントラボディの設計ルールを見つける
研究者たちはまず、45種類のイントラボディをヒト細胞で発現させたときの可溶性を測定しました。全体の疎水性、予測構造の品質、結合ループの性質といった多くのタンパク質特徴を系統的に比較し、どの因子がイントラボディの可溶性を最もよく説明するかを検討しました。単純な要因が際立ちました:生理学的pH付近での全体の電荷です。強い負の正味電荷を持つイントラボディは可溶性を保ちやすく、中性や正の電荷を持つものは凝集しやすい傾向がありました。AlphaFoldのような高度な構造信頼度スコアなどは可溶性と相関しませんでした。この観察により、イントラボディが細胞抽出液の可溶性画分にどれだけ存在するかを推定する、実用的な電荷ベースのモデルを構築できました。
リンカーとドメインを再設計して挙動を改善する
この知見をもとに、研究チームは標的認識を損なわずに調整可能な特徴に着目しました。鍵となる要素は、二つの可変ドメインをつなぐ短いペプチド「リンカー」です。既存の設計は多くが電荷を変えない中性リンカーを使用していますが、この位置に負に帯電するアミノ酸を導入することでイントラボディの全体電荷を下げ、標的結合を維持しながら可溶性を大幅に改善できました。また、可変ドメインの順序(重鎖側が先か軽鎖側が先か)や、結合ループ外の特定のフレームワーク位置がタンパク質の折りたたみや可溶性に影響することも明らかになりました。より壊れやすい領域を保護するドメイン順序の選択や、慎重に配置した電荷入れ替え変異の導入が性能をさらに向上させました。
人工知能を使って大規模にイントラボディを構築する
個別の試行錯誤を超えるために、著者らは単純な電荷ルールと深層学習に基づく高度なタンパク質設計ソフトを組み合わせました。既知の抗体バックボーンから「逆折りたたみ(inverse folding)」アプローチを用いて、新しい配列を提案させ、望ましい形状を保ちながら表面特性、特に安定性と可溶性を促進する電荷パターンを持たせました。重要な結合ループの変化は制限して認識を保ち、周囲の表面をアルゴリズムが再設計するようにしました。評価の結果、これらAI指導のイントラボディの多くは高度に可溶であるだけでなく、人手設計の変種より熱安定性が高く、変異型SOD1、p53、αシヌクレインなど、神経変性に関連する標的への結合能を維持していました。
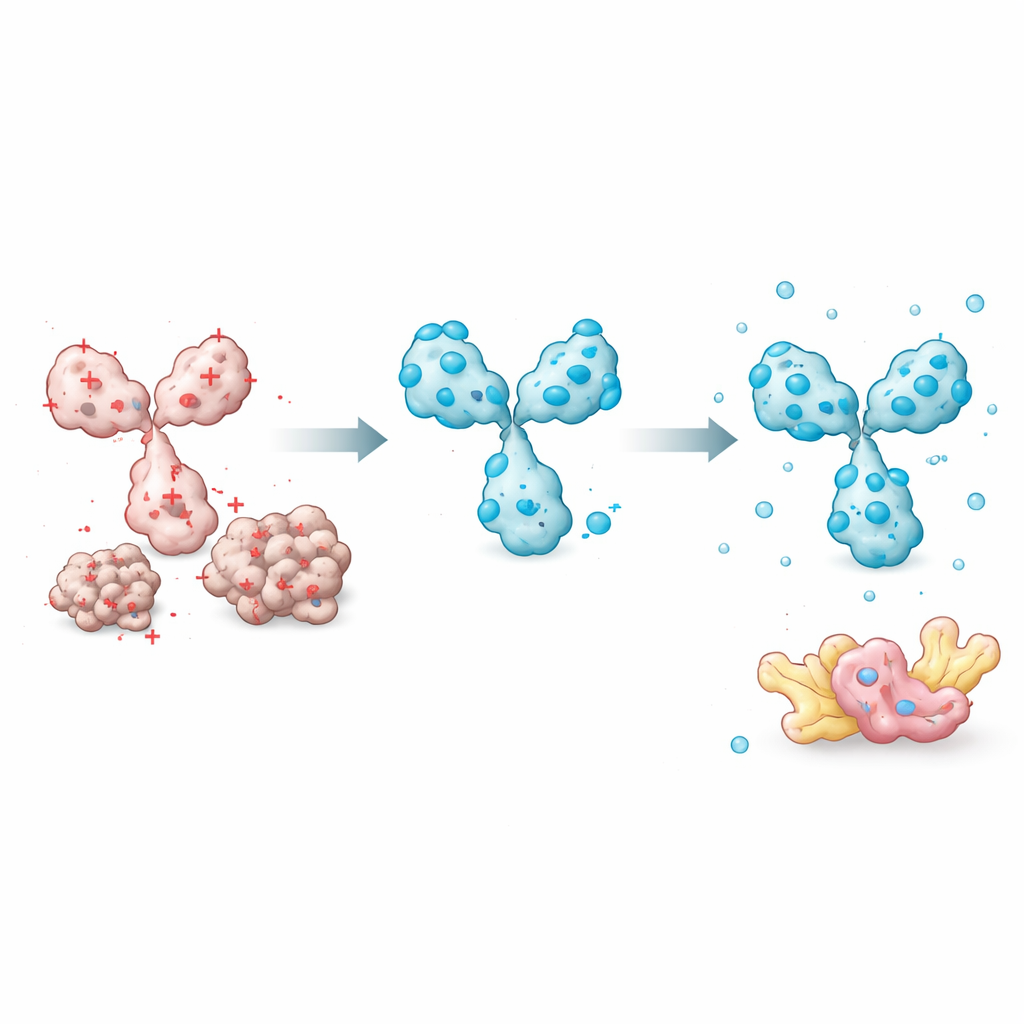
細胞内のタンパク質捕捉体ライブラリを構築する
これらのルールとツールを大規模に適用して、チームは672の抗体を計算的にイントラボディへと再フォーマットし、細胞内でうまく働くと予測される分子を作成しました。これらの設計物は、アルツハイマー病、パーキンソン病、ハンチントン病に関与するタンパク質を含む60以上の異なる細胞内標的を網羅しており、がん関連因子やリン酸化やアセチル化といった翻訳後修飾も対象に入っています。実験では、選択したイントラボディが変異型SOD1や特定の形状のαシヌクレインなど、疾患に関連する特定のタンパク質形態を正常型を無視して効率よく捕捉しました。全配列はオープンに公開され、著者らは同じ電荷ベースのモデルを用いて配列からイントラボディの可溶性を推定できるウェブツールも提供しています。
将来の医薬品と研究への意味
実用的には、この研究は既に臨床で研究されているものも含む膨大な既存抗体コレクションを、細胞内で確実に使えるツールキットへと変換します。単純な設計ルールに従うことで、研究者は初回の試作でうまく機能する可能性の高いイントラボディを作成でき、時間とコストを節約できます。一般の方への要点は、科学者たちが私たちの最良のタンパク質検出器を「配線替え」して、病気の多くが始まる細胞の混雑した内部で機能させる簡便な方法を見つけたということです。これにより、誤った折りたたみや機能不全に起因する疾患を追跡・研究・最終的に治療する新たな手法の開発が加速する可能性があります。
引用: O’Shea, C.M., Shahzad, R., Aghasoleimani, K. et al. Reliable repurposing of the antibody interactome inside the cell. Nat Commun 17, 2222 (2026). https://doi.org/10.1038/s41467-026-69057-0
キーワード: イントラボディ, 抗体工学, タンパク質の可溶性, 神経変性疾患, 生物学における人工知能