Clear Sky Science · ja
スーパー充電増強nDIA-MSにより薬剤誘発性のプロテオーム溶解度シフトをグローバルにプロファイリング
量だけでなくタンパク質の振る舞いが重要な理由
薬剤は細胞が作るタンパク質の量だけでなく、その局在や自由に漂うか細胞構造に付着するかといった存在形式も変え得ます。こうした「どこに」「どう存在するか」の変化はがんや神経変性などの疾患と密接に関連しますが、大規模に測定するのは難しい。本研究は、何千ものヒトタンパク質を一度にスキャンし、溶解度──自由な状態かより凝集した状態か──が二つの広く使われる実験用薬剤に曝露したときにどう変わるかを迅速かつ高感度に調べる手法を示します。
タンパク質をより速く、より鋭く観察する方法
著者らは現代生物学の基礎技術である質量分析法に基づいています。質量分析はペプチド断片の質量と量を測定する手法で、従来法は各タンパク質の量の把握に優れる一方で、DNAへの結合や濃縮体への移行などタンパク質状態の変化を明らかにするのは苦手です。本研究では、狭窓データ非依存取得(nDIA-MS)と呼ばれる質量分析の変法を改良しました。ペプチドを運ぶ液に小さな化学補助剤(スーパー充電試薬)を加えることで断片の電荷を増やし、信号を大きく強化します。
一般的な二つのスーパー充電添加剤、ジメチルスルホキシド(DMSO)とm-ニトロベンジルアルコール(mNBA)を比較したところ、全体の信号増強と検出タンパク質数の面では3%DMSOが最も有効であり、個々のペプチド断片の数と電荷を増やす点ではmNBAが優れていました。最適化した条件では、標準的な細胞消化試料1マイクログラムから15分の走行で約9,600のヒトタンパク質を同定でき、日常実験において驚異的な速度と深度の組み合わせを示します。この性能は、nDIA-MSを単なるタンパク質の定量だけでなく、ストレスに対する物理的状態の応答を探る手段として利用する道を開きます。
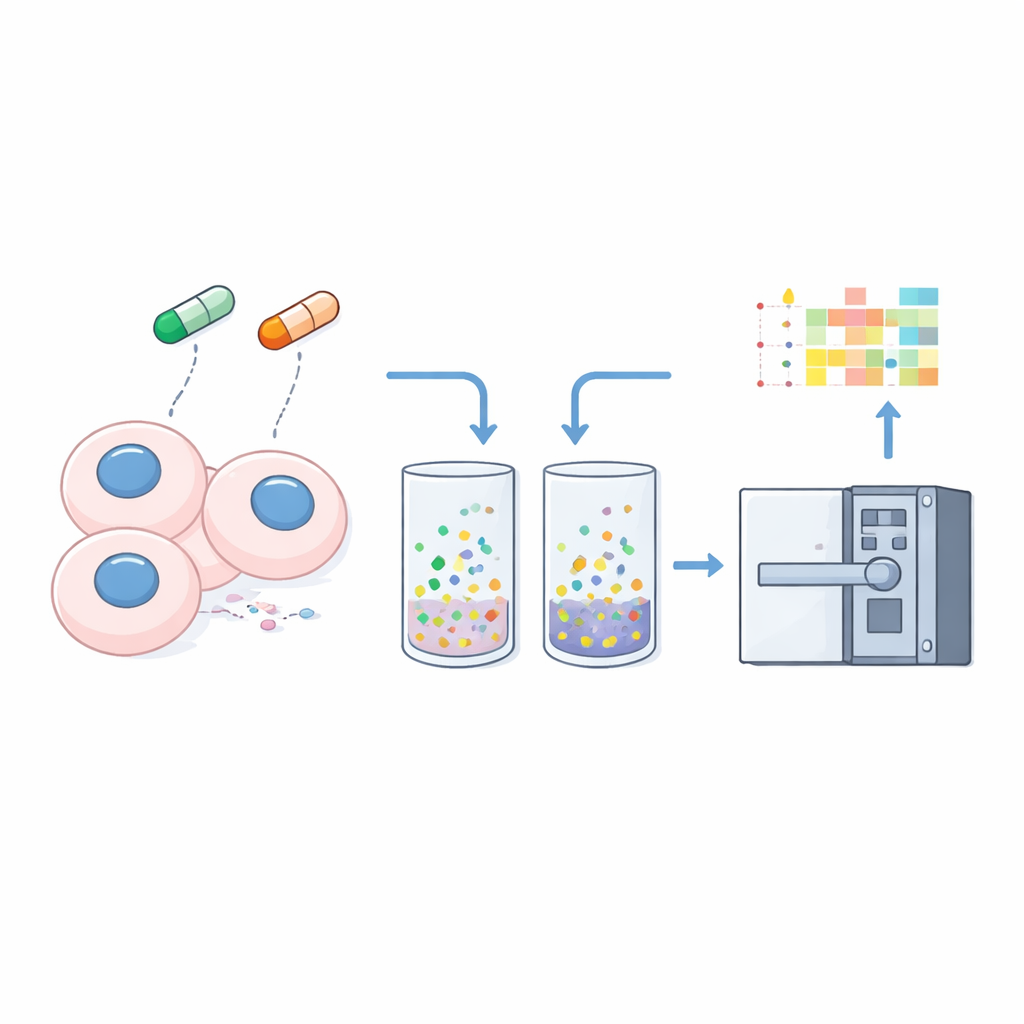
溶解度を細胞変化の可読化へ変える
溶解度を測定可能な指標に変換するために、研究者らは軽い界面活性剤で細胞を穏やかに前処理し、自由に溶けるタンパク質を抽出して、DNAや膜、その他の構造に強く結合した残留物を残します。最適化したnDIA-MS法で細胞全層ライセートとこの「不溶性」ペレットの両方を三つのがん細胞株で解析します。ペレット中の各タンパク質の量を全細胞試料に対する比で比較することで、単純な「不溶性比」を算出します。比率が高いほど細胞構造への強い結合を示し、低いほどより可溶で自由な状態を示唆します。
次に、研究チームは細胞を1時間だけ二つの薬剤、すなわち不要なタンパク質の分解を妨げるプロテアソーム阻害剤MG132と、重要なタンパク質修飾系であるSUMOの活性化を阻害するML‑792に曝露します。この短時間曝露は意図的で、遺伝子発現の変化が完全に進行する前の迅速な初期のタンパク質挙動のシフトを捉えることを狙っています。この短いウィンドウでも、8,694のタンパク質について溶解度と量の変化を定量でき、分画がチューブリンのような古典的な可溶性タンパク質とヒストンのようなクロマチン結合タンパク質をきれいに分けていることを確認できます。
細胞のタンパク質景観を再形成する薬剤
MG132とML‑792は広範だが異なるプロテオーム溶解度の再編を引き起こします。MG132は三つの細胞株で千を超えるタンパク質をより不溶性にし、600以上をより可溶性にします。影響を受ける多くのタンパク質はタンパク質品質管理、DNA損傷応答、遺伝子制御、自食作用(オートファジー)といった交差点に位置します。たとえばプロテアソーム活性化複合体の構成要素や欠陥タンパク質にタグを付けるアダプターは不溶性が増し、分解が阻害されると主要な品質管理因子自身がクロマチンや細胞膜などの構造に捕捉されることを示唆します。オートファジー関連タンパク質や損傷応答の因子、ストレス調節因子HSF1などもより不溶性で凝縮体様の状態へ移行し、核ストレス体の形成と一致します。
一方でML‑792は転写に関与するタンパク質およびSUMO系そのものを強く標的とします。SUMO活性化が阻害されると数百のタンパク質が不溶性または可溶性のいずれかに変化し、コアのSUMOタンパク質は予想どおり可溶性プールに移行します。本研究は印象的な挙動を浮き彫りにします:RNAポリメラーゼIIIのサブユニットは不溶性が増し、核内取り込みやクロマチン結合の変化を示唆します。SP100やDAXXのような核小体に関連する主要な抑制因子はより可溶性になり、SUMO修飾がこれらを隔離するのに役立っていることを示します。両薬剤を単独あるいは連続して適用すると、NAB2、SMAD2、RB1を含むいくつかのタンパク質が協調的あるいは逆向きの溶解度シフトを示し、ユビキチン系とSUMO系という二つのタグ付けシステムがタンパク質局在を制御する際の微妙な相互作用を明らかにします。
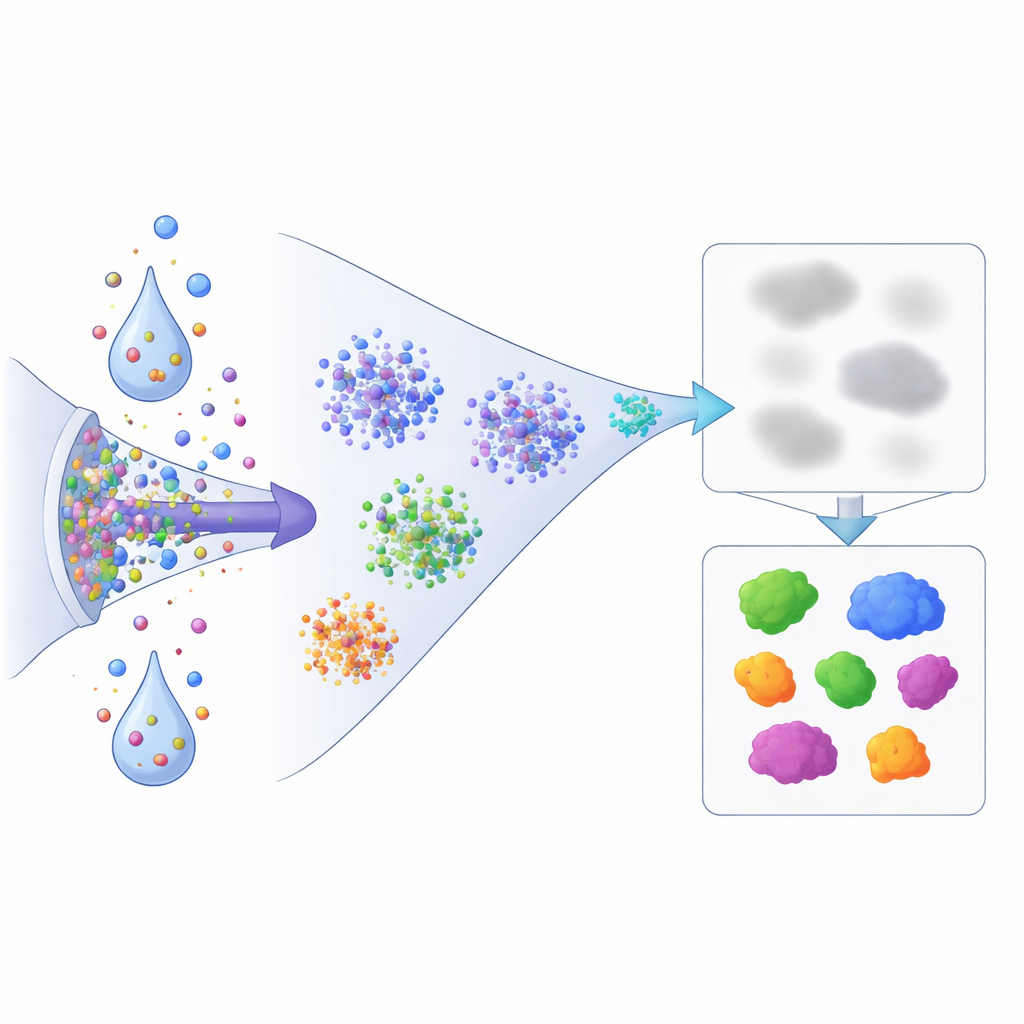
今後の創薬にとっての意義
非専門家にとっての中心的なメッセージは、細胞がストレスを受けたり薬剤処理されたときにタンパク質は単に量が上下するだけでなく、移動し、凝縮し、細胞構造への結び付きの強さを変えるということです。本研究は高速でプロテオーム全体を監視し、そうした変化が起きる様子を観察する手段を提供します。調整した質量分析ワークフローと単純な可溶性対不溶性の比較を組み合わせることで、著者らは一般的な実験薬が内部のタンパク質景観を迅速に再編成することを示し、標準的な量の測定では見逃される現象をとらえます。このアプローチは、候補薬が細胞全体のタンパク質状態をどう変えるかをマッピングする道を開き、予期せぬ標的、ストレス経路、障害点を発見する手助けをし、治療作用や副作用の理解に重要な知見をもたらす可能性があります。
引用: Xiong, Y., Zhang, H., Tan, L. et al. Supercharging-enhanced nDIA-MS enables global profiling of drug-induced proteome solubility shifts. Nat Commun 17, 2350 (2026). https://doi.org/10.1038/s41467-026-69025-8
キーワード: プロテオーム溶解度, 質量分析法, プロテアソーム阻害剤 MG132, SUMO化阻害剤 ML-792, タンパク質状態の遷移