Clear Sky Science · ja
コア–シェル型脂質ナノ粒子の内部構造を設計することでmRNAのエンドソーム放出が効率化される
なぜこの新しいデリバリー技術が重要なのか
COVID-19ワクチンから実験的ながん治療まで、多くの注目すべき新薬はメッセンジャーRNA(mRNA)を基盤にしています。しかし厄介な問題があります:これらの脆弱な鎖が細胞内に入ると、多くは小さな袋状の構造であるエンドソームに捕らえられ破壊されてしまいます。本研究は、mRNAを運ぶ小さな脂質の泡、すなわち脂質ナノ粒子の内部構造を巧妙に再設計することを紹介します。内部を固い金のコアを中心に再編成することで、研究者らは細胞の作業空間(タンパク質を実際に合成できる場所)へ逃れられるmRNAの割合を劇的に改善しました。
小さな運び手により良い体の設計を与える
現在のmRNAワクチンや治療法は、mRNAを包む脂質の混合物からなる柔らかい塊状の粒子に主に依拠しています。本来、これらの粒子に含まれる「イオナイザブル(可イオン化性)」脂質はエンドソーム内部の酸性環境で正に帯電し、エンドソーム膜を裂いてmRNAを解放するはずです。実際には、mRNAの負の電荷がこの効果の多くを打ち消してしまい、投与されたmRNAのうちタンパク質合成機構に到達するのは約2%にすぎません。著者らは単純だが強力な問いを投げかけました:脂質の化学を変えるだけでなく、粒子の内部構造を再設計してmRNAと脂質が互いにどこに位置するかを制御したらどうか、ということです。
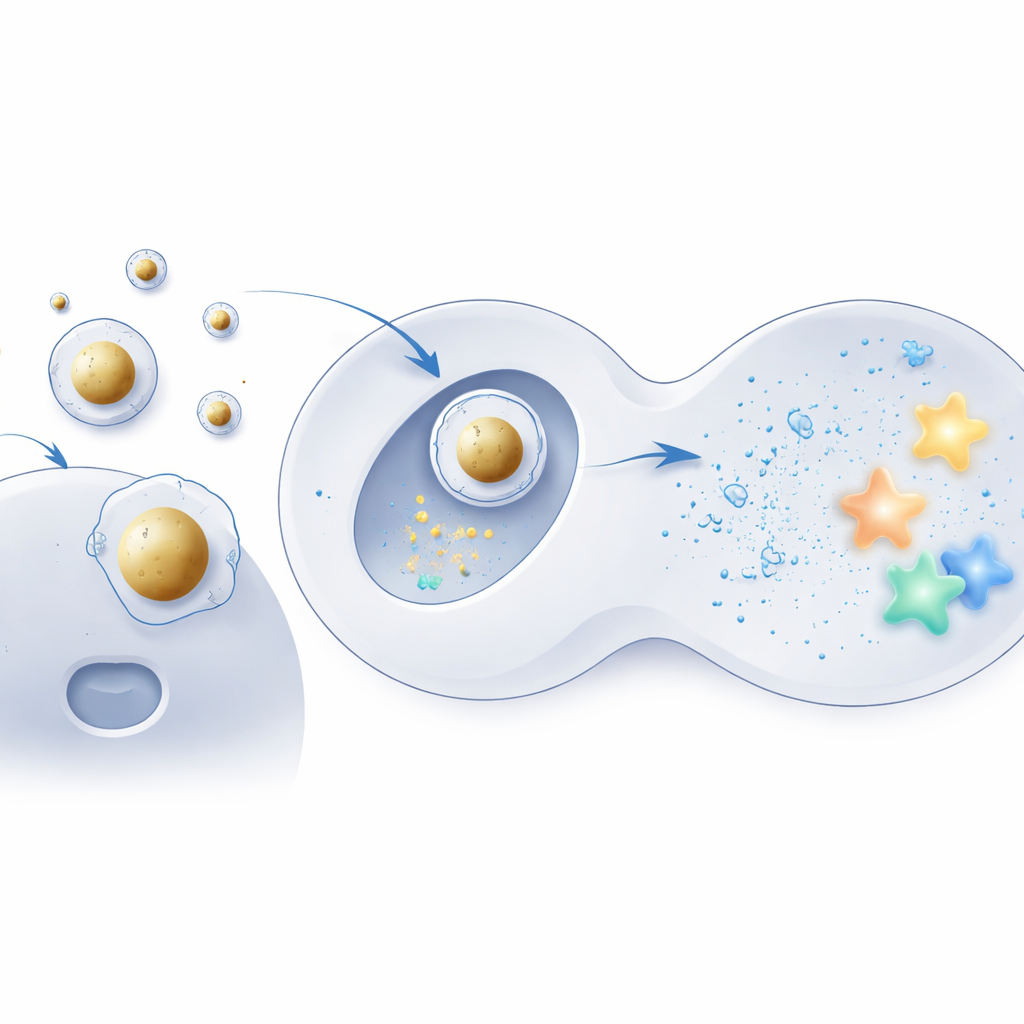
金を中心に据えたデリバリー殻を構築する
このアイデアを検証するために、研究チームは剛直なコアとして微小な金球を用い、従来の処方で使われるイオナイザブル脂質で被覆しました。負に帯電したmRNAはまずこれらのコアに凝縮され、その後に補助脂質や安定化分子の馴染みある混合物で包まれて秩序あるコア–シェル構造が作られました。電子顕微鏡観察と計算シミュレーションは、これらの「Au‑LNPs」が非常に均一で熱力学的に安定し、水性かつ生体に近い条件で形状をよく保つことを示しました。重要なのは、全体の脂質組成は標準的な粒子と同じままであり、変化の本質は成分ではなく内部構造であることが分離された点です。
再配列された内部がどのように脱出を高めるか
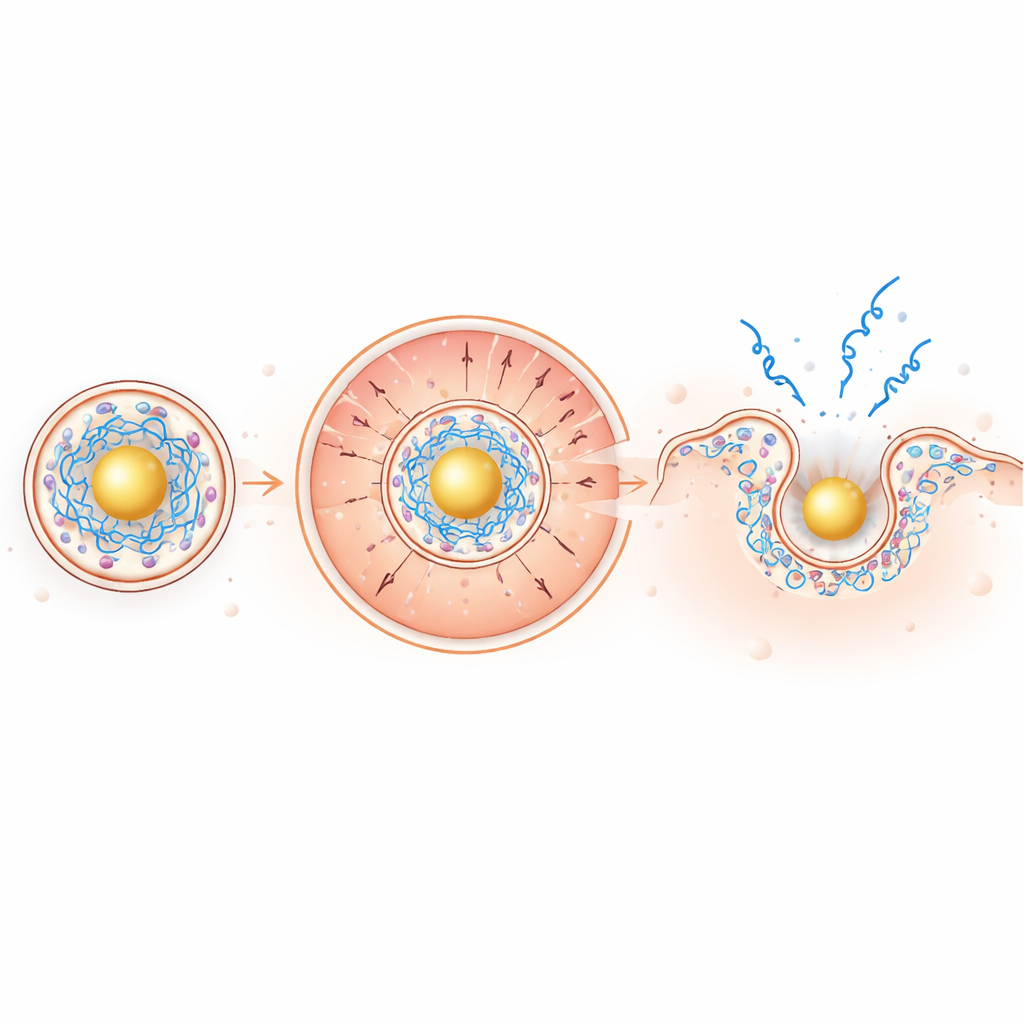
軽度に酸性のエンドソーム環境では、金を基盤としたコアが強く正に帯電し、負に帯電したmRNAを内側へ引きつける一方で、正に帯電するイオナイザブル脂質を外側へ、周囲の膜に向かって押し出します。この電荷駆動の分離は膜を破壊する脂質をまさに必要な場所に集めます。モデル膜試験や赤血球での実験では、新しい粒子は低pHで膜を穿孔する効果が高く、中性pHでは穏やかに振る舞うことが示され、安全性という面で望ましい特性でした。生細胞内では、蛍光標識されたmRNAのイメージングにより、エンドソーム脱出が約2倍に増加し、さらに細胞質内でmRNAが広がる範囲は従来粒子と比べて驚くべき約100倍に増えていました。
培養からマウスへ:より強いシグナルとより強い防御
これらの物理的優位性は生物学的な利得に結びつきました。複数の細胞種にわたり、金コア粒子は標準的な処方よりも遥かに高いレベルのレポータタンパク質産生を駆動し、特に低用量で顕著でした。マウスでは、筋肉や静脈への注射後にmRNA誘導タンパク質の出力が最大で5〜7倍向上し、粒子の体内分布が変わることはありませんでした。SARS‑CoV‑2スパイクmRNAワクチンの送達に用いると、再設計された粒子は初回接種後の抗体レベルを概ね2倍にし、ブースター後にはさらに増強し、ウイルス中和能の高い抗体も多く生み出しました。難治性のトリプルネガティブ乳がんモデルでは、新粒子で運ばれたmRNAワクチンが腫瘍をより効果的に縮小し、腫瘍活動の指標を低下させ、顕著に生存期間を延長しました。
安全性と将来の薬への道筋
コアに金を使っているにもかかわらず、これらの粒子はマウスでよく耐容されるように見えました。体重、炎症マーカー、組織検査に重大な毒性は示されず、臓器中の金レベルは2日以内に基準値へ戻っていきました。著者らは金は主に概念実証の足場として用いられたに過ぎず、同じ内部設計原理は他の安全なまたは生分解性の材料にも応用できると強調しています。専門外の読者への中心的なメッセージは、mRNAを何で包むかと同じくらい、キャリア内部にどのように詰めるかが重要になり得る、ということです。脂質ナノ粒子により規律ある内部配列を与えることで、本研究はmRNAデリバリーの長年のボトルネックを克服する新たな手法を提示し、感染症、がん、その他の分野におけるより効果的なワクチンや治療法の実現に道を開きます。
引用: Li, T., Zhang, J., Guo, J. et al. Engineered internal architecture of core-shell lipid nanoparticles promotes efficient mRNA endosomal release. Nat Commun 17, 2187 (2026). https://doi.org/10.1038/s41467-026-69017-8
キーワード: mRNAデリバリー, 脂質ナノ粒子, エンドソーム脱出, ナノ医療, RNAワクチン