Clear Sky Science · ja
細胞外マトリックスが三重陰性乳がんの転移における循環腫瘍細胞のクラスター形成を仲介する
血流中で悪性乳がん細胞はどう結束するか
乳がんが広がる際、多くの場合は遊離したがん細胞が血流に入り、離れた臓器で新たな腫瘍の種をまきます。本研究は一見単純だが重要な問いを投げかけます:通常の“粘着剤”を失った最も攻撃的ながん細胞が、なぜなおも緊密なクラスターとして移動できるのか、そしてそれがなぜ致死性を高めるのか?
従来の細胞接着に代わる粘着性の糖被膜
研究者たちは、CTC(循環腫瘍細胞)を多く血中に放出することの多い、特に侵襲性の高い三重陰性乳がん(TNBC)に注目しました。多くのがんで、CTCのクラスターは単独の細胞よりもはるかに転移を起こしやすいことが知られています。通常、こうしたクラスターは上皮細胞接着装置(近接する細胞間を分子のリベットのようにつなぐ特別なタンパク複合体)で保たれます。しかしTNBC細胞はしばしばこれらの接着タンパク質を失うため、接着剤がないのにクラスターを維持できるという矛盾が生じます。大型のがん遺伝子データベースを解析したところ、TNBC腫瘍では細胞の外側骨格にあたる細胞外マトリックスに関わる遺伝子群が豊富であることが分かりました。中でもHAS2という遺伝子は、細胞を被う長い糖性ポリマーであるヒアルロン酸(HA)を合成する酵素を作ります。高いHAS2およびHAの発現は、侵襲性や転移能と強く関連していました。
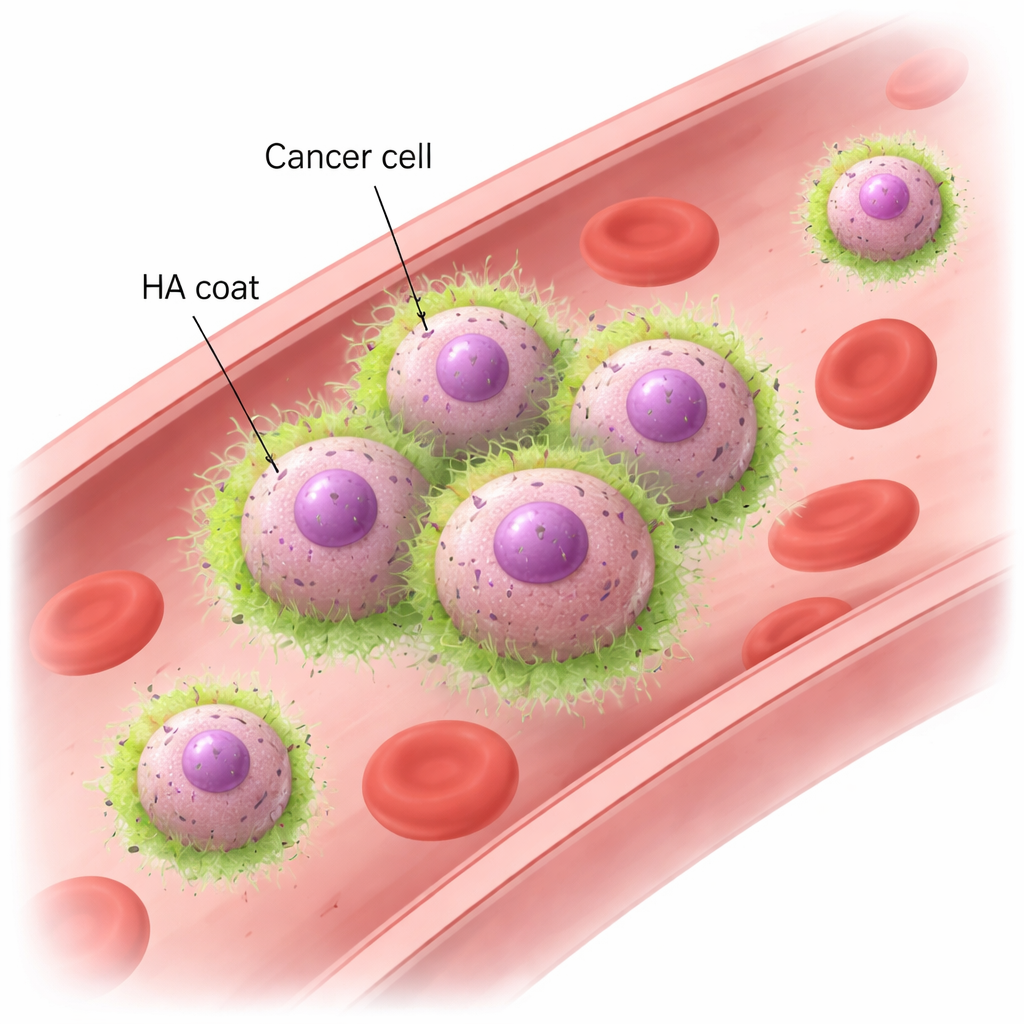
ヒアルロン酸とCD44:細胞が“手をつなぐ”新しい仕組み
マウスモデルとヒト乳がん細胞株を用いて、研究チームは、転移性TNBC細胞が血流を模したせん断流にさらされると急速にクラスターを形成することを示しました。これらのクラスターは実際の血管で生じるほどの力にも耐えられる一方、侵襲性の低い乳がん細胞は崩れて単独で漂います。顕微鏡観察では、転移性細胞はHAの“被膜”に包まれており、細胞どうしが接触する場所に特に高濃度で存在することが示されました。HAを分解する酵素で取り除くかHAS2を抑えると、静置した場合には一緒に沈降できても、流れの下ではクラスター化する能力を失いました。細胞側の主要な相手はHAを結合する表面受容体CD44です。CD44がない細胞は表面にHAを保持できず、クラスターを作ることができませんでした。逆に、クラスター化しない細胞にHAS2とCD44の両方を導入すると、強固なクラスター形成能を獲得しました。これらの実験は、HAとCD44の相互作用が、速い血流中でがん細胞を結びつけるために必要かつ十分であることを示しています。
微小突起と機械的ロックが強固なクラスターを作る
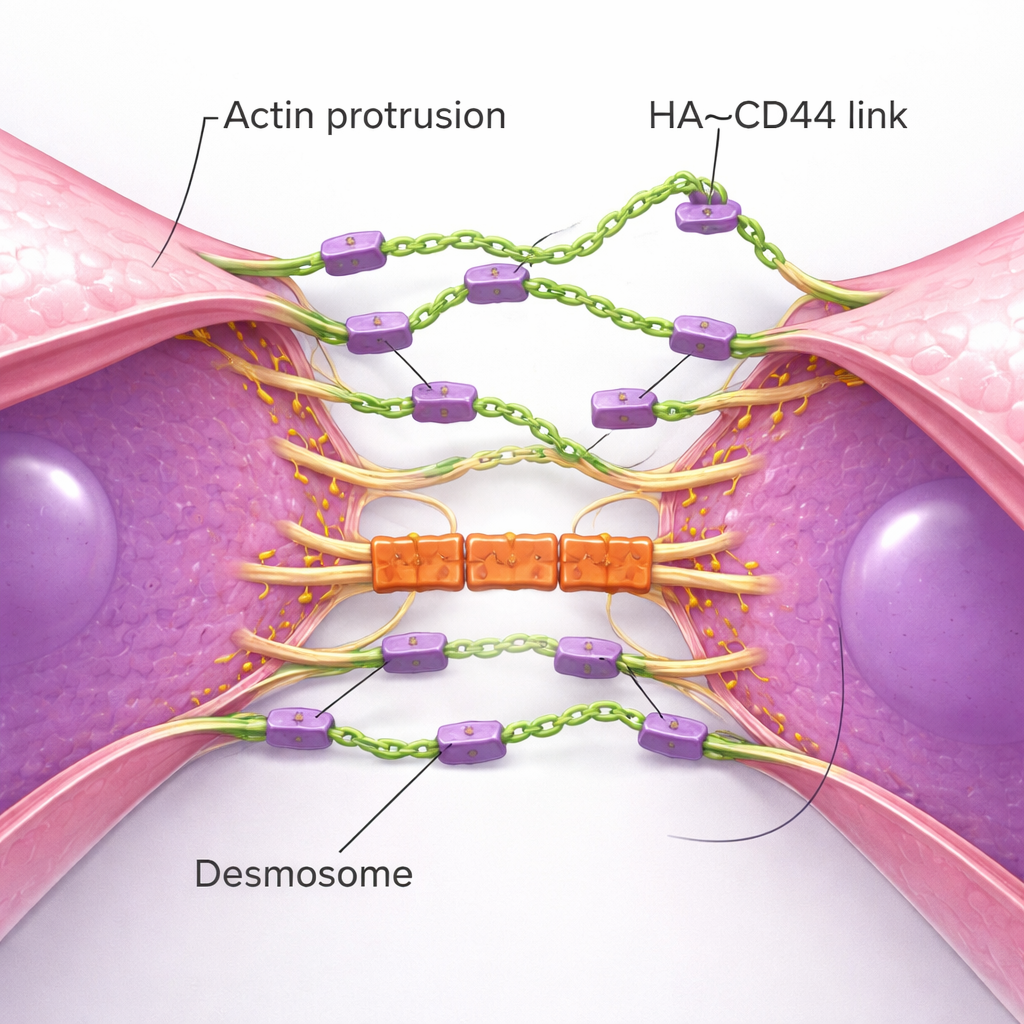
高解像度イメージングはクラスター形成の物理的な舞台裏を明らかにしました。単独のTNBC細胞は多数の細いアクチン依存の膜突起(触手のようなもの)を伸ばし、そこにCD44が散在し先端にHAを備えています。二つの細胞が近づくと、まずこれらの触手同士が接触し、初期のHA–CD44橋を形成します。時間が経つにつれ、突起は互いに沿って滑り、細胞体全体を引き寄せて膜の広い領域がほぼ並置するまでになります。この過程は正常な上皮細胞が接着装置を組み立てる様子に似ていますが、ここでは硬いタンパク鎖ではなく柔軟な糖の被膜が駆動役を果たします。接触域が成熟すると、別の構造群が加わります:デスモソームと呼ばれる堅牢な接合体で、細胞膜を内部骨格に結びつけます。デスモソームタンパクはHAベースの接触が確立した後に蓄積し、血流の引き剥がし力に対抗する機械的“ロック”として作用します。デスモソーム成分を減らすと、クラスターは形成されてもより高いせん断応力で崩壊しました。
クラスター化が生存と転移に与える影響
HAベースのクラスター化システムは単に一緒にいる手段以上のもので、直接的に生存率を高めていました。長時間にわたる模擬血流下で、HAに富むクラスターは有害な活性酸素種のレベルがはるかに低く、HAを失った単独細胞に比べて細胞死が大幅に少なかったのです。マウスモデルでは、HAS2を欠くTNBC細胞は産生されるCTCが大幅に少なく、形成されるクラスターは小さく、肺転移は劇的に減少しましたが、原発腫瘍の成長自体は同程度でした。対照およびHAS2欠損の細胞で予め形成したクラスターをマウスに注入すると、HAに乏しい細胞は肺への定着に成功する確率がはるかに低かったです。さらに、HA被膜をもつCTCは、HAを持たないがん細胞や好中球などの正常な免疫細胞を、CD44を発現していれば混合クラスターへ“勧誘”することができました。転移性TNBCの患者の血液サンプルでも同様のパターンが観察され、CTCはしばしばHA被膜をもち、腫瘍細胞間および腫瘍と非腫瘍細胞の接触点でHAが濃縮していました。
患者と将来の治療にとっての意義
専門外の読者への要点は、最も致死的な乳がん細胞の一部は単独で移動するのではなく、小さく協力的なチームとして移動し、その結束は正常組織にある従来の細胞間“リベット”ではなく、糖性の外被とそれを受け取る受容体によって保たれている、ということです。このHA–CD44に基づく機構は、血流という過酷な環境で細胞の生存を助け、互いに、あるいは支持的な血中細胞と連携し、離れた臓器でより効率よく新たな腫瘍を種まきします。HA産生(例えばHAS2の阻害)を標的にするか、HAとCD44の相互作用を遮断することは、理論的にはこれらのクラスターを弱め、TNBCの転移を抑える手段となりうるため、抗転移治療の新たな方針を示唆します。
引用: Bobkov, G.O., Patel, K.J., Lege, B.M. et al. Extracellular matrix mediates circulating tumor cell clustering in triple-negative breast cancer metastasis. Nat Commun 17, 1352 (2026). https://doi.org/10.1038/s41467-026-69007-w
キーワード: 三重陰性乳がん, 循環腫瘍細胞, ヒアルロン酸, CD44, 転移