Clear Sky Science · ja
共有結合阻害剤の設計によりGDP結合型およびGTP結合型の両方のKRAS G12Cに対する活性を付与
将来のがん治療にとってなぜ重要か
KRASという遺伝子の変異が駆動するがんは長く治療が難しいと考えられてきました。最近、最も一般的な変異型の一つであるKRAS G12Cを遮断する新薬が患者に用いられ、その状況は変わりつつあります。本稿はさらに意欲的な問いを探ります:細胞内でKRAS G12Cが働く主要な二つの状態の両方を阻害できる薬を設計できるか、そのことはがん治療をより速く、より強く、あるいはより持続的にできるだろうか?
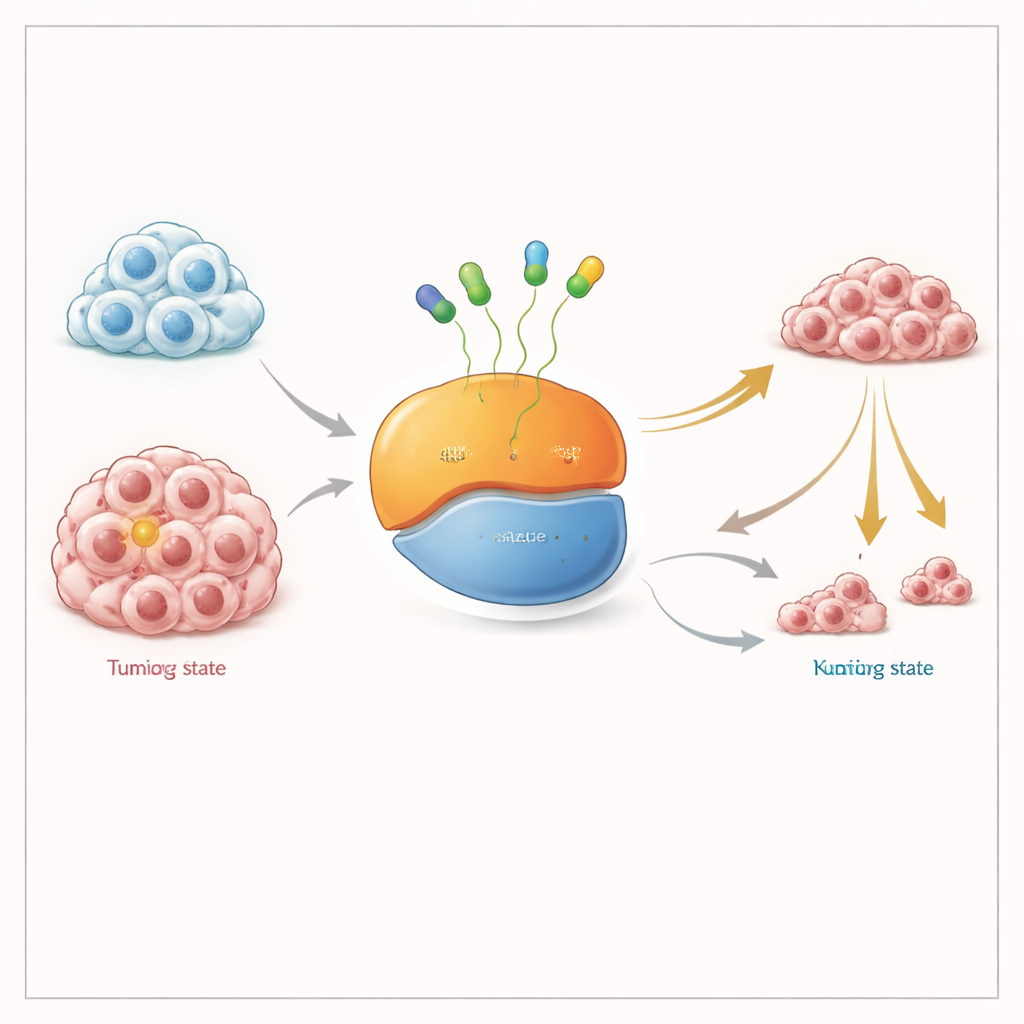
分子スイッチを二か所でオフにする
KRASは細胞成長シグナルの微小なオン/オフスイッチのように振る舞います。オフ状態ではGDPという分子を保持し、オン状態ではGTPを保持します。KRAS G12C変異はこのスイッチを部分的にオンに固定し、腫瘍成長を助長します。既存のFDA承認薬は「オフ」型に結合してそれをロックします。時間が経つと、より多くのKRAS分子がその形を経由するため、変異タンパク質の総プールが機能不全に陥ります。多くの研究者は、KRASをオン型とオフ型の両方でつかめる薬はより効果的であるはずだ、と主張してきました。特に腫瘍がより多くのKRASをオン状態に保つことで適応する場合にそうです。
新しい種類の分子フックの設計
著者らはそのような二重用途の薬を作ることを目指しました。彼らは現行の薬が既に結合する、Switch IIと呼ばれる柔軟な領域の近くにある小さな溝に注目しました。分子がその溝にどれだけしっかり収まるかを変える代わりに、変異した12位のシステインに永久的な化学結合を形成する「ウォーヘッド」部分を再設計しました。コンピューターモデリングと数十のバリアントの合成を通じて、彼らはシステインにやや異なる角度から近づく特別な三部分からなるウォーヘッドを発見しました。この微妙な位置のずれにより、よりかさばるGTP分子のための余地が生まれ、新しい化合物はKRASがGDPを結んでいる時もGTPを結んでいる時も結合できるようになりました。生化学的試験は、候補化合物が両方の状態でKRASと主要なシグナルパートナーであるRAFとの結合を妨げられることを確認しました。
タンパク質が自身をどのように再配列するかを見る
これらの分子がなぜ機能するのかを理解するため、チームは薬がKRASに結合した高分解能の結晶構造を決定しました。これらのスナップショットは、新しいウォーヘッドが化学骨格の異常な部位で反応し、フッ素原子を切り離して、システインを標的とする典型的な抗がん薬とは異なる炭素に共有結合を形成することを示しました。この変化した化学が、GTPが存在する場合でも薬がSwitch IIポケットに収まる助けになっています。構造解析はまた、阻害剤が結合すると小さな水分子を押しのけ、下流のシグナルタンパク質と通常接触する別のループであるSwitch Iをわずかに再配列させることを明らかにしました。こうしたアロステリックな再配列により二つのアミノ酸残基が引き寄せられて強い塩橋が形成され、表面が歪んでRAFが結合して成長シグナルを伝達できなくなります。
迅速なシャットダウン、しかし長期的な効果の増強はなし
これらの構造的知見に基づき、研究者らはKRAS G12Cに効率的かつ選択的に共有結合する二つのリード分子を洗練しました。他のシステインをもつタンパク質には概ね影響を与えませんでした。がん細胞株では、これらの二重状態阻害剤はMAPK経路として知られる重要なシグナル中継を速やかにブロックし、ERKタンパク質上の化学的なタグの消失や細胞増殖の強い抑制として測定されました。これらは非活性状態のみを標的とする比較薬よりも細胞内でKRASをより迅速に不活化しました。マウス腫瘍モデルでは、あるリード化合物が経口利用性に優れ、迅速に共有結合を形成して標的を修飾し、腫瘍縮小や増殖抑制を示しました。しかし、チームが二重状態化合物と非活性状態化合物を長期間比較したところ、最終的には両クラスともKRASのシャットダウン、経路抑制、腫瘍制御のレベルは類似に達しました。
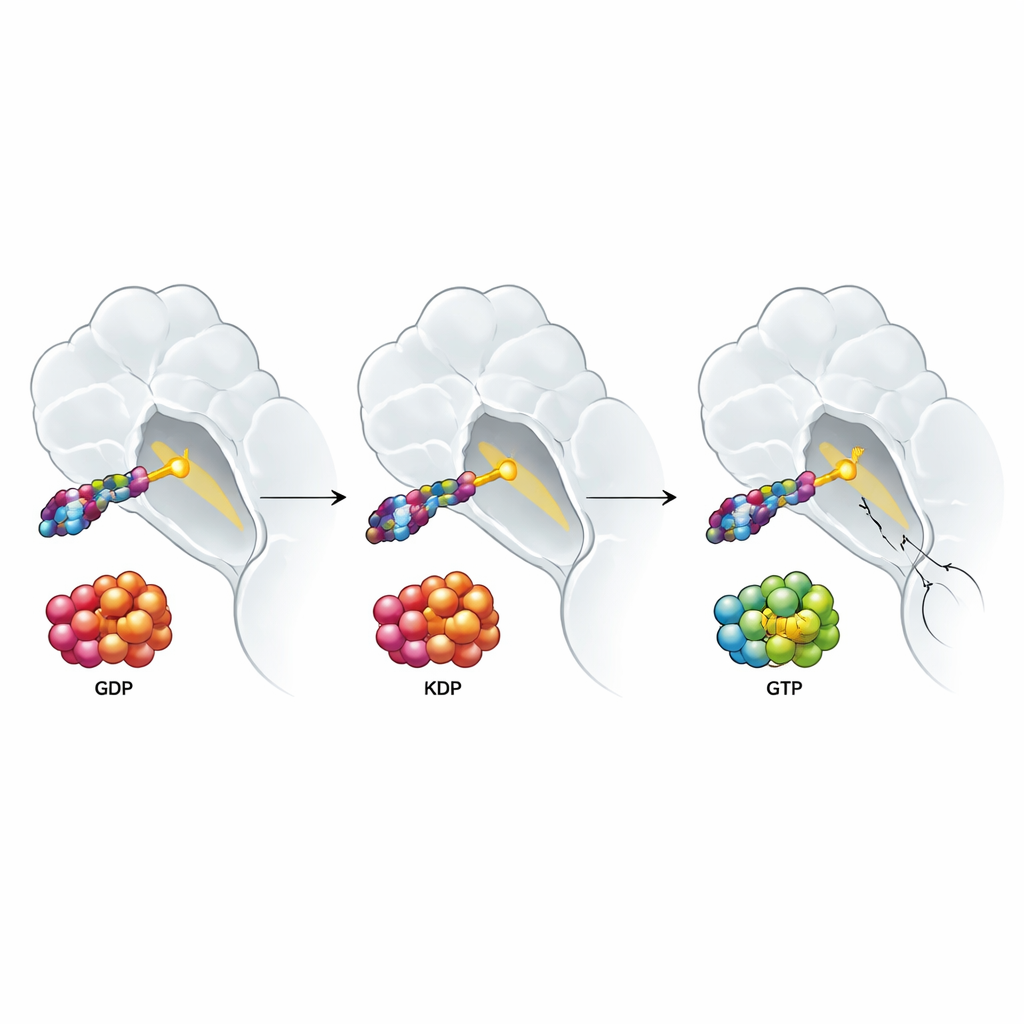
なぜ腫瘍周辺の成長シグナルが依然として勝つのか
研究はまた、腫瘍環境からのシグナルがこれらの薬にどのように影響するかを調べました。多くの腫瘍周辺に豊富に存在するEGFやHGFといった成長因子は、RASタンパク質を活性なGTP結合型に押しやり、標的治療への応答を鈍らせることが知られています。KRAS G12Cの活性型に結合する薬ならこの問題を回避できると予想されるかもしれません。ところが著者らは、二重状態阻害剤も非活性状態阻害剤も、こうした成長因子の存在下では効力を失うことを見出しました。詳細な実験は、驚くべき原因を示しました:正常な非変異型のRAS(H‑RASおよびN‑RAS)の活性化であり、これらがKRAS G12Cを回避して成長シグナルを流し続けることができるのです。研究者らが肺がん細胞株でH‑RASおよびN‑RASを欠失させると、成長因子による耐性はKRAS G12C標的薬の種類にかかわらずほとんど消失しました。一方、経路の下流段階を阻害する薬は、そもそも影響を受けにくいことが示されました。
患者と薬剤開発にとっての意味
総じて、本研究は共有結合型のKRAS G12C薬をオン状態とオフ状態の両方でタンパク質に結びつけることが化学的・構造的に可能であり、これらの二重状態阻害剤が既存薬より速やかにシグナルを遮断できることを実証しました。しかし、迅速な結合は前臨床モデルにおいて明確に優れた腫瘍制御や成長因子駆動の耐性解決にはつながりませんでした。患者にとっては、単に活性型KRASへの作用を追加するだけでは十分でない可能性が示唆されます;他のRASファミリー成員や下流のシグナルノードにも対処する併用戦略が必要になるかもしれません。それでも、新しいウォーヘッドとここで示された構造的設計図はKRAS標的化のためのツールキットを拡張し、将来の世代の精密ながん治療の設計に役立つでしょう。
引用: Condakes, M.L., Zhang, Z., Danahy, D.B. et al. Covalent inhibitor design confers activity against both GDP- and GTP-bound forms of KRAS G12C. Nat Commun 17, 2233 (2026). https://doi.org/10.1038/s41467-026-69003-0
キーワード: KRAS G12C, 共有結合阻害剤, 二重状態阻害, MAPKシグナル伝達, 薬剤耐性