Clear Sky Science · ja
分子的に同定された皮質基底前頭-視床回路は雄マウスの痛みの感覚的・情動的側面を調節する
なぜこの脳回路が痛みに重要なのか
痛みは鋭い刺すような感覚や鈍い痛み以上のもので、感情への衝撃を伴い、長年にわたり気分や行動を変えることがあります。多くの慢性痛患者は現行の薬物で十分な緩和を得られず、副作用に悩まされることも少なくありません。本研究は雄マウスで、痛みの強さと不快さの両面を脳が増減させるのを助ける、精密に定義された脳回路を明らかにしました。この経路をマッピングし操作することで、従来の鎮痛薬に頼らずに慢性痛を和らげる、より標的化された新しい方法の可能性が示唆されます。
思考する脳から痛みの中枢への隠れたハイウェイ
研究者たちは、意思決定、感情、痛みの制御に関わる前頭部の領域である内側前頭前皮質と、痛みの強度と不快感の両方を形作る深部の中継センターである視床に注目しました。彼らは、Foxp2と呼ばれる遺伝子でマークされた内側前頭前皮質の特定の細胞群が、視床への主要な出力経路を形成することを発見しました。これらの細胞は主に皮質の最も深い層に存在し、特定の視床核へ長い線維を伸ばし、前頭前皮質の他の典型的な標的はほとんど無視していました。トレーシング法と全脳マッピングを用いて、これらのFoxp2でマークされたニューロンが、痛み処理に影響を与えることで知られる三つの視床領域—傍条索核(parataenial nucleus)、背内側視床(mediodorsal thalamus)、腹内側視床(ventromedial thalamus)—と強く結びついていることを示しました。 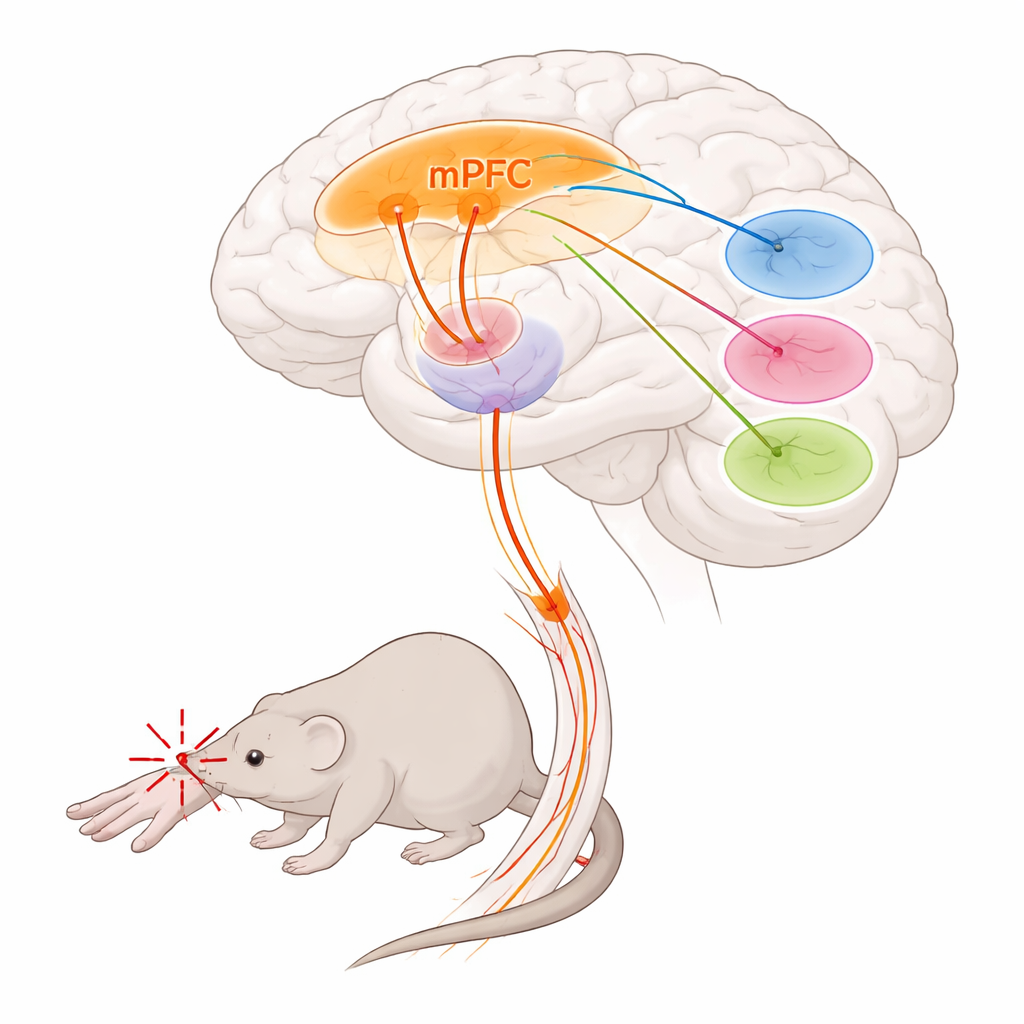
痛みが襲うとき、重要な制御センターが静まる
この経路が痛みの間にどのように振る舞うかを調べるため、科学者たちは内側前頭前皮質の上に微小レンズを埋め込み、覚醒したマウスで個々のFoxp2でマークされたニューロンの活動を記録しました。短時間の機械的挟圧、ホルマリンによる化学的痛み、長期にわたる炎症性の痛みの間、これらの細胞は一貫して活動を静めました:ほとんどの細胞が痛みの発生中および炎症後の日々に活動バーストが減少しました。この沈静化は微妙なものではなく、ある条件では3分の1からほぼ半数の細胞が著しく活動を低下させました。この発見は、急性および慢性の痛み状態が、痛みを抑えるはずの自然な前頭前皮質のブレーキシステムの沈黙を部分的に反映している可能性を示唆します。
回路をオン・オフすると痛みが再形成される
次に、研究チームはこの沈静化が単なる痛みの副作用なのか、痛みを引き起こす要因なのかを問いました。遺伝学的手法を用いて、彼らはFoxp2でマークされたニューロンの出力を長期にわたって遮断するか、短期的にその活動を増強しました。持続的な不活化はマウスの触覚・熱感受性を高め、この経路が通常は侵入する痛み信号を抑えていることを示しました。対照的に短期的な活性化は疼痛刺激の閾値を上げ、ホルマリンテストの後期の舐め行動(持続的・炎症性の痛みの指標)を減少させ、回路がオンにされた環境をマウスが好むようにして、痛みの情動的負担からの緩和を示しました。経路の特定の枝に光を当てることで、傍条索視床への投射は身体感覚の過敏性と対処行動の両方を低下させ、一方で背内側および腹内側視床への投射は主に情動的・行動的側面を調節することが示されました。これらの結果は、同じ前頭前皮質集団の異なる枝が痛み体験の異なる側面を制御する、精密に分岐した配線スキームを明らかにします。
化学的チューニング:鎮痛のためのコリン作動性ブースト
これらの前頭前皮質の鎮痛ニューロンを制御するものは何でしょうか。トレーシング実験は、水平斜帯と呼ばれる基底前脳のコリン作動性領域から強い入力があることを明らかにしました。この領域からFoxp2でマークされたニューロンに信号を送る多くの細胞は、注意や覚醒に関わる伝達物質であるアセチルコリンを使用します。このコリン作動性投射を活性化すると、機械的感受性と対処行動が低下し、炎症性過敏も緩和されましたが、痛みの否定的な情緒的トーンを明確に変えることはありませんでした。受け手側では、Foxp2でマークされたニューロンはα4β2ニコチン性受容体として知られる特定のアセチルコリン受容体型に富むことが見出されました。選択的なα4β2アゴニストを内側前頭前皮質に直接投与すると、慢性炎症状態でもマウスの熱および触覚に対する感受性が低下し、Foxp2でマークされたニューロンの活動が増強されました。これらのニューロンを遮断すると薬剤の効果は消え、 この受容体がこの細胞型を興奮させることによって特異的に鎮痛をもたらしていることが示されました。 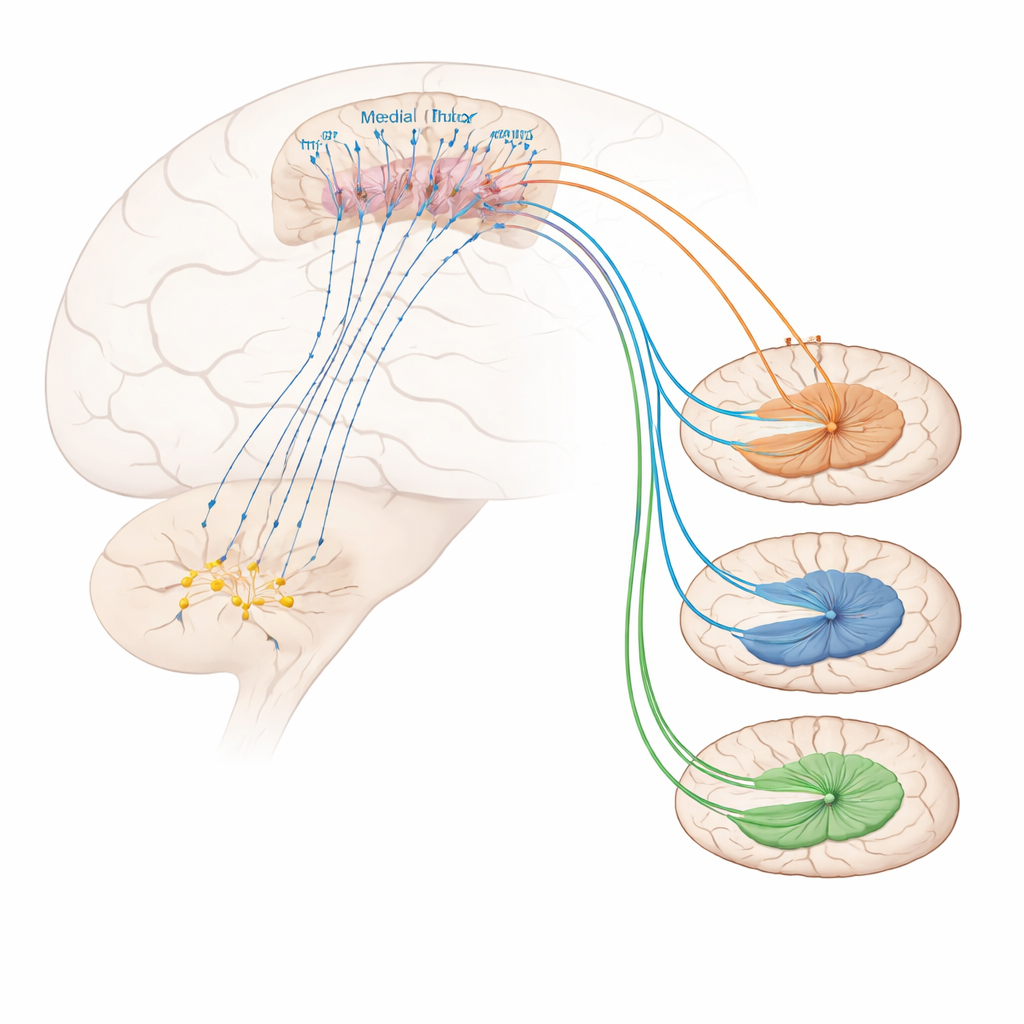
将来の痛み治療にとっての意義
日常的な言葉で言えば、この研究は三段階の正確な経路を特定しています:基底前脳のコリン作動性の“スターター”領域、内側前頭前皮質の特化した制御細胞群、そして痛みの強さ、感情的なつらさ、反応の仕方をそれぞれ別個に支配する視床の異なる中継ハブです。痛みはこの回路を低下させるように見え、直接刺激するかそのアセチルコリン受容体を標的にすることで再活性化すると、雄マウスの炎症性痛の刺すような痛みと苦痛の両方が軽減されました。これらの知見をヒトや他の慢性痛の形態に翻訳するには多くの作業が残っていますが、結果は有望な戦略を示しています:感覚をすべて麻痺させるのではなく、将来の治療は脳自身の鎮痛回路を回復または微調整して、より効果的で長期的に安全な療法を目指すかもしれません。
引用: Xie, G., Liu, Y., Qi, X. et al. A molecularly defined basalo-prefrontal-thalamic circuit regulates sensory and affective dimensions of pain in male mice. Nat Commun 17, 2134 (2026). https://doi.org/10.1038/s41467-026-69001-2
キーワード: 慢性痛, 内側前頭前皮質, 視床, コリン作動性シグナル伝達, ニコチン性受容体