Clear Sky Science · ja
HaloTag技術に触発されたグルタミン酸の共有結合修飾
タンパク質の「アンカー」を薬物標的に変える
多くの現代的ながん治療薬は、細胞内のタンパク質に結合して作用します。しかし、最も重要なタンパク質の中には、薬がつかめる明確な“取っ手”を持たないものが多くあります。本研究は、広く使われる実験ツールであるHaloTagに着想を得た巧妙な化学的工夫を導入し、通常は到達が難しいタンパク質上の部位に結合する方法を示しています。その部位はがんに関連する増殖シグナルを制御する働きを持ち、この手法は腫瘍を駆動する経路をより持続的に遮断する新たな薬開発の道を開く可能性があります。
なぜほとんどの共有結合薬は同じ部位を狙うのか
ここ数年、いわゆる標的共有結合薬は注目される薬のクラスとなってきました。これらは穏やかに反応性のある化学基を持ち、タンパク質の特定のアミノ酸と永久的な結合を形成して薬を固定します。ほとんどの薬は比較的まれで反応性の高いシステインを標的にします。一方で、アスパラギン酸やグルタミン酸ははるかに一般的で、タンパク質の形状や機能に重要なことが多いにもかかわらず、その酸性のカルボキシラート基は細胞内の水性環境では反応性が低く、選択的に修飾するのが難しいのです。そのため、グルタミン酸やアスパラギン酸を狙った共有結合薬の成功例はこれまでごくわずかでした。
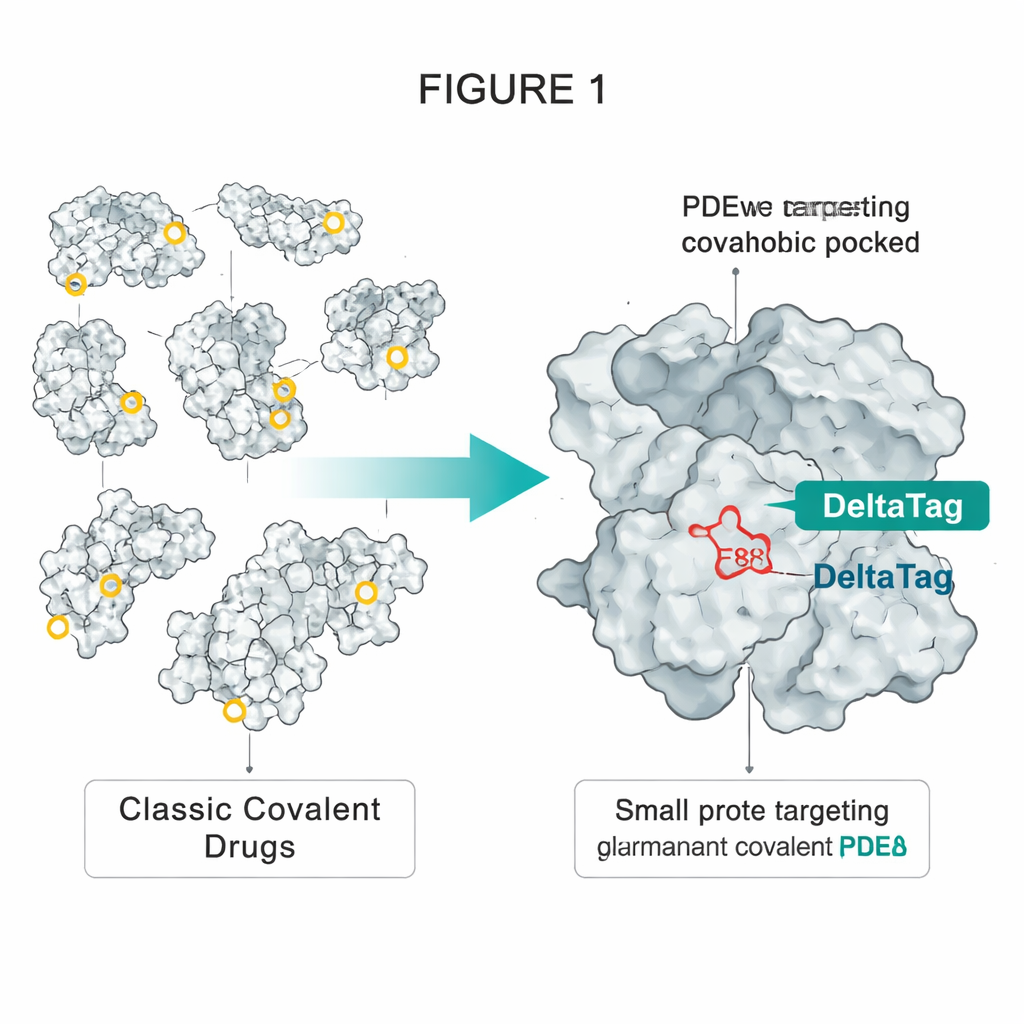
HaloTag技術からのトリックの借用
著者らは、蛍光色素で恒久的に標識できるように設計された広く用いられる工学的タンパク質であるHaloTagに着想を得ました。HaloTagでは、疎水性ポケットの奥に配置された特定のアスパラギン酸が、色素上の単純なクロロアルカン鎖と反応して安定なエステル結合を形成します。研究チームは、別のタンパク質であるPDEδにもやや似た疎水性ポケットがあり、そこにアクセス可能な単一のグルタミン酸(E88)が存在することに気付きました。PDEδはRhebなどの脂質修飾されたシグナルタンパク質を細胞内で輸送し、これらをmTORC1のような成長促進複合体が活性化される膜へ導きます。以前の非共有結合型PDEδ阻害剤はこのシャトルを阻害できましたが、別のタンパク質Arl2が時間とともに阻害剤をポケットから引き離してしまうため、その効果は限定的でした。
グルタミン酸に鍵をかけるDeltaTagの設計
この「押し出し」問題を克服するため、研究者らは既知の高親和性PDEδ阻害剤を出発点として、その側鎖の一つをHaloTag配位子で使われるようなハロアルカン“ウォーヘッド”を運ぶように再設計しました。タンパク質の結晶構造に基づく数回の構造的調整を経て、彼らはDeltaTagと呼ばれる化合物に到達しました。主な特徴は、フェネチルブロミド基が配置されており、分子がPDEδの脂質ポケットに収まると、ブロミドがE88と反応するよう精密に整列する点です。生物物理学的測定と高分解能X線構造解析により、DeltaTagがこのグルタミン酸と特異的に共有結合性のエステル結合を形成し、PDEδ上の他の潜在的により反応性の高いアミノ酸は触れられていないことが確認されました。化合物はタンパク質を効率的に標識するのに十分反応性がありながら、水中や主要な硫黄系抗酸化物質であるグルタチオン存在下でも安定で、広範で無差別なダメージを避けられるものでした。
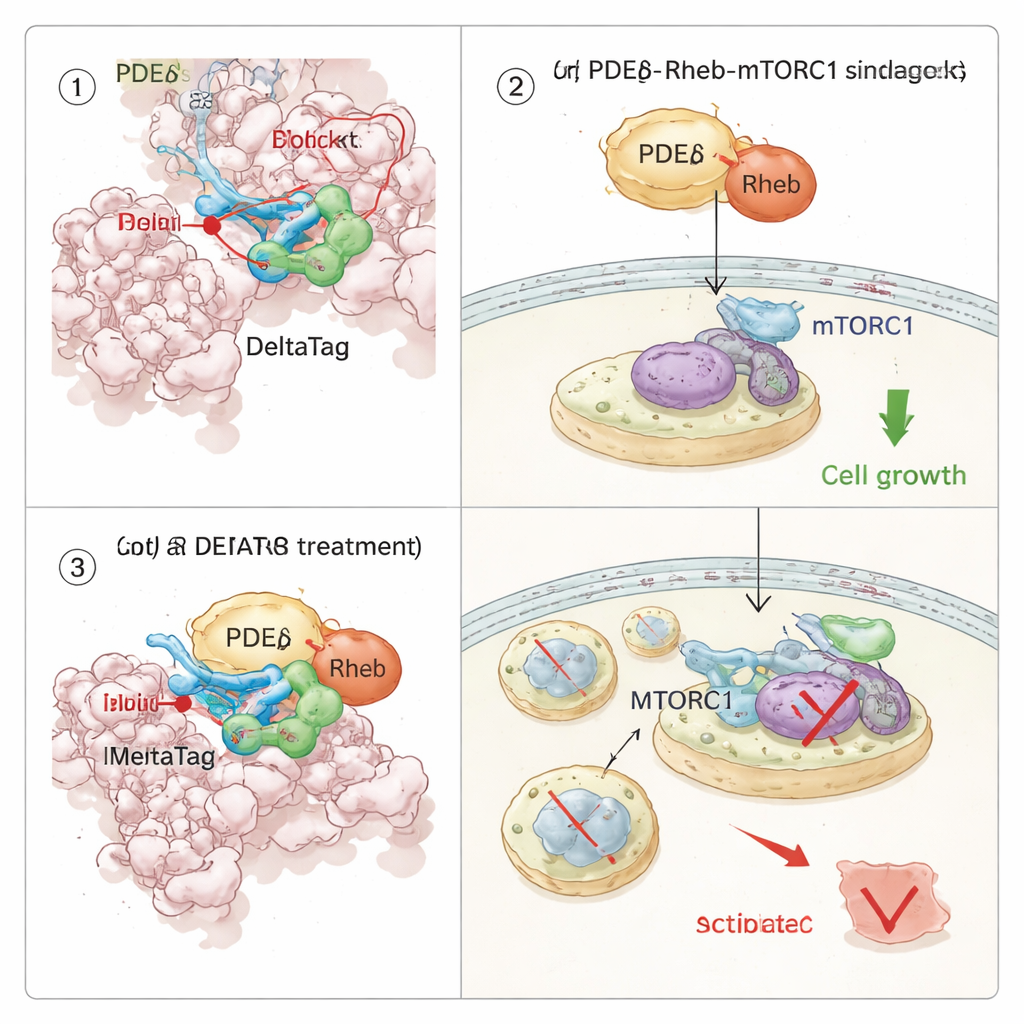
がん細胞内で増殖経路を書き換える
PDEδはRhebをシャトルするため、RhebはmTORC1増殖経路をオンにすることから、研究チームはPDEδの共有結合阻害が細胞シグナル伝達にどのように影響するかを調べました。数千のタンパク質を横断する熱安定性プロファイリングを用いて、DeltaTagが細胞抽出液中で選択的にPDEδに結合し、Rheb–mTOR軸に関連するタンパク質に摂動を与えることを示しました。生細胞イメージング実験では、DeltaTagによりRhebは細胞内の拡散状パターンからより集積した内部膜へ再配置され、通常のシャトルが乱されていることと一致しました。グローバルなホスホプロテオミクスと特定のウェスタンブロット解析は、リボソームタンパク質S6のリン酸化で追跡されるmTORC1活性が時間とともに低下し、関連する経路で補償的なシグナルが上昇することを明らかにしました。重要なことに、変異KRASで駆動され強いmTORシグナルを必要とするいくつかのヒトがん細胞株において、DeltaTagは密接に関連する可逆的阻害剤よりも細胞増殖をより効果的に遅らせ、PDEδを欠く細胞では影響が弱かったことから、その主要な作用がオンターゲットであることが支持されました。
新たな種類の薬物標的への扉を開く
本研究は、HaloTagから借用した比較的単純なハロアルカン化学を用いて、タンパク質の疎水性ポケットに埋もれた単一のグルタミン酸に対して、永久的かつ高選択的な結合を形成する小分子を構築できることを示しています。モデル系であるPDEδでは、その共有結合リンクにより従来の可逆的薬剤よりもがんに関連する増殖経路の遮断がより持続的になります。より広い観点では、戦略的に配置されたグルタミン酸またはアスパラギン酸を有する限り、疎水性空洞を持ち通常の「反応性」アミノ酸を欠く他のタンパク質にも同様の設計論理を適用できる可能性があります。さらなる最適化が進めば、DeltaTagのようなグルタミン酸標的の共有結合阻害剤は化学生物学の有用なツールとなり、最終的には現状では薬剤化が難しいタンパク質に対処する新規治療法のリード化合物となるかもしれません。
引用: Zhang, R., Liu, J., Gasper, R. et al. Covalent modification of a glutamic acid inspired by HaloTag technology. Nat Commun 17, 1257 (2026). https://doi.org/10.1038/s41467-026-68999-9
キーワード: 共有結合阻害薬, グルタミン酸ターゲティング, PDEδ, mTORシグナル伝達, がん薬設計