Clear Sky Science · ja
異なる二重膜非対称性を持つ膜内ドメインを備えた合成細胞の設計
なぜ小さな合成バブルが重要なのか
すべての生細胞は、賢く柔軟な皮膚のように振る舞う膜に包まれています。この“皮膚”は均一ではなく、内側と外側、さらには表面の異なる斑点でさえ組成や形状が大きく異なることがあります。これらの差は細胞がシグナルを送ったり、タンパク質を結合したり、分裂したりするのに役立ちます。しかし、この複雑さを再現する単純で制御可能なモデル膜を作ることは著しく困難でした。本研究は、両側で非対称かつ側方にパターン化された領域をもつ細胞サイズの「合成細胞」を実用的に作る方法を紹介し、より現実的な細胞模倣体の構築や膜パターンが芽生えや分裂をどのように駆動するかを研究する道を開きます。 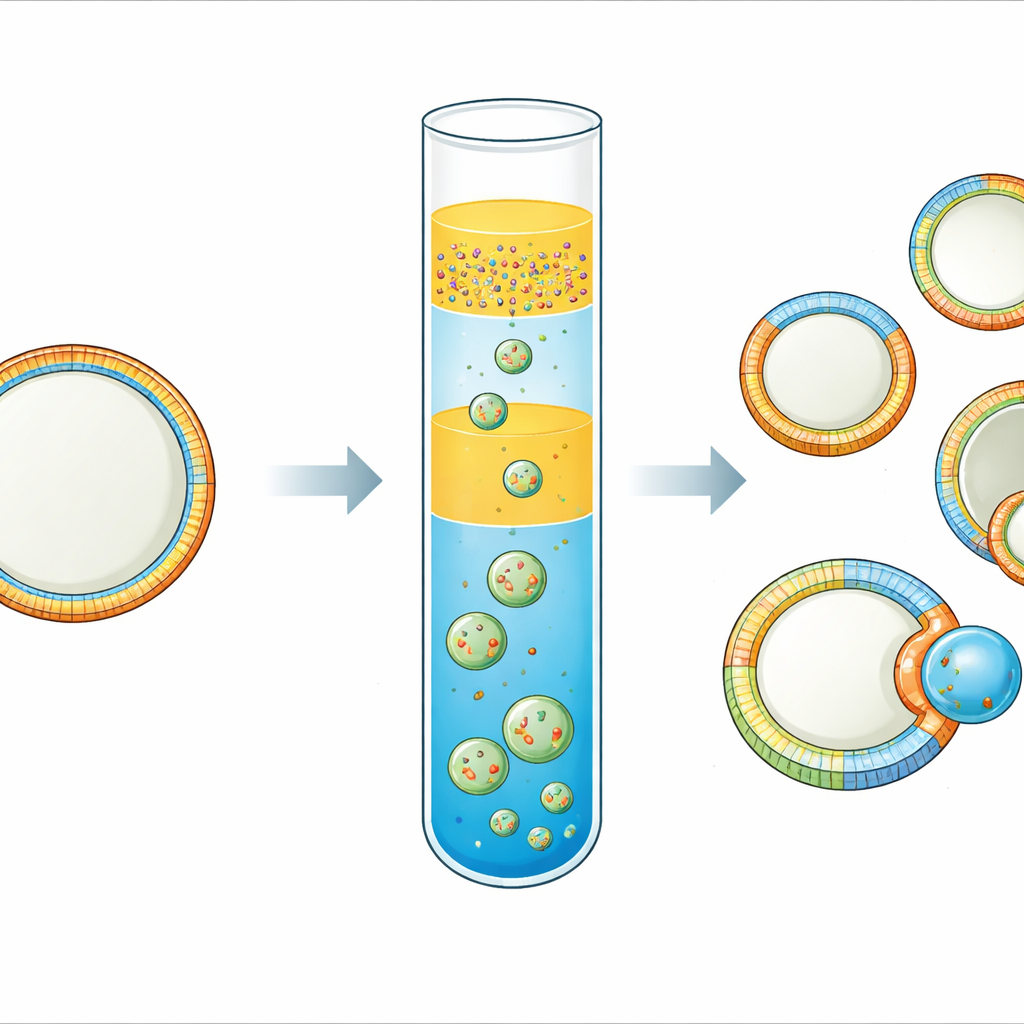
より良い細胞模倣体の構築
実際の細胞膜は非対称です:内側は負に帯電した脂質が豊富でシグナル伝達タンパク質を引き寄せる一方、外側は細胞間認識を仲介する異なる脂質を持ちます。多くの実験手法で巨大小胞—脂質でできた中空の球—を作れますが、通常その両葉は同一になりがちで、内部へのアクセスも難しいです。非対称性を生む他の手法は複雑な装置や特殊な脂質を必要としたり、小胞が基板に貼り付いてしまうことが多い。著者らは、高いバイオ分子の封入性と、生細胞に近い堅牢で調節可能な非対称性を兼ね備えた、自由に浮遊する細胞サイズの小胞を作ることを目指しました。
非対称膜のための三層レシピ
研究チームは「逆乳化」技術を改良しました。これは脂質で覆われた微小な水滴を油–水界面に通過させて小胞を形成する方法です。彼らの主要な革新は三層の油相構成です。底層には外葉用の脂質を含む油を置き、その上に脂質を含まない薄いスペーサー油を置き、さらにその上に内葉用の脂質を運ぶ第二の油中の乳化水滴を置きます。短時間の遠心工程で、水滴はスペーサーと底層を通過して二重の脂質被膜を獲得し、小胞として閉じます。密度の異なる二種の油を選び、スペーサーを挟むことで脂質プール間の混合が大きく抑えられ、内側と外側の葉は異なる組成を保持します。
両側が本当に異なるかを検証する
葉が実際に異なるかを確認するため、研究者たちは化学的およびタンパク質ベースの指標を用いました。ある実験では、蛍光脂質を片方の葉だけに加え、外側溶液中の膜を通過できない消光剤で曝露しました。蛍光脂質が外側にあるときは信号がほとんど消えましたが、内側にあるときはほとんど変化せず、大部分の標識脂質が意図した側に留まっていることを示しました。別の実験では、ビオチン標識脂質(ストレプトアビジン用)やHisタグ付きGFPが結合する特殊なヘッドグループなど、特定のタンパク質に結合する脂質を片方の葉だけに配置しました。反対側の区画(内側または外側)にタンパク質を加えると、それらは対応する脂質が同じ側にある場合にのみ結合し、強い非対称性とタンパク質機能の保持を裏付けました。
ラフトを作り膜の芽生えを観察する
実際の細胞膜には「ラフト」と呼ばれる微小領域があり、コレステロールやスフィンゴミエリンなどの特定脂質が濃縮してタンパク質をクラスタリングし形状に影響を与えます。逆乳化法でこのような相分離を達成するのは、コレステロールが油に溶け込みやすく膜に入りにくかったため困難でした。底層の油にスクアレンを使うことで、標準的な鉱物油よりコレステロールを保持しにくくし、液相秩序領域(liquid-ordered)と液相非秩序領域(liquid-disordered)が共存する膜を再現性よく形成できるようになりました。次に、この側方パターンと葉の非対称性を組み合わせ、一方のドメインは内側葉にストレプトアビジンを結合するリガンドを持ち、別のドメインは外側でコレラ毒素を結合する糖脂質を持つようにしました。 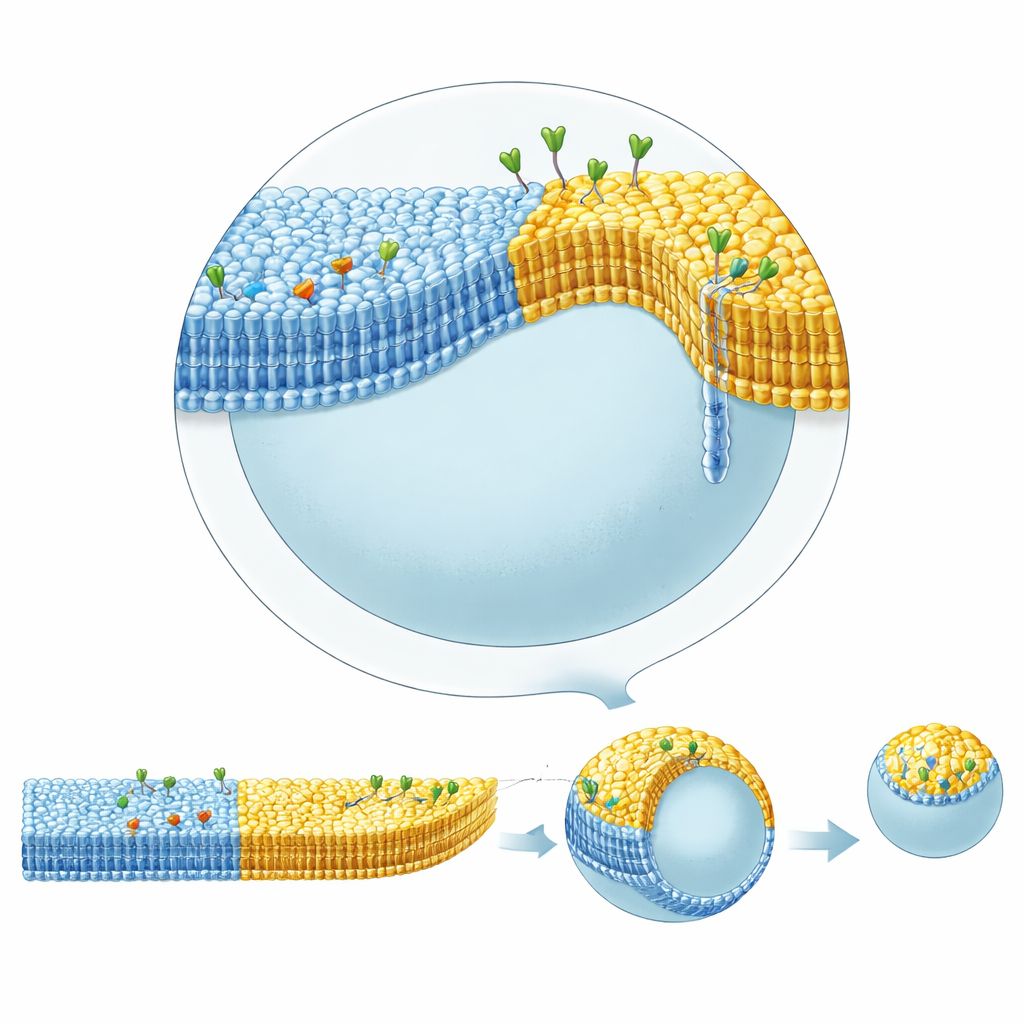
タンパク質とパターンが形状変化を駆動する仕組み
これらの複雑な小胞は顕著な形状ダイナミクスを示しました。外側の秩序領域にある糖脂質にコレラ毒素が結合すると、その領域は狭いネックでつながれた外向きの曲がりをもつ芽(バッド)として膨らみ、わずかな浸透的脱水で完全に娘小胞として切り離されることがありました。この芽生えはATPのようなエネルギー担体や特殊な分裂機構を必要とせず、脂質組成、ドメイン境界、非対称なタンパク質結合の相互作用だけから生じました。内側の非秩序ドメインに結合したストレプトアビジン量を増やすと、秩序ドメインの外向き曲率を相殺して徐々により球状の形に戻すことができました。小胞輪郭の詳細な幾何学的解析は、膜の曲率がドメイン間の境界で急変すること、そして芽生えの際に閉じる狭いネックが少なくとも数十ピコニュートンの力に耐える必要があることを示し、ドメイン構造とタンパク質クラウディングが膜を力学的に形成する様を定量化しました。
将来の合成細胞にとっての意義
平易に言えば、著者らは現実の細胞膜に近い形で二面性とパターンを備えた柔らかい細胞サイズの泡を作るためのレシピを開発しました。方法は比較的単純で多くの異なる脂質に適用でき、タンパク質や他の大きな分子を内部に封入できるため、ボトムアップでより生きたような人工細胞を構築する道を開きます。こうした合成細胞は、膜パターンがシグナル、輸送、分裂をどのように制御するかを分解して研究する助けになり、最終的には体内で形を変えたり分裂したりするスマートな薬剤担体として利用される可能性があります。
引用: Yandrapalli, N., Seemann, T., Lipowsky, R. et al. Engineering synthetic cells with intramembrane domains possessing distinct bilayer asymmetries. Nat Commun 17, 2620 (2026). https://doi.org/10.1038/s41467-026-68997-x
キーワード: 合成細胞, 脂質膜, 膜の非対称性, 相分離, 膜の芽生え