Clear Sky Science · ja
コアフコシル化抑制のための共有結合阻害剤によるヒトフコシルトランスフェラーゼ8のアロステリー性の活用
小さな糖を遮断することががんにとって重要になる理由
細胞は常にタンパク質に短い糖鎖を付加して、その働きを微調整しています。中でも「コアフコシル化」と呼ばれる糖修飾は、腫瘍の成長、転移、免疫回避、さらには現代のがん治療薬に対する抵抗性に寄与します。本論文は、この糖を付加するヒト酵素に存在する隠れた制御点を見つけ出し、その制御点に結合して酵素を不活化する新しい低毒性分子を設計した研究を報告します。彼らの成果は、DNAやタンパク質を直接攻撃するのではなく、細胞表面の糖パターンを巧妙に書き換える薬の新たな道筋を開きます。
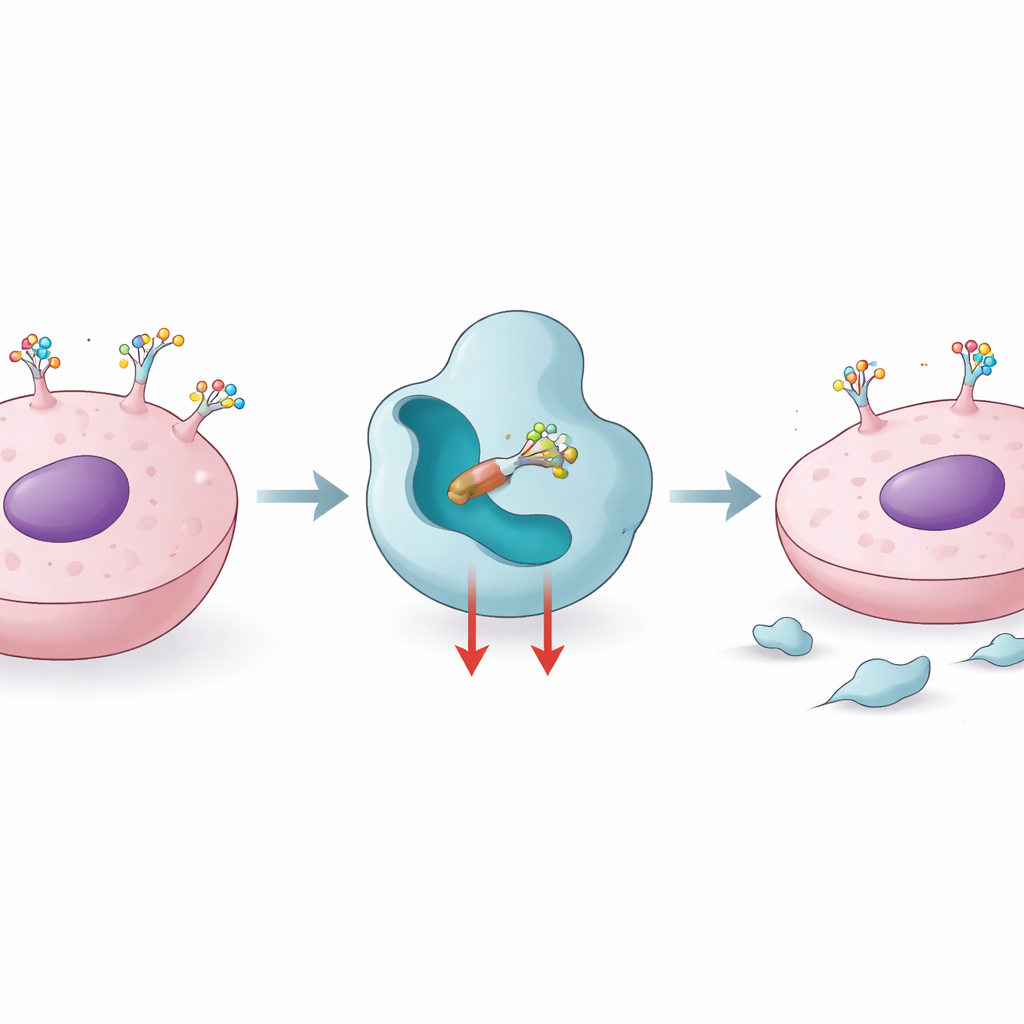
細胞が糖タグを使って病態を形作る仕組み
細胞内で合成されたタンパク質は、糖鎖が付加・編集される分子レベルの「仕上げライン」を通過します。コアフコシル化はその一例で、FUT8という酵素が多くのタンパク質に付いた糖鎖の特定位置に単一のフコースを付加します。FUT8の発現や活性が上がると、細胞増殖、運動、免疫認識を制御する分子上でこの糖修飾が増えます。研究は、FUT8の高活性を悪性黒色腫、トリプルネガティブ乳がん、肺がん、標的薬や一部抗体療法への耐性と結びつけています。FUT8を阻害することで、PD‑1のような免疫ブレーキタンパク質が細胞表面から除かれ、腫瘍が免疫系に対してより可視化されるため、FUT8はがん免疫療法や生物学的製剤の改良の魅力的な標的となります。
より賢く選択的な阻害剤の必要性
FUT8に対する薬剤設計が難しかった理由は、多くの関連酵素が同じ基本的な糖の基質を用いることにあります。これまでの阻害剤の多くはその基質を模倣しており、広範で非選択的なフコシル化経路の停止と、臨床試験を中止させた凝固障害などの望ましくない副作用を引き起こしました。著者らは、混雑した主要な基質結合部位を避け、むしろFUT8上のユニークな“遠隔”部位を制御スイッチとして探す方が良い戦略だと考えました。酵素活性をモニターするハイスループットスクリーニングを用いて6000超の化合物をふるいにかけ、FUT8活性を低下させると同時に培養皿上でがん細胞の浸潤を抑える鎖状分子をいくつか特定しました。
隠れた制御ポケットの発見
X線結晶構造解析を用いて、研究チームはFUT8が2つの阻害剤と結合した三次元構造を解きました。驚いたことに、どちらの化合物も糖供与体や受容体が結合する通常の部位には位置していませんでした。代わりに、酵素の二つの主要なローブの間に伸びる長くチャンネル状のポケットに収まり、活性中心には近いが別個の位置を占めていました。この部位への結合は、特に糖供与体を把持するのに重要なループやアミノ酸残基を押しのけるように作用しました。計算機シミュレーションは、このポケットが満たされるとFUT8の全体的な運動とエネルギー地形が変化し、触媒反応に不利な形状を好むことを示しました。言い換えれば、これらの阻害剤はアロステリックに働き、遠位のスイッチを押すことで酵素の作動部分の位置関係を乱していたのです。
ヒット分子を精密な共有結合ツールに変える
この構造マップを手掛かりに、研究者たちはポケットに占有するだけでなく、自然にそのチャネル側へ振れる近接リジン残基(K216)に永久的に結合できる分子を探しました。反応性のあるN‑ヒドロキシスクシンイミドエステルを含む試薬SSOが同じ溝に結合し、K216と共有結合を形成して酵素を不活性状態に固定することを見出しました。SSOと初期ヒットであるNH125の共通特徴を基に、両者の断片を融合してCAIFと名付けた新分子を設計しました。結晶構造はCAIFがチャンネルに沿って貫通し、疎水性残基の間にきつくフィットし、K216と共有結合を作ることを確認しました。この設計により、親化合物に比べてFUT8阻害が数倍向上し、関連酵素への影響は抑えられ、FUT8のアロステリックポケットの独特な形状が浮き彫りになりました。
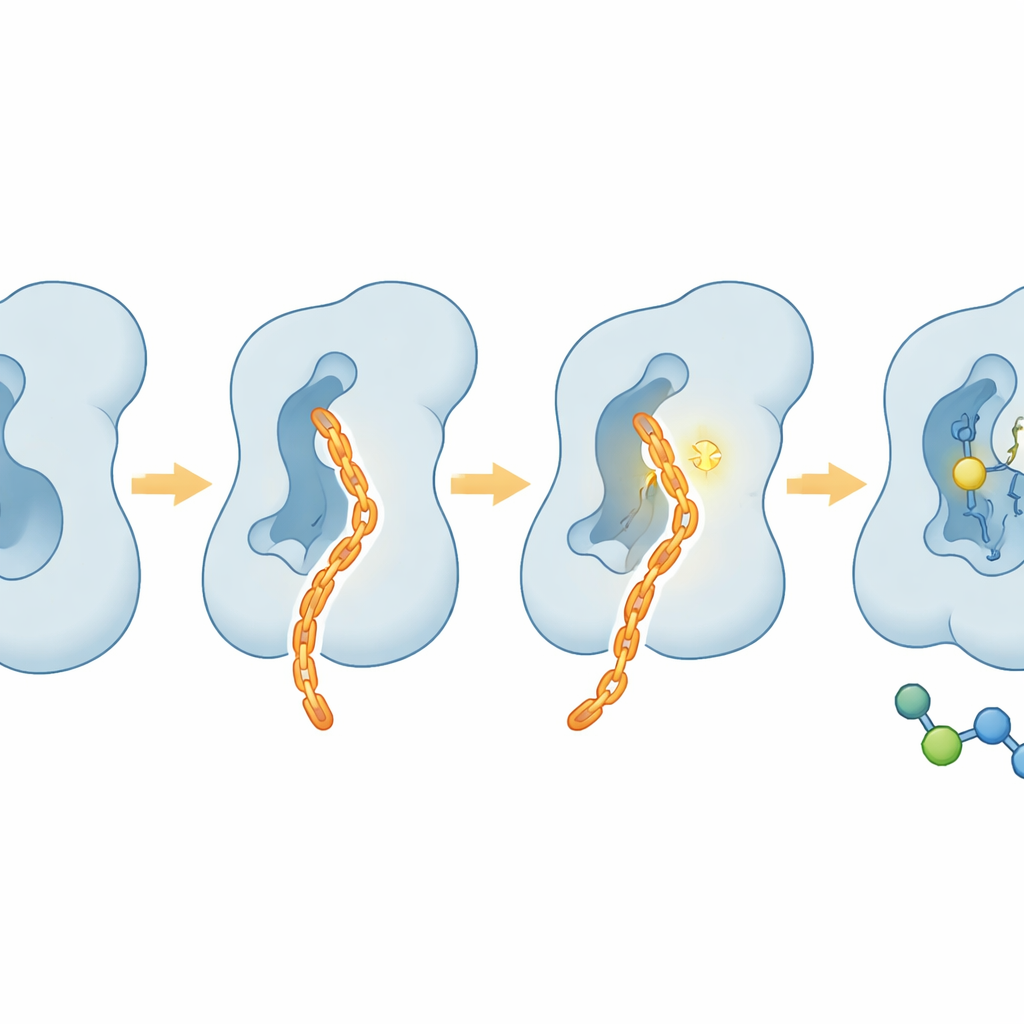
細胞には優しく、腫瘍挙動には厳しい
試験管外の実験を越えて、チームはCAIFが生細胞内でどのように振る舞うかを調べました。複数のヒト細胞株で、CAIFは高濃度でも毒性がごくわずかであり、細胞の基本的な機構を広く毒するものではないことを示しました。それでも糖結合色素で明らかになったように、細胞表面のコアフコシル化は著しく低下し、従来の汎用阻害剤よりFUT8に対してはるかに高い選択性を示しました。がん細胞の浸潤アッセイでは、CAIFは一般的に用いられる糖ベースの阻害剤よりも行動上の指標であるマトリックスを通る細胞移動を抑制し、転移能の抑制で優れていました。これらの効果は、FUT8が直接的に細胞分裂を駆動するのではなく、浸潤や免疫回避を促進するという既知の役割と整合します。
将来のがん治療にとっての意義
本研究がCAIF自体をすぐに薬として使えると主張するものではありません。むしろ、FUT8にはこれまで知られていなかった創薬可能なアロステリックポケットが存在し、単一のリジンに対して耐久的な結合を形成する慎重に形作られた分子で標的化できることを実証した点に意義があります。この部位を利用することで、がんの進行、免疫逃避、薬剤耐性の交差点に位置する糖修飾酵素を選択的に抑えることができ、関連酵素を大きく手つかずのままにできます。本研究は、疾患関連タンパク質上の糖パターンを再設計する次世代阻害剤の設計図を提供し、最終的にはがん免疫療法や改良された抗体医薬のツールキットを広げる可能性を秘めています。
引用: Jiang, J., He, D., Ke, M. et al. Exploiting human fucosyltransferase 8 allostery with a covalent inhibitor for core fucosylation suppression. Nat Commun 17, 2607 (2026). https://doi.org/10.1038/s41467-026-68971-7
キーワード: FUT8阻害, コアフコシル化, 共有結合性アロステリック阻害剤, がんのグリコシル化, グリコシルトランスフェラーゼ創薬設計